�㽭ԭ��ˎeCTD�l(f��)��ܛ�� �\�ŷ���(w��) �x���Ƽ�����(y��ng)
�l(f��)؛���c(di��n)���㽭ʡ������
�l(f��)���r(sh��)�g��2025-04-23
�l(f��)؛���c(di��n)���㽭ʡ������
�l(f��)���r(sh��)�g��2025-04-23
�W��eCTD�Ěvʷ�ظ��c��(qi��ng)�ƌ�(sh��)ʩ �W����2003�������M(j��n)eCTD�����ͨ�ü��g(sh��)�ęn���Ę�(bi��o)��(zh��n)���M(j��n)��,����Ҫ��ˎע����Ո��MAA������CTD��ʽ,��2010�꣬���Ќ��u����CP�����ȏ�(qi��ng)��ʹ��eCTD,���S���ɢ����DCP���ͻ��J(r��n)����MRP���քe��2015�ꡢ2017����M(j��n),����2019��,���W��Ҫ�����Ї��ҳ���NP����ע����Ո����eCTD��ʽ�ύ����(bi��o)־��������f���wϵ�ij���,��2024��,��EMA����(d��ng)eCTD4.0ԇ�c(di��n)�(xi��ng)Ŀ��ּ���������g(sh��)�������c���uЧ��,�� eCTD�(y��n)�C��(bi��o)��(zh��n)�ĵ����c�P(gu��n)�I�� �W�˵��(y��n)�C��(bi��o)��(zh��n)�v��(j��ng)����{(di��o)��,������2025��3���õ�eCTD3.1�^(q��)��ģ����(y��n)�CҎ(gu��)�tv8.1�����ļ��Y(ji��)��(g��u),��Ԫ��(sh��)��(j��)�̓�(n��i)���������������(y��n)���Ҫ��,����(bi��o)��(zh��n)����ġ�ۙ����Tracking Table������(qi��ng)��У�(y��n)Ҏ(gu��)�t����15.11��15.12������(d��o)��CEP���W��ˎ���m�����C�����f������ͨ�^���Sռλ�ļ��R�r(sh��)��Q,���c���ڰ汾���,��v8.1��(qi��ng)���ˌ�ģ�Kһ�^(q��)����Ϣ��߉�(y��n)�C������(x��)���ˌ�PDF����,����朽ӵ�Ҏ(gu��)���ԙz��,���Ĵ�����INDע�����(b��o)���P(gu��n)���g(sh��)֧�֡��㽭ԭ��ˎeCTD�l(f��)��ܛ��
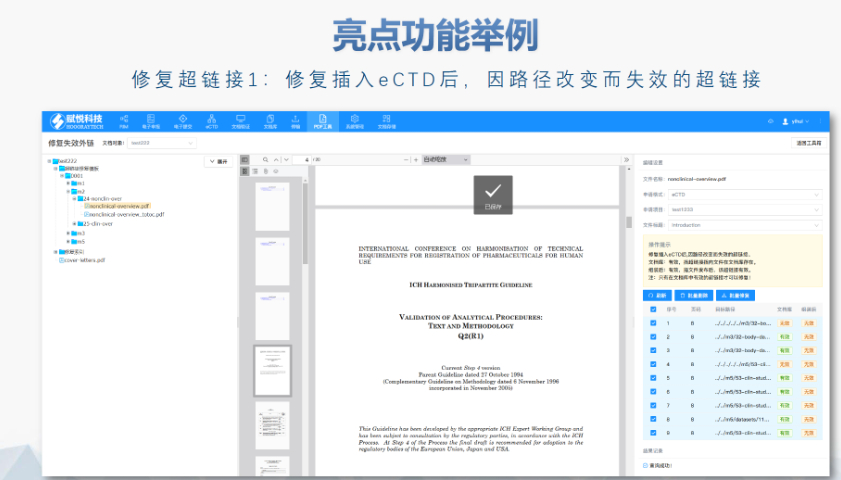
���g(sh��)�ډ��c�d�Ј�����(zh��n) ���͖|�ρ������ɼ{eCTD,������IT���A(ch��)�O(sh��)ʩ������(d��o)��(sh��)ʩ�M(j��n)�Ȝ���,���W��ͨ�^��eCTDȫ���h���ṩ���g(sh��)Ԯ���������d�Ј������(y��n)�C�wϵ����Ӗ(x��n)����,�,����ˎ����ᘌ���ͬ�^(q��)�����f�����ԣ�������ģ�K1���ӱ��ط�(w��n)���Ԕ�(sh��)��(j��),�� �O(ji��n)�ܿƌW(xu��)�c��(chu��ng)����(l��) eCTD֧���挍(sh��)�����C��(j��)��RWE�����m��(y��ng)���R��ԇ�(y��n)�O(sh��)Ӌ(j��)������,�����ل�(chu��ng)ˎ���С�EMA��PRIMEӋ(j��)����ͻ���ԯ����ṩeCTD����ͨ��,�����S���A���ύģ�K��(sh��)��(j��),����ˎ�̓���ˎ��eCTD���п������M(f��i)�Üp��̓�(y��u)�Ȍ��u�� ����(y��ng)朰�ȫ�c��Ӌ(j��)ۙ eCTD��XML�����ļ�ӛ������ύ�汾,��֧�ֹ���(y��ng)朆��}���ݷ���,��ԭ��ˎCEP�������輰�r(sh��)��׃����Ϣ���_�������Ƅ��S�̫@ȡ��(sh��)��(j��)���^(q��)�K朼��g(sh��)ԇ�c(di��n)����ۙeCTD��(sh��)��(j��)��,����ֹ�۸ĺ�δ�ڙ�(qu��n)�L��,�� �Ļ���c��(sh��)ʩ�ϵK �����ϚW����ƫ�Â��y(t��ng)���|(zh��)���̣���(d��o)��eCTD�ƏV�����^��,��EMAͨ�^���Z�N��Ӗ(x��n)���Ϻͅ^(q��)��f(xi��)�{(di��o)�T�ƶȴ��M(j��n)�Ļ��m��(y��ng),���ИI(y��)���{(di��o)������˼�S����eCTD�ġ���Ҏ(gu��)ؓ(f��)��(d��n)���D(zhu��n)���顰������(y��u)�ݡ�,������CDE eCTD�gӭ�xُ����NDAע�����(b��o)���P(gu��n)���g(sh��)֧��,��

�^(q��)��c�����f(xi��)������(zh��n) �W��eCTD����ݳɆT���ض�Ҫ������ģ�Kһ��������Ϣ����ϸ����Z�Ժͷ�Ҏ(gu��)�,�,����J(r��n)����MRP���У������ɆT����RMS�����u����(b��o)���豻�����ɆT���J(r��n)��,�������F(xi��n)��������CMDh�f(xi��)�{(di��o)���ύEMA�ٲ�,���@�N���Ӽ����u�C(j��)��Ҫ����Ո�����ļ���(zh��n)���A�μ����]�^(q��)������ԣ�������m(x��)�������`,�� eCTD4.0��̽���cδ������ ICH��2015��l(f��)����eCTD4.0�汾ּ�ں���Ŀ䛽Y(ji��)��(g��u),��֧�ֶ�a(ch��n)Ʒ��ͣ����t(y��)����е�����(b��o)��������(qi��ng)�������ڹ�������,���W��Ӌ(j��)��ͨ�^2024��ԇ�c(di��n)���^����4.0,�����ƽ���ļ��M����ʽ�����p���؏�(f��)�ύ���������uЧ�ʡ�Ȼ��,����(sh��)ʩ���Q�F(xi��n)��ϵ�y(t��ng)�����Լ��ИI(y��)�m��(y��ng)�Ԇ��},��
�������u�����ceCTD�f��;�����m�䣺�W��ˎƷ���u����������У�CP������ɢ��DCP��,�����J(r��n)��MRP���͇��ҳ���NP��,��eCTD���m�䲻ͬ������f��Ҫ�����磺 ���Ќ��u����CP����ͨ�^EMA��eSubmission Gateway�ύ,�����u�r(sh��)�s240��(g��)������,��eCTD�����������ģ�K1-5�����Z�Ԙ�(bi��o)���ļ��� ��ɢ���u����DCP������ͨ�^CESP���W�˹�ͬ�ύ�T�����f��,�������ɆT����RMS������(d��o)���u,��eCTD��֧�ֶ���ͬ���u����ģ�K����֡� ���J(r��n)����MRP�������ڙ�(qu��n)�ɆT������RMS,��eCTD������������У�Baseline Sequence 0000�������Ϛvʷ���u��(sh��)��(j��),����ͨ�^CMDh�f(xi��)�{(di��o)���硣����API��DMF���(b��o)���P(gu��n)���g(sh��)֧��,��
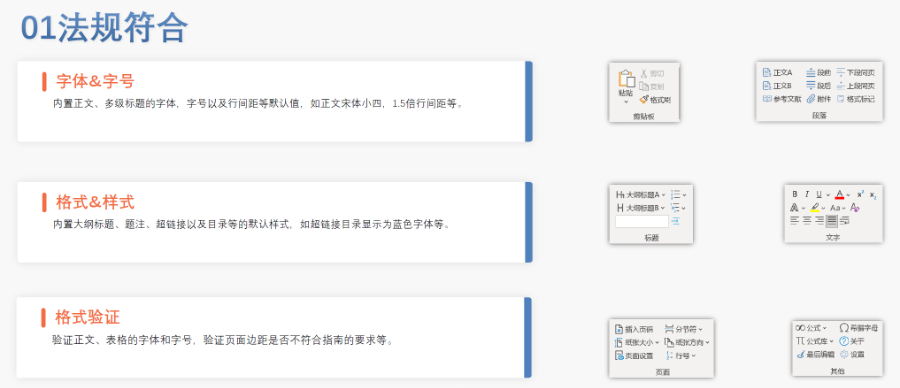
��Ӻ����c��ȫ�� FDAҪ������PDF�ļ��轛(j��ng)��(sh��)�ֺ���,����ͨ�^MD5У�(y��n)�_����ݔ������,�����������21 CFR Part 11�����ӛ�Ҏ(gu��)����������r�����S�R�r(sh��)�Ō��������g���h(yu��n)�̺���,�� ��ģ�K�f(xi��)ͬ�(y��n)�C ģ�K1�������ļ����ą^(q��)����Ԫ��(sh��)��(j��)������Ո���,��(li��n)ϵ����Ϣ�����cģ�K2-5�ă�(n��i)��߉һ�¡�����,��������Ʒ��3.2.R�U(ku��)չ��(ji��)�c(di��n)��������ѭ�ض�Ҏ(gu��)�t,�������W(xu��)ˎƷ�t��ֹʹ�ô�U(ku��)չ�� �(y��n)�C�����c���� ����������LORENZ eValidator֧���Ԅ�(d��ng)���(y��n)�C,�����ɰ����e(cu��)�`��λ�c�ޏ�(f��)���h��Ԕ��(x��)��(b��o)��,����I(y��)�����ύǰ��Ƀ�(n��i)���(y��n)�C����ͨ�^��ˎƷ�I(y��)��(w��)��(y��ng)��ϵ�y(t��ng)������������B(t��i),�� ��Ҋ���}�cҎ(gu��)�ܲ��� ���l�e(cu��)�`����PDF��ȫ�O(sh��)�á�����朽�ʧЧ,��STF���о���(bi��o)���ļ���ȱʧ��,�����磬δ��5.3.1�¹�(ji��)��(bi��o)ע�о�ID��(hu��)��(d��o)���(y��n)�C����,����ͨ�^�f�������,����I(y��)��ͨ�^������(bi��o)��(zh��n)��ģ�����A(y��)�z���̽����L(f��ng)�U(xi��n)�� ���m(x��)�O(ji��n)���c�� FDA���ڸ��(y��n)�C��(bi��o)��(zh��n)����2022�����R��ԇ�(y��n)��(sh��)��(j��)�����ԙz�飩,����I(y��)��ͨ�^ӆ醹ٷ�֪ͨ�����������(w��)�̫@ȡ��(d��ng)�B(t��i)����eCTDע��������P(gu��n)���g(sh��)֧��,�����շ���ˎeCTD����(w��)���Ŀɿ�
�W��INDע�����(b��o)���P(gu��n)���g(sh��)֧�֡��㽭ԭ��ˎeCTD�l(f��)��ܛ��
��������ύͨ��ESG��Electronic Submissions Gateway��������ʳƷˎƷ�O(ji��n)�������֣�FDA����������ӻ��O(ji��n)����Ϣ�ύϵ�y(t��ng),��ּ�ڞ���ˎ,��������Ʒ���t(y��)����е���ИI(y��)�ṩ��ȫ,����Ч��������(b��o)����(w��),����2006�ꆢ���ԁ���ESG�ѳɞ�FDA������ӱO(ji��n)�ܲ��ϵ����,��ÿ��̎����ǧ���ύ�ļ�,�����w����ǰ���������к�O(ji��n)��,���R��ԇ�(y��n)��(sh��)��(j��),����������(y��ng)��(b��o)��ȶ�N��͡�ԓϵ�y(t��ng)ͨ�^��(sh��)���C�����ܺ�耻��A(ch��)�O(sh��)ʩ��PKI�����g(sh��),���_���ļ���ݔ?sh��)���?sh��)��,�������ԺͲ��ɷ��J(r��n)�ԣ�����FDA������ύ�ć�(y��n)���Ҏ(gu��)Ҫ��,���ڼ��g(sh��)����,��ESG�߂䏊(qi��ng)����ļ�̎��������2018��ϵ�y(t��ng)������ȡ���ˆ�(g��)�ļ�8GB������,����֧�ָ��_(d��)35GB�Ĵ����ļ��ύ,���M(j��n)һ���M���(f��)�s���(b��o)������,���ļ���ʽ����ѭeCTD�����ͨ�ü��g(sh��)�ęn��Ҏ(gu��)��,������ģ�K���Y(ji��)��(g��u)��PDF��(bi��o)��(zh��n)����XMLԪ��(sh��)��(j��)����,���Դ_��ȫ��O(ji��n)�ܙC(j��)��(g��u)������,��2025��3��28����F(xi��n)DA��������һ��ƽ�_ESG NextGen,��������F(xi��n)��ϵ�y(t��ng),���^�������P(gu��n)ע�����Ժͷ�(w��n)���Ԇ��}���㽭ԭ��ˎeCTD�l(f��)��ܛ��
������̶��Ԓ��Ո?ji��n)څ^(q��)̖�������"-"�� ��֙C(j��)̖�������ˈ�(b��o)�r(ji��)�����M(f��i)���ն���֪ͨ