-
航瑞智能助力維尚家具打造自動倉儲系統(tǒng),,實現(xiàn)成品物流智能化升級
-
航瑞智能:準確把握倉儲痛點,,打造多樣化智能倉儲方案
-
高度集成化自動化立體倉庫:開啟高效物流新時代_航瑞智能
-
探秘倉儲物流中心:輸送機與RGV打造高效智能物流體系
-
共享裝備攜手航瑞智能打造砂芯智能倉儲,實現(xiàn)倉儲物流智能化升級
-
桁架機械手與輸送機:打造高效智能流水線
-
?采用WMS倉庫管理系統(tǒng)能夠給企業(yè)帶來哪些好處,?
-
?航瑞智能:精細把握倉儲痛點,,打造多樣化智能倉儲方案
-
往復(fù)式提升機:垂直輸送系統(tǒng)的智能化解決方案
-
航瑞智能:準確把握倉儲痛點,,打造多樣化智能倉儲方案
昆山抗體試劑進出口審批單
生物試劑多對運輸條件要求苛刻。許多生物試劑具有溫度敏感性,,像常見的酶,、抗體等,在運輸過程中需嚴格維持特定溫度范圍,,稍有偏差就可能導(dǎo)致試劑活性降低甚至失活,。常用冷鏈運輸方式,包括干冰冷藏,,其適用于少量試劑的短途運輸,,能維持低溫環(huán)境,但要注意干冰揮發(fā)帶來的安全問題,,確保包裝有良好通風(fēng),;低溫冷藏車則可用于大量試劑長距離運輸,車內(nèi)配備先進的制冷設(shè)備,,能精細控制溫度在規(guī)定范圍,;專業(yè)冷鏈物流服務(wù)憑借專業(yè)的設(shè)備和成熟的管理體系,為生物試劑運輸提供多方位保障,。企業(yè)要選擇具備專業(yè)資質(zhì)和豐富經(jīng)驗的運輸商,,運輸前仔細檢查設(shè)備是否正常運行,,運輸中利用先進的監(jiān)控系統(tǒng)實時監(jiān)控溫度并做好詳細記錄,確保溫度始終符合試劑儲存要求,。對于一些易氧化,、潮解或需惰性氣體保護的生物試劑,要采用合適包裝和防護措施,,例如充入氮氣等惰性氣體,防止運輸過程中試劑變質(zhì),,進而影響產(chǎn)品質(zhì)量與使用效果,。生物試劑進口時,需提前了解目的國對生物制品的準入法規(guī),。昆山抗體試劑進出口審批單

生物試劑進口的標簽與說明書必須符合國內(nèi)政策要求,。標簽應(yīng)清晰標注產(chǎn)品名稱、規(guī)格,、生產(chǎn)企業(yè),、生產(chǎn)日期、有效期,、儲存條件,、批準文號(注冊證編號)等關(guān)鍵信息,且文字表述應(yīng)準確,、規(guī)范,,使用中文(可同時標注外文)。說明書內(nèi)容要詳盡,,涵蓋產(chǎn)品組成,、適用范圍、使用方法,、注意事項,、不良反應(yīng)等信息,為使用者提供多方面指導(dǎo),。對于診斷類生物試劑,,說明書還需明確檢測原理、性能指標,、臨床預(yù)期用途等內(nèi)容,。標簽與說明書的格式和內(nèi)容需經(jīng)監(jiān)管部門審核,確保其符合《藥品說明書和標簽管理規(guī)定》《醫(yī)療器械說明書和標簽管理規(guī)定》等法規(guī),,避免誤導(dǎo)使用者,,保障患者和消費者權(quán)益。昆山抗體試劑進出口審批單生物試劑進口申報需準確填報產(chǎn)品的原產(chǎn)國信息,。
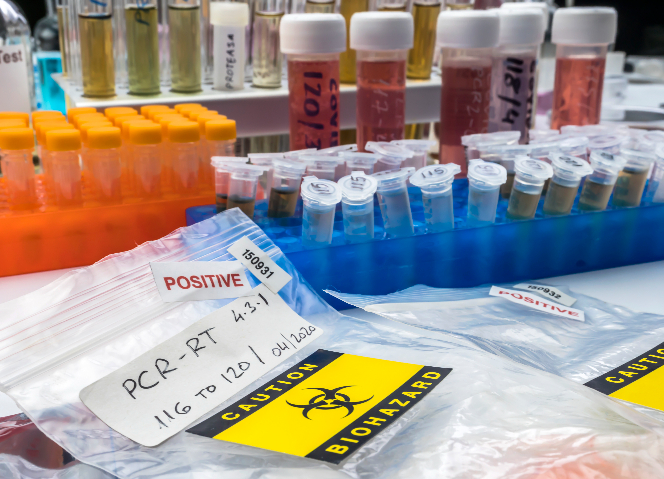
包裝對于生物試劑進出口至關(guān)重要,。從材質(zhì)選擇上,,要依據(jù)試劑特性而定。例如,,強酸強堿類化學(xué)試劑生物試劑,,需采用耐酸堿腐蝕的玻璃或特殊塑料材質(zhì)包裝,防止包裝被腐蝕而導(dǎo)致試劑泄漏,。對于有遮光要求的試劑,,像某些光敏性生物活性試劑,包裝需使用棕色玻璃或添加遮光材料的包裝容器,,避免光照引發(fā)試劑變質(zhì),。在包裝結(jié)構(gòu)方面,要確保密封性良好,,對于易揮發(fā)或需隔絕空氣的試劑,,會采用多層密封包裝,并可能添加干燥劑,、脫氧劑等輔助材料,。同時,包裝外部要有清晰,、準確的標識,,標注試劑名稱、規(guī)格,、儲存條件,、危險警示等信息,且標識要符合國際通用標準以及目標市場的法規(guī)要求,,以保障運輸,、儲存和使用過程中的安全與便利。
生物試劑進出口過程中,,完善的文件管理和記錄保存極為重要,。企業(yè)要妥善留存各類進出口相關(guān)文件,像合同,、發(fā)票,、裝箱單、提單,、報關(guān)單,、檢驗檢疫報告、資質(zhì)證書,、認證文件等,,這些文件既是通關(guān)必備,也是后續(xù)追溯業(yè)務(wù)流程、應(yīng)對監(jiān)管檢查的重要依據(jù),。同時,,企業(yè)內(nèi)部要建立詳盡記錄制度,記錄試劑從采購(生產(chǎn)),、運輸,、儲存到銷售(出口)各環(huán)節(jié)信息,例如溫度記錄,、質(zhì)量檢測結(jié)果,、操作流程等,以便及時察覺問題并采取措施,,保障整個進出口業(yè)務(wù)鏈的可追溯性與合規(guī)性 ,。生物試劑進口需嚴格遵守目的國的生物安全相關(guān)管理規(guī)定。

生物試劑進口前,,產(chǎn)品注冊是關(guān)鍵環(huán)節(jié)。按藥品管理的生物試劑,,需向 NMPA 提交注冊申請,,包含產(chǎn)品研發(fā)、生產(chǎn)工藝,、質(zhì)量標準,、臨床試驗數(shù)據(jù)(如適用)等詳細資料,經(jīng)嚴格審評審批流程,,審評中心評估產(chǎn)品安全性,、有效性和質(zhì)量可控性,審批通過后方可獲得進口藥品注冊證,。醫(yī)療器械類生物試劑注冊同樣嚴謹,,依據(jù)風(fēng)險程度分為不同類別管理。低風(fēng)險產(chǎn)品實行備案管理,,進口商向所在地設(shè)區(qū)的市級藥品監(jiān)督管理部門提交備案資料,;中、高風(fēng)險產(chǎn)品則需向 NMPA 申請注冊,,經(jīng)技術(shù)審評,、臨床試驗核查(若有)等程序,取得醫(yī)療器械注冊證后才能進口,,確保進口產(chǎn)品符合國內(nèi)質(zhì)量與安全要求,。對于生物試劑出口,要提前掌握進口國的檢疫程序,。昆山抗體試劑進出口審批單
出口生物試劑要重視進口國對標簽內(nèi)容完整性的要求,。昆山抗體試劑進出口審批單
進出口生物試劑,契合目標市場標準是關(guān)鍵,。出口時,,產(chǎn)品必須滿足進口國法規(guī)及相關(guān)國際標準,。例如出口歐盟,生物試劑需符合歐盟指令與協(xié)調(diào)標準,,通過 CE 認證,,涵蓋安全性、健康影響等多方面評估,;出口美國,,則要符合美國食品藥品監(jiān)督管理局(FDA)要求并完成對應(yīng)注冊程序。進口生物試劑時,,要確保符合我國藥品,、醫(yī)療器械等相關(guān)法規(guī)。藥品類生物試劑需符合我國藥品注冊標準,,從成分純度到穩(wěn)定性都有明確規(guī)范,;醫(yī)療器械類生物試劑要完成國內(nèi)注冊或備案,產(chǎn)品研發(fā),、生產(chǎn),、質(zhì)量控制等各環(huán)節(jié)都得達標,否則無法順利通關(guān),,更不能進入市場銷售,,甚至可能面臨召回與處罰。昆山抗體試劑進出口審批單
- 上海自動化倉庫哪家靠譜 2025-06-03
- 化妝品監(jiān)管倉儲物流 2025-06-03
- 上??缇潮O(jiān)管倉庫配送 2025-06-03
- 倉庫如何收費 2025-06-03
- 南京特殊物品進口審批備案代辦 2025-06-03
- 上海自動化倉庫怎么樣 2025-06-03
- 危險品監(jiān)管倉庫公司 2025-06-03
- 保稅區(qū)倉儲費用 2025-06-03
- 上海海關(guān)監(jiān)管倉庫收費標準 2025-06-03
- 上海貨物監(jiān)管倉儲派送 2025-06-02
- 上海標準國內(nèi)配送流程 2025-06-04
- 奉賢區(qū)有哪些國內(nèi)配送詢問報價 2025-06-04
- 南京靠譜的人臉識別 2025-06-04
- 永康清潔車控制器現(xiàn)貨 2025-06-04
- 黑龍江國際出口公司 2025-06-04
- 河源澳大利亞雙清到門哪幾種 2025-06-04
- 嘉定區(qū)各地專線物流 2025-06-04
- 內(nèi)蒙古酒柜海運家具到任意地區(qū) 2025-06-04
- 湖州激光AGV小車哪家好 2025-06-04
- 新型城市配送一體化 2025-06-04