-
廣東中翔新材料簽約德米薩智能ERP加強(qiáng)企業(yè)管理水平
-
碩鋮工業(yè)簽約德米薩智能進(jìn)銷存系統(tǒng)提升企業(yè)管理水平
-
燊川實(shí)業(yè)簽約德米薩醫(yī)療器械管理軟件助力企業(yè)科學(xué)發(fā)展
-
森尼電梯簽約德米薩進(jìn)銷存系統(tǒng)優(yōu)化企業(yè)資源管控
-
喜報(bào),!熱烈祝賀德米薩通過國際CMMI3認(rèn)證
-
德米薩推出MES系統(tǒng)助力生產(chǎn)制造企業(yè)規(guī)范管理
-
德米薩醫(yī)療器械管理軟件通過上海市醫(yī)療器械行業(yè)協(xié)會(huì)評(píng)審認(rèn)證
-
德米薩ERP助力客戶成功對(duì)接中石化易派客平臺(tái)
-
選擇進(jìn)銷存軟件要考慮哪些因素
-
德米薩告訴您為什么說ERP系統(tǒng)培訓(xùn)很重要,?
昆山酶類試劑進(jìn)出口審批備案代辦
包裝和標(biāo)識(shí)在生物試劑進(jìn)出口中至關(guān)重要。包裝材料要堅(jiān)固耐用且能適應(yīng)試劑特性,,比如強(qiáng)酸強(qiáng)堿類試劑具有腐蝕性,需用耐腐蝕性包裝,,如特制的玻璃或塑料材質(zhì)容器,;對(duì)光照敏感試劑則要采用遮光包裝,像棕色玻璃或添加遮光材料的包裝容器,,以避免光照引發(fā)試劑變質(zhì),。包裝需具備良好密封性,防止泄漏,,對(duì)于一些高活性,、易揮發(fā)的生物試劑,多層密封包裝是常見選擇,。標(biāo)識(shí)方面,,必須清晰標(biāo)注產(chǎn)品名稱、成分,、規(guī)格,、生產(chǎn)企業(yè)、生產(chǎn)日期,、有效期,、儲(chǔ)存條件、使用說明等信息,,且語言要符合目標(biāo)市場要求,,通常需使用英語,在一些非英語國家,,可能還需翻譯為當(dāng)?shù)卣Z言,,方便使用者準(zhǔn)確獲取信息。對(duì)于危險(xiǎn)生物試劑,,要依據(jù)國際標(biāo)準(zhǔn)張貼危險(xiǎn)貨物標(biāo)識(shí),,如國際《關(guān)于危險(xiǎn)貨物運(yùn)輸?shù)慕ㄗh書》中的相關(guān)標(biāo)準(zhǔn),確保運(yùn)輸,、儲(chǔ)存和使用過程中的安全,,避免因包裝標(biāo)識(shí)不當(dāng)引發(fā)安全事故或通關(guān)受阻,給企業(yè)帶來巨大損失,。生物試劑進(jìn)口需關(guān)注目的國針對(duì)生物試劑的特殊關(guān)稅政策,。昆山酶類試劑進(jìn)出口審批備案代辦

進(jìn)出口生物試劑均需通過嚴(yán)格檢驗(yàn)檢疫。出口時(shí),,企業(yè)要主動(dòng)向海關(guān)與檢驗(yàn)檢疫部門申報(bào),,提供詳細(xì)產(chǎn)品信息,、生產(chǎn)批次,、質(zhì)量檢測報(bào)告等資料。檢驗(yàn)檢疫部門會(huì)根據(jù)試劑特性與進(jìn)口國要求,進(jìn)行質(zhì)量抽檢,,檢測純度,、活性、微生物限度等指標(biāo),,對(duì)于一些傳染病診斷試劑,,對(duì)其微生物限度和特異性要求極高。對(duì)可能攜帶病原體,、有害生物因子的試劑進(jìn)行生物安全檢測,,防止有害生物跨境傳播。進(jìn)口生物試劑時(shí),,同樣要接受我國檢驗(yàn)檢疫部門查驗(yàn),,企業(yè)需配合做好貨物查驗(yàn)、抽樣檢測等工作,,對(duì)于冷鏈生物試劑,,還要滿足冷鏈貨物檢驗(yàn)檢疫要求,如落實(shí)核酸檢測,、消毒等防控措施,,確保產(chǎn)品符合國內(nèi)外檢驗(yàn)檢疫標(biāo)準(zhǔn),保障公共衛(wèi)生安全與市場秩序,,為國內(nèi)科研,、醫(yī)療等領(lǐng)域提供安全可靠的生物試劑。寧波酶類試劑進(jìn)出口審批流程生物試劑進(jìn)口申報(bào)時(shí),,需明確試劑的生物活性等級(jí),。

生物試劑種類繁多,常見有化學(xué)試劑類,,如各種緩沖液,、培養(yǎng)基成分等,其進(jìn)出口相對(duì)常規(guī),,但也要符合化學(xué)試劑相關(guān)法規(guī),,對(duì)純度、雜質(zhì)限量有要求,。生物活性試劑,,像抗體、重組蛋白等,,具有生物活性,,保存和運(yùn)輸條件苛刻,進(jìn)出口時(shí)對(duì)冷鏈要求嚴(yán)格,,且需提供詳細(xì)產(chǎn)品活性數(shù)據(jù)與質(zhì)量證明,。診斷試劑作為特殊一類,,用于疾病診斷,各國對(duì)其監(jiān)管更為嚴(yán)格,,進(jìn)口時(shí)要通過復(fù)雜注冊(cè)審批程序,,確保產(chǎn)品準(zhǔn)確性、特異性和穩(wěn)定性,。此外,,還有細(xì)胞類生物試劑,如細(xì)胞株,、干細(xì)胞等,,不運(yùn)輸需特殊條件維持細(xì)胞活性,進(jìn)出口還涉及生物安全評(píng)估,,防止外來物種入侵和生物安全風(fēng)險(xiǎn),。不同類型生物試劑進(jìn)出口特點(diǎn)各異,企業(yè)需針對(duì)性應(yīng)對(duì),。
進(jìn)出口生物試劑,,契合目標(biāo)市場質(zhì)量與安全標(biāo)準(zhǔn)是關(guān)鍵。出口時(shí),,產(chǎn)品必須滿足進(jìn)口國法規(guī)及相關(guān)國際標(biāo)準(zhǔn),。比如出口歐盟,生物試劑需符合歐盟指令與協(xié)調(diào)標(biāo)準(zhǔn),,通過 CE 認(rèn)證,;出口美國,則要符合美國食品藥品監(jiān)督管理局(FDA)要求并完成對(duì)應(yīng)注冊(cè)程序,。進(jìn)口生物試劑時(shí),,要確保符合我國藥品、醫(yī)療器械等相關(guān)法規(guī),。藥品類生物試劑需符合我國藥品注冊(cè)標(biāo)準(zhǔn),,從成分到穩(wěn)定性都有嚴(yán)格規(guī)范;醫(yī)療器械類生物試劑要完成國內(nèi)注冊(cè)或備案,,產(chǎn)品研發(fā),、生產(chǎn)、質(zhì)量控制等各環(huán)節(jié)都得達(dá)標(biāo),,不然無法順利通關(guān),,更不能進(jìn)入市場銷售,甚至可能面臨召回與處罰,。出口生物試劑要注意進(jìn)口國對(duì)產(chǎn)品售后服務(wù)的規(guī)定,。
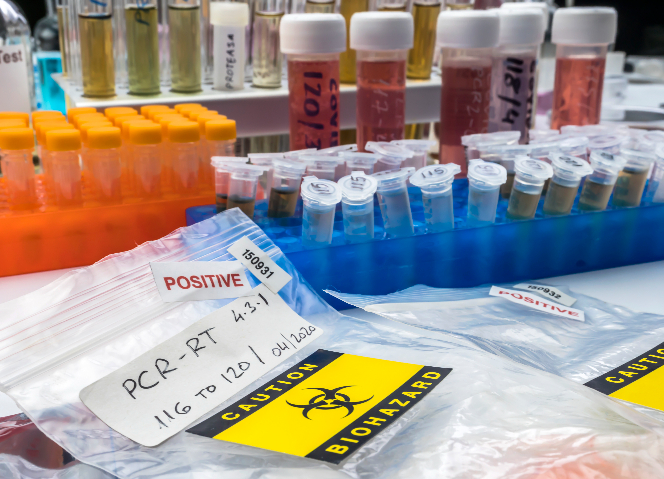
在生物試劑進(jìn)出口領(lǐng)域,法規(guī)政策起著關(guān)鍵的規(guī)范作用,。不同國家和地區(qū)對(duì)生物試劑的進(jìn)出口有著嚴(yán)格規(guī)定,。例如,,我國依據(jù)《中華人民共和國藥品管理法》《醫(yī)療器械監(jiān)督管理?xiàng)l例》等法規(guī),對(duì)作為藥品或醫(yī)療器械管理的生物試劑,,要求企業(yè)具備相應(yīng)資質(zhì),,如藥品經(jīng)營許可證,、醫(yī)療器械經(jīng)營備案憑證等,。對(duì)于一些特殊生物試劑,可能還涉及《生物制品批簽發(fā)管理辦法》,,需取得批簽發(fā)證明方可進(jìn)口,。美國食品藥品監(jiān)督管理局(FDA)對(duì)進(jìn)口生物試劑也有詳細(xì)準(zhǔn)則,從產(chǎn)品注冊(cè),、標(biāo)簽要求到生產(chǎn)質(zhì)量管理規(guī)范(GMP)符合性審查等,,確保產(chǎn)品安全有效。企業(yè)在開展進(jìn)出口業(yè)務(wù)前,,務(wù)必深入研究目標(biāo)市場法規(guī),,完成各類許可申請(qǐng)與注冊(cè)流程,避免因違規(guī)遭受處罰,,影響業(yè)務(wù)開展,。出口生物試劑要留意進(jìn)口國對(duì)產(chǎn)品說明書語言的要求。上海港免疫診斷試劑進(jìn)出口
生物試劑進(jìn)口申報(bào)需準(zhǔn)確提供產(chǎn)品的生產(chǎn)工藝信息,。昆山酶類試劑進(jìn)出口審批備案代辦
若生物試劑含有毒有害物質(zhì),,進(jìn)口前需通過環(huán)保部門的審批。企業(yè)要向當(dāng)?shù)厣鷳B(tài)環(huán)境部門提交進(jìn)口申請(qǐng),,說明生物試劑所含毒有害物質(zhì)的種類,、含量、用途,、處理方式等信息,。生態(tài)環(huán)境部門會(huì)依據(jù)相關(guān)環(huán)保法規(guī),評(píng)估試劑進(jìn)口對(duì)環(huán)境的潛在影響,,如是否符合污染物排放標(biāo)準(zhǔn),、是否具備妥善的廢棄物處理方案等。只有在獲得環(huán)保部門許可后,,企業(yè)才能進(jìn)行后續(xù)進(jìn)口操作,,確保生物試劑進(jìn)口不會(huì)對(duì)國內(nèi)生態(tài)環(huán)境造成危害。涉及人類遺傳資源的生物試劑進(jìn)口,,受《中華人民共和國人類遺傳資源管理?xiàng)l例》約束,。進(jìn)口單位必須向有關(guān)部門科學(xué)技術(shù)行政部門申請(qǐng)人類遺傳資源許可。申請(qǐng)過程中,,需詳細(xì)說明試劑來源,、涉及的人類遺傳資源種類與數(shù)量,、使用目的、合作方信息等,。有關(guān)部門科學(xué)技術(shù)行政部門會(huì)對(duì)申請(qǐng)進(jìn)行嚴(yán)格審查,,考量是否符合保護(hù)我國人類遺傳資源安全、促進(jìn)合理利用等要求,,獲批后企業(yè)方可進(jìn)口,,避免我國人類遺傳資源非法外流及不當(dāng)使用。昆山酶類試劑進(jìn)出口審批備案代辦
- 上海港免疫診斷試劑進(jìn)出口前置審批備案 2025-05-18
- 南京核酸試劑進(jìn)出口監(jiān)管法規(guī) 2025-05-17
- 上海港化妝品監(jiān)管倉儲(chǔ)怎么樣 2025-05-17
- 上海港核酸試劑進(jìn)出口監(jiān)管法規(guī) 2025-05-17
- 昆山核酸試劑進(jìn)出口監(jiān)管法規(guī) 2025-05-17
- 無錫特殊物品進(jìn)口貿(mào)易 2025-05-17
- 上海港化妝品監(jiān)管倉庫哪家專業(yè) 2025-05-17
- 南京生物試劑進(jìn)出口清關(guān)手續(xù) 2025-05-17
- 杭州核酸試劑進(jìn)出口前置審批代辦 2025-05-17
- 上海酶類試劑進(jìn)出口審批備案代辦 2025-05-17
- 山東靈活性國內(nèi)專線運(yùn)輸 2025-05-18
- 楊浦區(qū)倉庫倉儲(chǔ)托管 2025-05-18
- 嘉定區(qū)企業(yè)郵件mailroom桌到桌服務(wù) 2025-05-18
- 山東哪里有化工品運(yùn)輸聯(lián)系方式 2025-05-18
- 二手無菌生產(chǎn)線進(jìn)口清關(guān)公司 2025-05-18
- 能數(shù)據(jù)分析的一件代發(fā)第三方倉儲(chǔ) 2025-05-18
- 合肥貨物大件運(yùn)輸公司 2025-05-18
- 宜興靠譜的道路貨物運(yùn)輸介紹 2025-05-18
- 嘉定區(qū)現(xiàn)代化國內(nèi)配送服務(wù)電話 2025-05-18
- 金山區(qū)裝卸搬運(yùn)設(shè)計(jì)方案 2025-05-18