天津有什么藥物安全性評價(jià)
藥物安全性評價(jià),***應(yīng)對******聯(lián)防聯(lián)控機(jī)制科研攻關(guān)組印發(fā)《關(guān)于規(guī)范醫(yī)療機(jī)構(gòu)開展藥物***臨床研究的通知》[36],專門針對研究者發(fā)起的臨床試驗(yàn)提出了要求,。這個(gè)《通知》的發(fā)布使得由研究者發(fā)起的臨床試驗(yàn)的門檻變高,。新的申請行政審核流程和條件,以及臨床實(shí)施的要求和結(jié)果都不能低于“經(jīng)藥品監(jiān)管部門批準(zhǔn)的****適應(yīng)癥的藥物臨床試驗(yàn)”的要求,即必須滿足一些基本要求,。如果一種藥物在體外試驗(yàn)中在細(xì)胞層面產(chǎn)生抑制的活性,或在***的動物試驗(yàn)中證明***有效,同時(shí)已經(jīng)批準(zhǔn)上市的藥物就可以有充足理由上臨床試驗(yàn),。用上市藥物作對照主要是它們都有確切的藥物安全性評價(jià),,有大量的臨床數(shù)據(jù)可以參考,包括藥物服用劑量,、時(shí)長,、副作用都有一定依據(jù)。體外試驗(yàn)技術(shù)在藥物安全性評價(jià)中的應(yīng)用是什么,?天津有什么藥物安全性評價(jià)
藥物安全性評價(jià)的地位和價(jià)值體現(xiàn)在以下三個(gè)方面:1.在支持新藥臨床研究時(shí),,并不需要在進(jìn)入臨床研究(I期)前完成所有相關(guān)研究,而是分階段來分別支持I,、Ⅱ,、Ⅲ期臨床研究,為如何進(jìn)行臨床研究提供重要參考,,具體體現(xiàn)在臨床研究方案中的給藥劑量(尤其是I期臨床研究的起始劑量),、安全性檢查/監(jiān)測指標(biāo)和檢測時(shí)機(jī)的確定,危險(xiǎn)性的預(yù)測和救治措施的實(shí)施等方面,;2.在臨床研究過程中,,甚至上市后,出現(xiàn)非預(yù)期重要的安全性問題且難以判斷/預(yù)測其風(fēng)險(xiǎn)性等情況下,,需再次進(jìn)行有關(guān)的非臨床安全性研究(包括機(jī)制研究),,通過臨床研究信息為非臨床安全性研究提供方向和目標(biāo),以減少臨床研究和(或)臨床應(yīng)用的風(fēng)險(xiǎn),;3.在臨床研究完成后,,受試藥的臨床有效性和安全性已有一個(gè)基本結(jié)論,此時(shí)藥物安全性評價(jià)的某些結(jié)果(如致*性等)可能是比較終確定受試藥是否批準(zhǔn)上市(利弊權(quán)衡)的重要依據(jù)之一,。河北推薦的藥物安全性評價(jià)多少錢英瀚斯藥物安全性評價(jià),,為新藥候選化合物的確定及開發(fā)提供依據(jù)。
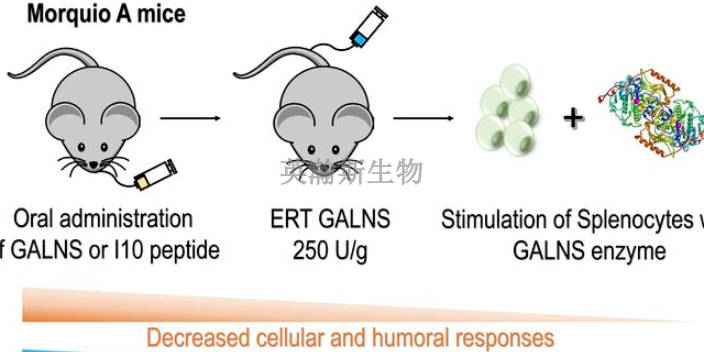
藥物安全性評價(jià),。目前,,我國已經(jīng)超過40個(gè)創(chuàng)新型抗體藥物申請臨床試驗(yàn),且多個(gè)品種同期在歐美申報(bào)進(jìn)入臨床,,國內(nèi)單抗藥物未來申報(bào)趨勢正由“生物類似藥”向“全球新”轉(zhuǎn)變,。相比于工業(yè)界日新月異的技術(shù)發(fā)展,基于既往國情制定的指導(dǎo)原則與技術(shù)要求已經(jīng)顯現(xiàn)滯后,。過去幾年創(chuàng)新型抗體藥物的“審評周期長,、發(fā)補(bǔ)次數(shù)多”,因此,對于創(chuàng)新藥的審評能力與技術(shù)要求一直存在擔(dān)憂,,如:審評與審批是否會成為制約新藥開發(fā)的限速步驟,、國內(nèi)外IND階段的藥學(xué)研究內(nèi)容與要求尚不統(tǒng)一等,。隨著我國藥品審評審批**的深入,未來藥品注冊法規(guī)與相關(guān)技術(shù)要求將會持續(xù)更新,,結(jié)合國情并與國際接軌,;對于創(chuàng)新型抗體的藥學(xué)評價(jià),也將充分考慮其作為“創(chuàng)新藥”的研發(fā)規(guī)律與技術(shù)特點(diǎn),,在保證臨床安全性的前提下分階段,、適時(shí)進(jìn)行要求,重點(diǎn)關(guān)注影響臨床藥物安全性評價(jià)的重大藥學(xué)問題,;同時(shí),,未來出臺指導(dǎo)原則、申報(bào)資料技術(shù)要求等文件將進(jìn)一步實(shí)現(xiàn)對創(chuàng)新藥研發(fā)“事前指導(dǎo)”,。相信在工業(yè)界創(chuàng)新驅(qū)動與監(jiān)管界風(fēng)險(xiǎn)管控的互動推進(jìn)下,,未來將有更多的創(chuàng)新型抗體藥物會及早進(jìn)入臨床試驗(yàn),造福病患,。
龐大的數(shù)據(jù)資源使得學(xué)術(shù)界,、商界和政界更加關(guān)注新藥上市后評價(jià)和風(fēng)險(xiǎn)得益的考慮。也就是說近年來大量創(chuàng)新藥物的上市,,伴隨著可能出現(xiàn)的安全性問題,臨床IV期(藥品上市后的藥物安全性評價(jià)**研究)得到了藥企和醫(yī)院等機(jī)構(gòu)的重視,,從臨床療效的研究逐步轉(zhuǎn)變到臨床安全有效研究的角度,,從大數(shù)據(jù)分析中來收集真實(shí)世界證據(jù),認(rèn)識藥物上市后的真實(shí)世界,。特別是快速通道批準(zhǔn)的新藥,,有的由于病例數(shù)極少或技術(shù)原因只在少數(shù)病例上完成II期臨床,就被批準(zhǔn)上市,。不論進(jìn)口引進(jìn)或臨床使用,,醫(yī)生和患者更需考慮進(jìn)入IV期臨床研究的新藥的療效安全和經(jīng)費(fèi)的承受能力等風(fēng)險(xiǎn)。英瀚斯生物以客戶需求為導(dǎo)向的原則靈活進(jìn)行研究設(shè)計(jì),,提供***的藥物安全性評價(jià),。
疫苗新藥臨床前研究中的藥物安全性評價(jià)內(nèi)容:(3)一般藥理試驗(yàn)常規(guī)的一般藥理試驗(yàn)并不適用疫苗,建立在重復(fù)給藥試驗(yàn)中進(jìn)行一般藥理試驗(yàn)相關(guān)指標(biāo)的檢測,。(4)生殖毒性試驗(yàn)FDA認(rèn)為凡是用于青春期少年,、成人和可能懷孕的婦女的疫苗均應(yīng)進(jìn)行生殖毒性試驗(yàn),用于懷孕婦女的疫苗應(yīng)在臨床研究開始之前完成生殖毒性試驗(yàn),。用于有懷孕可能的疫苗可以在申報(bào)生產(chǎn)時(shí)提供生殖毒性試驗(yàn)資料,,但是受試者在臨床研究期間應(yīng)采取避孕措施。(5)過敏試驗(yàn)疫苗臨床上比較常見的有過敏反應(yīng),,然而如何通過臨床前動物試驗(yàn)來預(yù)測包括疫苗在內(nèi)的生物制品的過敏反應(yīng),,是毒理學(xué)家和藥品審評部門面對的一大難題。目前國內(nèi)通常使用豚鼠主動全身過敏反應(yīng)(ASA)和被動皮膚過敏試驗(yàn)(PCA)來預(yù)測化合物或生物制品在臨床上引起過敏反應(yīng)的可能性。另外,,小鼠局部淋巴結(jié)試驗(yàn)(LLNA)是近年來國外研究較為關(guān)注的一種有可能用來預(yù)測人體過敏反應(yīng)的試驗(yàn)方法,。藥物安全性評價(jià)是新藥研發(fā)的必需組成部分。黑龍江比較好的藥物安全性評價(jià)價(jià)格
英瀚斯生物具備藥物安全性評價(jià)配套動物實(shí)驗(yàn)室,、細(xì)胞實(shí)驗(yàn)室,。天津有什么藥物安全性評價(jià)
疫苗新藥臨床前研究中藥物安全性評價(jià)的難點(diǎn)在于疫苗本身并不直接發(fā)揮預(yù)防或***作用,而是通過誘導(dǎo)免疫系統(tǒng)產(chǎn)生抗體或活化T細(xì)胞發(fā)揮作用,。在疫苗研發(fā)中需要考慮疫苗可能會產(chǎn)生的安全問題,。(1)疫苗成分本身作為毒性物質(zhì)對機(jī)體的直接損傷。(2)疫苗誘導(dǎo)免疫系統(tǒng)引起的與免疫相關(guān)的毒性,。(3)污染物和殘余雜質(zhì)引起的毒性,。疫苗制備的過程中的各個(gè)環(huán)節(jié)具有可能帶入污染物或?qū)е職堄嚯s質(zhì)的存在,控制此類毒性也是質(zhì)量控制研究的主要目的,。(4)若疫苗載體在體內(nèi)變異,,將威脅患者的生命。(5)其它未知的毒性,。天津有什么藥物安全性評價(jià)
南京英瀚斯生物科技有限公司是一家有著雄厚實(shí)力背景,、信譽(yù)可靠、勵(lì)精圖治,、展望未來,、有夢想有目標(biāo),有組織有體系的公司,,堅(jiān)持于帶領(lǐng)員工在未來的道路上大放光明,,攜手共畫藍(lán)圖,在江蘇省等地區(qū)的醫(yī)藥健康行業(yè)中積累了大批忠誠的客戶粉絲源,,也收獲了良好的用戶口碑,,為公司的發(fā)展奠定的良好的行業(yè)基礎(chǔ),也希望未來公司能成為*****,,努力為行業(yè)領(lǐng)域的發(fā)展奉獻(xiàn)出自己的一份力量,,我們相信精益求精的工作態(tài)度和不斷的完善創(chuàng)新理念以及自強(qiáng)不息,斗志昂揚(yáng)的的企業(yè)精神將**南京英瀚斯生物科技供應(yīng)和您一起攜手步入輝煌,,共創(chuàng)佳績,,一直以來,公司貫徹執(zhí)行科學(xué)管理,、創(chuàng)新發(fā)展,、誠實(shí)守信的方針,員工精誠努力,,協(xié)同奮取,,以品質(zhì),、服務(wù)來贏得市場,我們一直在路上,!
- 遼寧子宮內(nèi)膜異位癥模型是哪家 2025-06-01
- 山東大鼠腦缺血再灌注模型哪家好 2025-06-01
- 貴州動物腦缺血再灌注模型服務(wù) 2025-06-01
- 內(nèi)蒙古推薦的腦缺血再灌注模型價(jià)格 2025-06-01
- 山東比較好的肺纖維化模型如何構(gòu)建 2025-06-01
- 內(nèi)蒙古MCO腦缺血再灌注模型公司 2025-06-01
- 甘肅MCO腦缺血再灌注模型公司 2025-06-01
- 江西推薦的臨床前動物實(shí)驗(yàn)外包 2025-05-31
- 貴州有什么臨床前動物實(shí)驗(yàn)機(jī)構(gòu) 2025-05-31
- 湖北高質(zhì)量臨床前動物實(shí)驗(yàn)價(jià)格 2025-05-31
- 云南雙錐混合機(jī)結(jié)構(gòu)圖 2025-06-01
- 江蘇抗原檢測自測植絨前鼻拭子出口企業(yè) 2025-06-01
- 重慶蛋白質(zhì)組學(xué)自動化設(shè)備源頭廠家 2025-06-01
- 三層真空包裝的培養(yǎng)基大概價(jià)格 2025-06-01
- 鹽田區(qū)便宜的生物試劑專賣店 2025-06-01
- 上海專業(yè)ELISA試劑盒廠家價(jià)格 2025-06-01
- 深圳內(nèi)窺鏡模組廠家 2025-06-01
- 安徽二類械字號貼劑供應(yīng) 2025-06-01
- 無錫國內(nèi)人工智能輔助診斷設(shè)備銷售方法 2025-06-01
- 國產(chǎn)小型集中供水系統(tǒng)品牌 2025-06-01