內(nèi)蒙古臨床前動物實驗檢測
關(guān)于臨床前動物實驗的故事,。過去十余年,,國內(nèi)某團隊也一直致力于理想的“超級疫苗”研究,基于已有的研究基礎(chǔ),,在此次**科研攻關(guān)中,,他們設(shè)計出新的疫苗抗原分子,,建立哺乳動物細胞表達系并純化了抗原蛋白,,用微劑量免疫動物后(小動物5微克,大動物10微克),,產(chǎn)生了高達百萬倍試紙測試效價的抗體,。免疫抗體經(jīng)在國家批準(zhǔn)的P3實驗室測定,中和病毒的效價都達到了要求,,有的超過了檢測單位設(shè)定的比較高限,。目前,他們已開始進行臨床前動物實驗,,在免疫猴子,、小鼠和雪貂準(zhǔn)備攻毒中和實驗。英瀚斯專業(yè)做中成藥臨床前動物實驗外包,。內(nèi)蒙古臨床前動物實驗檢測
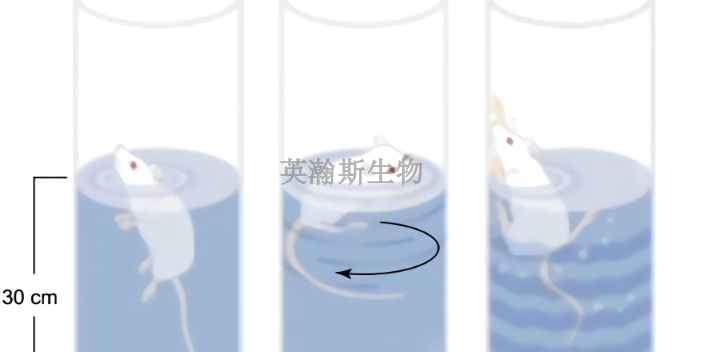
臨床前動物實驗的目的主要是通過相關(guān)動物模型來考察產(chǎn)品的安全性和有效性,,以及臨床相關(guān)參數(shù)的確定,預(yù)測其在人群中使用時可能出現(xiàn)的不良事件,,降低臨床試驗受試者和臨床使用者承擔(dān)的風(fēng)險,,并為臨床試驗方案的制定提供依據(jù)。動物實驗研究作為初步驗證醫(yī)療器械安全性及有效性的重要手段,,動物實驗的質(zhì)量管理對保證動物實驗研究數(shù)據(jù)的真實,、可靠、準(zhǔn)確,、科學(xué)和完整至關(guān)重要,。因此,研究機構(gòu)需要加強對臨床前動物實驗的質(zhì)量管理,,監(jiān)管部門也將不斷加強對該領(lǐng)域的規(guī)范要求并加強科學(xué)監(jiān)管,。北京專注臨床前動物實驗?zāi)募液门R床前動物實驗的具體內(nèi)容和要求?
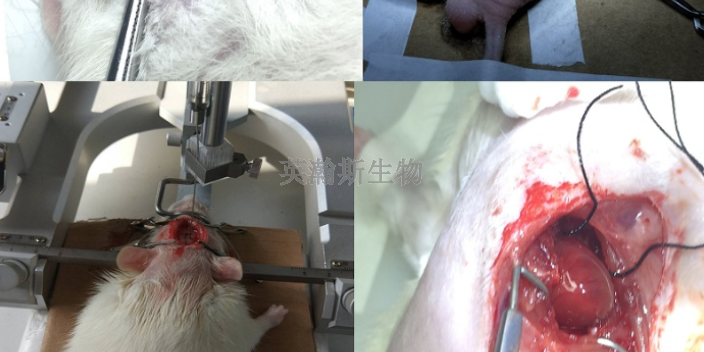
臨床前動物實驗推薦南京英瀚斯生物,。,,常規(guī)流程上,疫苗研發(fā)從細胞水平的體外實驗,、到臨床前動物實驗,再到人體臨床試驗,,是一個漫長的過程,。證明疫苗安全有效的過程非常緩慢,從少數(shù)人的臨床試驗,,只是觀察免疫反應(yīng)副作用等,,到需要成千上萬人來測試疫苗效果的大型試驗,這一過程至少需要1年時間,。與動物疫苗在實驗室獲得結(jié)果不同,,評價人的疫苗有效性依賴于長時間的統(tǒng)計數(shù)據(jù),,我們需要在一定時間內(nèi)監(jiān)測注射疫苗者與注射安慰劑者的***率的差別,而在這個過程中,,通常還會有各種影響因素干擾結(jié)果,,這也就是疫苗進程**拉長的原因。
臨床前動物實驗就在英瀚斯一站式實驗中心,。凡是沒有經(jīng)過院方倫理委員會的審核,,一般是不合乎規(guī)范的。合乎規(guī)范也頗值得琢磨,。有的是法律,,有的是行政管理,有的是行業(yè)認可的標(biāo)準(zhǔn),,比如針對臨床***的一些共識等?,F(xiàn)在的問題是,沒有一個統(tǒng)一的規(guī)范,,也就很難定義違不違規(guī)了,。對此,首先是要完善干細胞***的基礎(chǔ)研究,,踏踏實實完成從臨床前動物實驗到臨床試驗的過程,,不可急功近利。同時,,技術(shù)需要創(chuàng)新和嘗試,,由此帶來的風(fēng)險要靠嚴(yán)格的規(guī)范去控制,但不能因為害怕承擔(dān)可能的風(fēng)險,,使規(guī)則的制定都停滯不前,。生物藥臨床前動物實驗研究;
炎*轉(zhuǎn)化是**高發(fā)的一個重要因素,,在國家自然科學(xué)基金重大研究計劃“非可控性炎癥惡性轉(zhuǎn)化的調(diào)控網(wǎng)絡(luò)及其分子機制”資助下,,研究人員不僅在炎*轉(zhuǎn)化的方法學(xué)和技術(shù)上取得突破,還建立起專業(yè)的數(shù)據(jù)庫,,為炎*轉(zhuǎn)化研究搭建強有力的平臺,。首先,該重大研究計劃為理解復(fù)雜的炎*轉(zhuǎn)化過程,,著力建立臨床前動物實驗?zāi)P妥鳛榛A(chǔ),。“如果沒有理想的動物模型,,研究將非常困難,。”王紅陽坦言。在指導(dǎo)**組的組織下,,多個團隊開展攻關(guān),,新建動物模型20種,改良現(xiàn)有動物模型22種,,總共提供了42種新的動物模型,。英瀚斯是專業(yè)的中成藥臨床前動物實驗外包公司。陜西專注臨床前動物實驗機構(gòu)
醫(yī)療器械臨床試驗前動物試驗研究要點有哪些,?內(nèi)蒙古臨床前動物實驗檢測
臨床前動物實驗,,TGN1412是TeGenero的較早產(chǎn)品,從生產(chǎn)到進入臨床試驗才2年多時間,從MHRA批準(zhǔn)TGN1412進入臨床試驗到試驗開始總共才45天。ESG指出,雖然臨床前動物實驗沒有發(fā)現(xiàn)嚴(yán)重不良反應(yīng),但不能因此估測出一個TGN1412用于人類的安全劑量,藥物的安全性未得到充分論證,。實施臨床試驗的研究者沒有受到良好培訓(xùn),志愿者對可能發(fā)生的危險也了解不足,。媒體和公眾都指責(zé)MHRA為了吸引醫(yī)藥公司到英國進行臨床研究而放寬了藥物臨床研究的審批。從而使一家*有15名雇員,、風(fēng)險資本驅(qū)動的德國小公司不在本國進行臨床試驗,卻轉(zhuǎn)而選擇英國,。內(nèi)蒙古臨床前動物實驗檢測
- 山西小鼠eae模型如何構(gòu)建 2025-06-12
- 重慶子宮內(nèi)膜異位癥模型有哪些 2025-06-11
- 吉林小鼠子宮內(nèi)膜異位癥模型造模方法 2025-06-11
- 浙江哪里有子宮內(nèi)膜異位癥模型實驗外包 2025-06-11
- 福建專業(yè)的子宮內(nèi)膜異位癥模型怎么造模 2025-06-11
- 山西靠譜的子宮內(nèi)膜異位癥模型造模方法 2025-06-11
- 山西小鼠子宮內(nèi)膜異位癥模型哪家口碑好 2025-06-10
- 廣東靠譜的子宮內(nèi)膜異位癥模型如何構(gòu)建 2025-06-10
- 湖北大鼠子宮內(nèi)膜異位癥模型 2025-06-10
- 青海專業(yè)的子宮內(nèi)膜異位癥模型有哪些 2025-06-10
- 常州70921-202高鹽核酸酶聯(lián)系方式 2025-06-12
- 推薦健身器材批發(fā)歡迎選購 2025-06-12
- 上海市隨訪一體機廠家 2025-06-12
- 咸陽怎么選活性益生菌產(chǎn)品 2025-06-12
- 蘇州一次性射頻消融有源器械設(shè)計開發(fā)服務(wù)報價 2025-06-12
- 杭州一次性醫(yī)療監(jiān)測設(shè)備生產(chǎn)制造 2025-06-12
- 襄陽推拿手法仿真測試系統(tǒng)廠家 2025-06-12
- 天津比較好的分子耗材 2025-06-12
- 福建抑菌洗劑推薦 2025-06-12
- 南京進口的全自動核酸提取儀 2025-06-12