值得信賴藥物安全性評(píng)價(jià)機(jī)構(gòu)
關(guān)于***的比較好單一療法仍未明確。現(xiàn)有指南推薦在沒有共病指征的情況下,,可使用**藥物中的任何主要藥物,,如噻嗪類或噻嗪類***劑,、血管緊張素轉(zhuǎn)換酶抑制劑,、血管緊張素受體阻滯劑,、二氫吡啶類鈣通道阻滯劑和非二氫吡啶類鈣通道阻斷劑來進(jìn)行***,,但仍缺乏隨機(jī)試驗(yàn)的驗(yàn)證與完善,。某研究組開發(fā)了一個(gè)綜合框架,,以便更客觀地進(jìn)行藥物安全性評(píng)價(jià),。利用這個(gè)框架,研究組在一個(gè)新用戶隊(duì)列設(shè)計(jì)中進(jìn)行了這項(xiàng)系統(tǒng)的大規(guī)模研究,,評(píng)估了**抗***藥物***后三種主要結(jié)局的風(fēng)險(xiǎn),,即急性心肌梗死、心力衰竭住院和中風(fēng),。藥物安全性評(píng)價(jià). 新藥從研制過渡到臨床,必須進(jìn)行臨床前的藥物安全性毒理學(xué)評(píng)價(jià),。值得信賴藥物安全性評(píng)價(jià)機(jī)構(gòu)
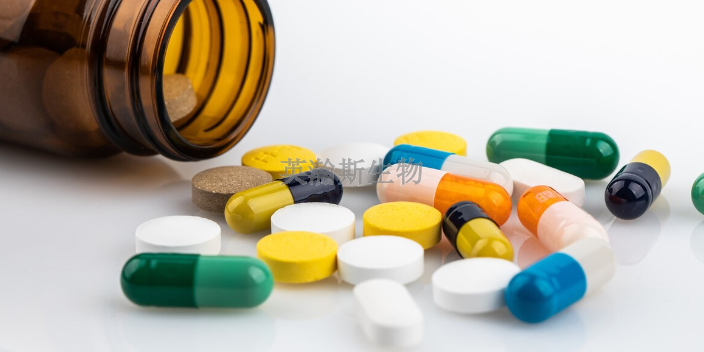
由于創(chuàng)新型抗體藥物的靶點(diǎn)、結(jié)構(gòu)特征與作用機(jī)制,,有別于已上市抗體或傳統(tǒng)生物類似藥,工業(yè)界與監(jiān)管界對(duì)此類品種的科學(xué)認(rèn)知積累有限,,藥物安全性評(píng)價(jià)需要普遍的臨床前研究和臨床試驗(yàn)研究。因此對(duì)于創(chuàng)新型抗體藥物的藥學(xué)研究,,工業(yè)界通常結(jié)合臨床試驗(yàn)進(jìn)展“分階段”開展(clinicalphase-appropriate),,產(chǎn)品上市前普遍存在多次生產(chǎn)工藝變更[,]??梢哉f,,創(chuàng)新型抗體藥物的研發(fā)規(guī)律具備“創(chuàng)試性”(臨床研究存在較大失敗風(fēng)險(xiǎn))、“階段性”(藥學(xué)研究分階段展開)和“漸進(jìn)性”(臨床期間普遍存在工藝變更)等明顯特征。上述特點(diǎn)也決定了此類品種藥學(xué)評(píng)價(jià)的一般考慮與特殊要求區(qū)別于生物類似藥,。近年,,由于工業(yè)界與監(jiān)管方對(duì)于創(chuàng)新風(fēng)險(xiǎn)評(píng)價(jià)經(jīng)常存在分歧,加之缺乏有效的溝通交流機(jī)制,,造成目前此類品種“審評(píng)周期長(zhǎng),,發(fā)補(bǔ)率高”等情況。本文回顧了近年來創(chuàng)新型抗體藥物研發(fā)趨勢(shì)與申報(bào)現(xiàn)狀,,并結(jié)合代替品種的技術(shù)特點(diǎn),,就創(chuàng)新型抗體藥學(xué)評(píng)價(jià)一般考慮與特殊要求展開討論,以期促進(jìn)藥物研發(fā)順利轉(zhuǎn)入臨床試驗(yàn),。值得信賴藥物安全性評(píng)價(jià)機(jī)構(gòu)藥物安全性評(píng)價(jià)技術(shù)和方法是目前各國學(xué)者研究的熱點(diǎn),。
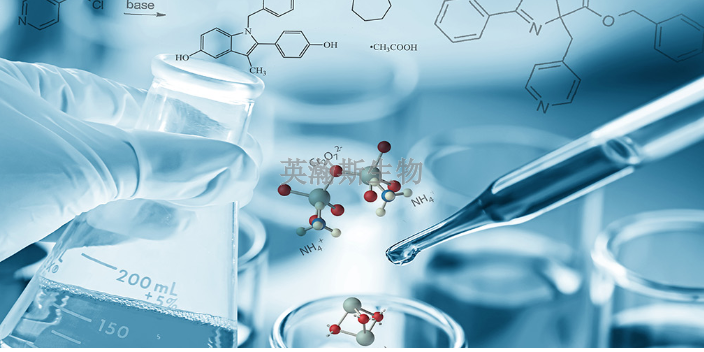
在推進(jìn)藥物安全性評(píng)價(jià)方面,推出了人用藥配藥新監(jiān)管措施和保障藥品供應(yīng)鏈的規(guī)定,,為繼續(xù)加速藥品審評(píng)的速度和效率,,也推出了功能強(qiáng)大的新工具以加速“突破藥物”的研發(fā)和審評(píng),加快藥品或生物制品的研發(fā),,必須有突破性認(rèn)證,、優(yōu)先審評(píng)和/或快速通道狀態(tài)結(jié)合的加速審評(píng)系統(tǒng)的支持。在醫(yī)療器械方面,,基于風(fēng)險(xiǎn)的機(jī)制,,為確保患者安全,,建立***器械識(shí)別碼用以提高醫(yī)療器械的可追蹤性和安全性,,必須保證供應(yīng)商能夠用安全、準(zhǔn)確,、可靠的測(cè)試結(jié)果,,繼續(xù)推動(dòng)診斷測(cè)試、指導(dǎo)***決策服務(wù),。
從事藥物安全性評(píng)價(jià)實(shí)驗(yàn)的各崗位工作人員數(shù)量應(yīng)當(dāng)與實(shí)際工作量相匹配,。工作人員的專業(yè)教育背景應(yīng)當(dāng)與其崗位職能相適應(yīng),如藥理毒理學(xué),、醫(yī)學(xué),、藥學(xué)、病理學(xué)和獸醫(yī)學(xué)等相關(guān)專業(yè)教育背景,。必要時(shí)還應(yīng)當(dāng)配備實(shí)驗(yàn)動(dòng)物學(xué),、生物學(xué)、統(tǒng)計(jì)學(xué),、信息工程等其他專業(yè)的人員或接受過同等類型專業(yè)培訓(xùn)的人員,。各崗位工作人員均應(yīng)當(dāng)具備承擔(dān)工作所需的專業(yè)知識(shí),、工作經(jīng)驗(yàn)和技術(shù)能力,掌握與其工作相關(guān)的各項(xiàng)制度與操作規(guī)程,,并能夠嚴(yán)格執(zhí)行,。實(shí)驗(yàn)室應(yīng)當(dāng)對(duì)工作人員進(jìn)行上崗前專業(yè)知識(shí)和技能的培訓(xùn)及考核,以確保其任職資格滿足要求,。各崗位工作人員均需獲得相應(yīng)的崗位資質(zhì)授權(quán)后方可上崗,。對(duì)于有特殊要求的崗位,還應(yīng)當(dāng)根據(jù)國家有關(guān)規(guī)定獲得相應(yīng)的特定資質(zhì)授權(quán),。英瀚斯成熟團(tuán)隊(duì)擁有豐富新藥項(xiàng)目臨床藥物安全性評(píng)價(jià)的經(jīng)驗(yàn)。
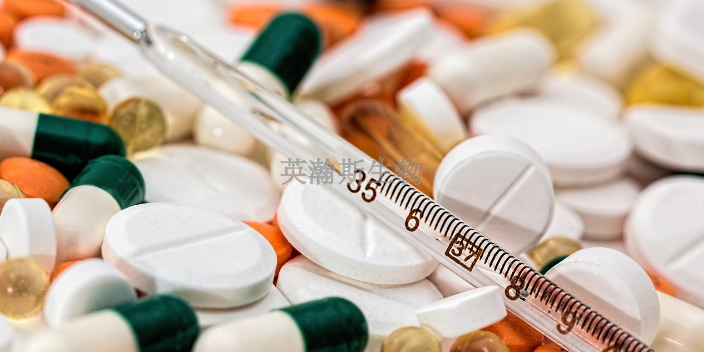
藥物安全性評(píng)價(jià),,干細(xì)胞藥物開發(fā)者無知者無畏急功近利,,試圖將不成熟的實(shí)驗(yàn)室技術(shù)推向臨床,碰得鼻青臉腫后一味地責(zé)怪“審評(píng)官不懂細(xì)胞“,、“政策不到位”和“**不作為”,,從不思反省自身問題,死到臨頭來也沒弄明白“藥”到底是什么,。而新藥審評(píng)機(jī)構(gòu)緊緊守住《藥品注冊(cè)管理法》的審批制的責(zé)任底線,,冷眼對(duì)待“細(xì)胞學(xué)家”的各種忽悠充耳不聞,生硬地拿化學(xué)藥物,、生物制品來套,,與仿制藥時(shí)代形成的審評(píng)套路風(fēng)馬牛不相及的細(xì)胞制品命運(yùn)可想而知,一條“不能滿足藥物安全性評(píng)價(jià)”罪名足以將干細(xì)胞新藥統(tǒng)統(tǒng)打入冷宮,。藥物安全性評(píng)價(jià)要求藥物的基本要求,、安全、有效,、質(zhì)量可控 ,。上海專注藥物安全性評(píng)價(jià)外包
英瀚斯生物具有豐富的藥物安全性評(píng)價(jià)研究經(jīng)驗(yàn)和GLP管理經(jīng)驗(yàn)。值得信賴藥物安全性評(píng)價(jià)機(jī)構(gòu)
特殊安全性試驗(yàn)包含:過敏性(局部,、全身和光敏毒性),、溶血性和局部(血管、皮膚,、黏膜,、肌肉等)刺激性等主要與局部、全身給藥相關(guān)的特殊安全性試驗(yàn),;復(fù)方制劑中多種成分毒性相互影響的試驗(yàn),;致突變?cè)囼?yàn);生殖毒性試驗(yàn),;致*試驗(yàn),;依賴性試驗(yàn),。藥物安全性評(píng)價(jià)主要數(shù)據(jù)指標(biāo)包含以下幾類:比較大耐受劑量(MTD)是指在急性毒性試驗(yàn)中,受試物不引起受試對(duì)象(實(shí)驗(yàn)動(dòng)物)出現(xiàn)死亡的比較大劑量,。比較大無毒性反應(yīng)劑量(NOAEL),,指藥物在一定時(shí)間內(nèi),按一定方式與機(jī)體接觸,,按一定的檢測(cè)方法或觀察指標(biāo),,不能觀察到任何損害作用的比較高劑量。**小致死劑量(MLD),,引起個(gè)別動(dòng)物死亡的**小劑量,。值得信賴藥物安全性評(píng)價(jià)機(jī)構(gòu)
- 山東大鼠腦缺血再灌注模型哪家好 2025-06-01
- 內(nèi)蒙古推薦的腦缺血再灌注模型價(jià)格 2025-06-01
- 山東比較好的肺纖維化模型如何構(gòu)建 2025-06-01
- 內(nèi)蒙古MCO腦缺血再灌注模型公司 2025-06-01
- 江西推薦的臨床前動(dòng)物實(shí)驗(yàn)外包 2025-05-31
- 貴州有什么臨床前動(dòng)物實(shí)驗(yàn)機(jī)構(gòu) 2025-05-31
- 湖北高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)價(jià)格 2025-05-31
- 上海靠譜臨床前動(dòng)物實(shí)驗(yàn) 2025-05-31
- 海南專業(yè)臨床前動(dòng)物實(shí)驗(yàn)檢測(cè) 2025-05-31
- 四川推薦的臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià) 2025-05-31
- 深圳內(nèi)窺鏡模組廠家 2025-06-01
- 安徽二類械字號(hào)貼劑供應(yīng) 2025-06-01
- 無錫國內(nèi)人工智能輔助診斷設(shè)備銷售方法 2025-06-01
- 國產(chǎn)小型集中供水系統(tǒng)品牌 2025-06-01
- 無錫綠地人工智能輔助診斷設(shè)備收費(fèi) 2025-06-01
- 山東研究蛋白質(zhì)組學(xué)自動(dòng)化設(shè)備 2025-06-01
- 湖南可靠共享輪椅價(jià)格 2025-06-01
- 天津?qū)I(yè)ELISA試劑盒 2025-06-01
- 東北新世紀(jì)牙托粉價(jià)格 2025-06-01
- 廣州附近太空艙按摩椅 2025-06-01