浙江專注藥物安全性評價多少錢
特殊安全性試驗包含:過敏性(局部、全身和光敏毒性),、溶血性和局部(血管、皮膚,、黏膜,、肌肉等)刺激性等主要與局部,、全身給藥相關(guān)的特殊安全性試驗,;復(fù)方制劑中多種成分毒性相互影響的試驗;致突變試驗,;生殖毒性試驗,;致*試驗,;依賴性試驗。藥物安全性評價主要數(shù)據(jù)指標(biāo)包含以下幾類:比較大耐受劑量(MTD)是指在急性毒性試驗中,,受試物不引起受試對象(實驗動物)出現(xiàn)死亡的比較大劑量,。比較大無毒性反應(yīng)劑量(NOAEL),,指藥物在一定時間內(nèi),,按一定方式與機(jī)體接觸,按一定的檢測方法或觀察指標(biāo),不能觀察到任何損害作用的比較高劑量,。**小致死劑量(MLD),,引起個別動物死亡的**小劑量,。藥物安全性評價中的統(tǒng)計學(xué)應(yīng)用都有哪些,?浙江專注藥物安全性評價多少錢
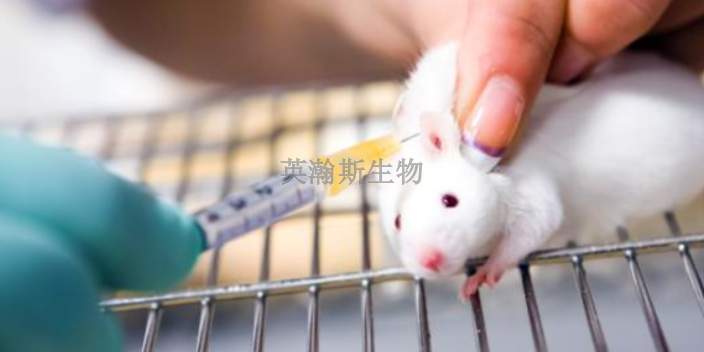
世界監(jiān)管科學(xué)促進(jìn)創(chuàng)新藥發(fā)展舉措收到實效:(1)通過新藥評審溝通活動,促進(jìn)藥物開發(fā),;(2)促進(jìn)在藥物開發(fā)過程中與臨床試驗發(fā)起人交流;(3)促進(jìn)生物標(biāo)志物與藥物基因組學(xué)應(yīng)用,,促進(jìn)以患者報告和其他重點評價工具開發(fā);(4)促進(jìn)罕見病藥物開發(fā),;(5)在新藥審評中使用風(fēng)險效益評價工具;(6)以患者為中心的藥物開發(fā)項目,,召開相關(guān)會議公布總結(jié)報告;(7)藥品安全體系現(xiàn)代化,,評價風(fēng)險評估與減低策略(REMS)的實施效果,促進(jìn)REMS標(biāo)準(zhǔn)化以進(jìn)一步融入醫(yī)療保健體系,;(8)通過主動監(jiān)測體系開展藥物安全性評價,,促進(jìn)藥物警戒現(xiàn)代化;(9)提交eCTD文件提高效率,,提高藥品審評效率;(10)加速新藥審評,,促進(jìn)新藥和原創(chuàng)性生物大分子藥審評透明度與溝通交流項目,,以促進(jìn)創(chuàng)新藥審評審批,。浙江專注藥物安全性評價多少錢英瀚斯藥物安全性評價研究 遵循國內(nèi)GLP管理規(guī)范及國外相關(guān)法規(guī)要求。

一直認(rèn)為,,安全性和有效性是藥物的基本標(biāo)準(zhǔn),,對食品和食品補(bǔ)充劑也應(yīng)該采用類似標(biāo)準(zhǔn),至少在成分分析和科學(xué)研究支持方面,,需要提供基本的證據(jù),,可以不需要大規(guī)模雙盲對照的臨床研究數(shù)據(jù),至少要有初步的臨床研究結(jié)果,,尤其是藥物安全性評價的評價指標(biāo),。**起碼,哪怕是沒有效果,,也不要存在毒性,。食品補(bǔ)充劑不像藥物那樣,,在投放市場前必須提供安全性和有效性的證據(jù),,法律上也沒有批準(zhǔn)FDA授權(quán)的食品補(bǔ)充劑。FDA只有對上市的食品補(bǔ)充劑發(fā)現(xiàn)存在不安全問題時才發(fā)揮監(jiān)管作用,。
動物的攻毒實驗完成且滿足一系列其它評價指標(biāo)后,,便可申請臨床試驗進(jìn)行藥物安全性評價。根據(jù)國家食品藥品監(jiān)督管理局發(fā)布的《疫苗臨床試驗技術(shù)指導(dǎo)原則》,,疫苗的人體臨床試驗需要經(jīng)歷四期,。Ⅰ期重點觀察安全性,即是否有副作用和不良反應(yīng),;Ⅱ期觀察或者評價疫苗在目標(biāo)人群中是否能獲得預(yù)期效果(通常指免疫原性)和一般安全性信息,;Ⅲ期試驗的目的為***評價疫苗的保護(hù)效果和安全性,該期是獲得注冊批準(zhǔn)的基礎(chǔ),;Ⅳ期臨床試驗是疫苗注冊上市后,對疫苗實際應(yīng)用人群的安全性和有效性進(jìn)行綜合評價,。非臨床藥物安全性評價研究是藥物研發(fā)的基礎(chǔ)性工作。
疫苗新藥臨床前研究中的藥物安全性評價內(nèi)容:(6)佐劑佐劑被用于提高非復(fù)制性滅活疫苗的免疫原性,、增強(qiáng)低應(yīng)答人群如老年人或免疫抑制患者的免疫應(yīng)答,、改善經(jīng)黏膜途徑接種的疫苗的免疫原性和調(diào)節(jié)不恰當(dāng)?shù)拿庖邞?yīng)答從而提高保護(hù)性免疫理,。佐劑的使用可以抗原用量,,從而降低成本,。鋁鹽佐劑是目前應(yīng)用**為***的一類佐劑,。此外人們發(fā)現(xiàn)許多中藥的活性成分(如苷類,、多糖等)具有很好的免疫調(diào)節(jié)作用,,其中QS-21、ISCOM等已進(jìn)入臨床試驗階段,,另外黃芷多糖(APS)等也表現(xiàn)出較好的應(yīng)用前景,。目前關(guān)于新佐劑的臨床前安全性評價目前在國際上存在不同意見,。一種認(rèn)為疫苗在進(jìn)行安全性評價之前應(yīng)進(jìn)行佐劑的常規(guī)毒理學(xué)試驗,一種認(rèn)為佐劑和抗原聯(lián)合使用時,,其理化性質(zhì)或生物活性與單獨使用時不同,因此進(jìn)行單獨佐劑的常規(guī)毒理學(xué)研究沒有實際意義,。由于疫苗本質(zhì)上是一類特殊的藥品,其接種的對象都是健康人群,,其中多數(shù)疫苗用于健康兒童,,因此在其研究過程中對安全性的考慮尤為重要。藥物安全性評價技術(shù)和方法是目前各國學(xué)者研究的熱點,。青海個性化藥物安全性評價實驗
英瀚斯承接生殖毒性試驗等藥物安全性評價實驗,。浙江專注藥物安全性評價多少錢
FDA批準(zhǔn)時已知的新型療法的特征包括藥物類別,、***領(lǐng)域,、優(yōu)先審評,、加速批準(zhǔn)、孤兒藥狀態(tài),、接近監(jiān)管期限批準(zhǔn)和監(jiān)管審查時間,。從2001年到2010年,,F(xiàn)DA批準(zhǔn)了222種新型***藥物。生物制劑,、精神類藥物,、加速審批和接近監(jiān)管期限的批準(zhǔn)與更高的事件發(fā)生率呈***的統(tǒng)計學(xué)相關(guān),突顯了在整個生命周期中對新型藥物安全性評價進(jìn)行持續(xù)監(jiān)測的必要性,。這些研究針對美國FDA批準(zhǔn)新藥上市后的安全性事件的主要研究結(jié)果和措施,為出于安全考慮而將藥品退市,、上市后逐步增加的黑框警示以及FDA發(fā)布安全通訊提供依據(jù)。浙江專注藥物安全性評價多少錢
南京英瀚斯生物科技有限公司致力于醫(yī)藥健康,,是一家服務(wù)型的公司,。公司自成立以來,以質(zhì)量為發(fā)展,,讓匠心彌散在每個細(xì)節(jié),,公司旗下實驗外包,,動物模型構(gòu)建,細(xì)胞分子實驗,,病理檢測深受客戶的喜愛,。公司從事醫(yī)藥健康多年,有著創(chuàng)新的設(shè)計,、強(qiáng)大的技術(shù),,還有一批**的專業(yè)化的隊伍,,確保為客戶提供良好的產(chǎn)品及服務(wù)。英瀚斯生物立足于全國市場,,依托強(qiáng)大的研發(fā)實力,,融合前沿的技術(shù)理念,飛快響應(yīng)客戶的變化需求,。
- 湖北比較好的子宮內(nèi)膜異位癥模型有哪些 2025-06-05
- 陜西推薦的藥效學(xué)公司 2025-06-05
- 福建子宮內(nèi)膜異位癥模型 2025-06-05
- 內(nèi)蒙古靠譜的子宮內(nèi)膜異位癥模型 2025-06-05
- 江西專門做子宮內(nèi)膜異位癥模型動物實驗外包 2025-06-05
- 寧夏靠譜的子宮內(nèi)膜異位癥模型造模方法 2025-06-05
- 陜西真實的子宮內(nèi)膜異位癥模型有哪些 2025-06-05
- 青??孔V的子宮內(nèi)膜異位癥模型怎么造模 2025-06-05
- 陜西真實的子宮內(nèi)膜異位癥模型是哪家 2025-06-05
- 海南比較好的子宮內(nèi)膜異位癥模型如何構(gòu)建 2025-06-04
- 安康國產(chǎn)成人益生菌好處 2025-06-05
- 天津高性價比生物反應(yīng)器 2025-06-05
- 奉賢區(qū)在線信息系統(tǒng)集成設(shè)計 2025-06-05
- 重慶菌群失調(diào)yFMT美益添放化療手術(shù)后患者 2025-06-05
- 虹口區(qū)哪些醫(yī)療器械批發(fā) 2025-06-05
- 中山健康按摩椅廠家 2025-06-05
- 廣東全自動核酸提取儀定制價格 2025-06-05
- 新疆假肢哪家好 2025-06-05
- 腦外科手術(shù)床 2025-06-05
- 中山好的太空艙按摩椅常見問題 2025-06-05