舟山代辦醫(yī)療器械注冊備案第三方機構
評估醫(yī)療設備注冊備案的成功率和風險需要考慮多個因素。首先,,成功率可以通過以下指標來評估:1.完整性和準確性:評估備案申請材料的完整性和準確性,,包括技術文件、測試報告,、質量管理體系等,。如果材料不完整或存在錯誤,可能導致備案失敗,。2.法規(guī)合規(guī)性:評估備案申請是否符合相關法規(guī)和標準要求,。如果備案申請不符合法規(guī)要求,可能會被拒絕,。3.專業(yè)指導:評估備案申請過程中是否有專業(yè)人士提供指導和支持,。專業(yè)指導可以提高備案成功率。風險評估方面,,可以考慮以下因素:1.法規(guī)風險:評估備案申請是否符合相關法規(guī)和標準要求,。如果備案申請存在法規(guī)風險,可能會面臨法律責任,。2.技術風險:評估備案的醫(yī)療設備技術是否成熟和可靠,。如果技術存在風險,可能會導致備案失敗或產品質量問題,。3.市場風險:評估備案的醫(yī)療設備在市場上的競爭情況和市場需求,。如果市場競爭激烈或市場需求不足,備案成功后的市場表現(xiàn)可能不理想,。注冊備案的醫(yī)療設備可以促進醫(yī)療技術的創(chuàng)新和發(fā)展,。舟山代辦醫(yī)療器械注冊備案第三方機構
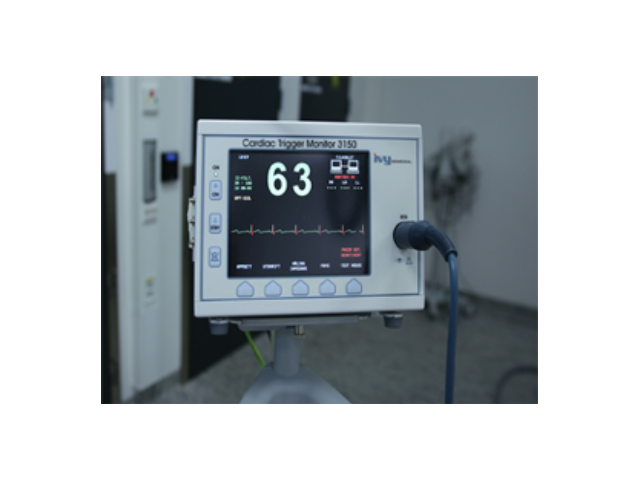
醫(yī)療設備注冊備案的流程通常包括以下幾個步驟:1.準備資料:首先,需要準備相關的申請資料,,包括設備的技術規(guī)格,、性能測試報告、生產工藝流程,、質量管理體系文件等,。2.選擇注冊機構:根據(jù)設備的類別和適用范圍,選擇合適的注冊機構進行注冊備案,。注冊機構可以是國家藥品監(jiān)督管理局的下屬機構或者是認可的第三方機構,。3.提交申請:將準備好的資料提交給注冊機構,,填寫相關的申請表格,并繳納相應的注冊費用,。4.技術評審:注冊機構會對提交的資料進行技術評審,,包括對設備的安全性、有效性,、質量控制等方面進行評估,。5.抽樣檢驗:根據(jù)需要,注冊機構可能會對設備進行抽樣檢驗,,以驗證其符合相關的技術標準和法規(guī)要求,。6.審核和批準:注冊機構會對評審結果進行審核,并根據(jù)評審結果決定是否批準設備的注冊備案,。如果通過審核,,將頒發(fā)注冊證書或備案證明。7.監(jiān)督檢查:注冊備案后,,注冊機構可能會進行定期或不定期的監(jiān)督檢查,,以確保設備的質量和安全性能得到持續(xù)的保證。常州醫(yī)療器械設備注冊備案怎么辦理注冊備案的醫(yī)療設備可以提供更可靠的診斷和醫(yī)療效果,。
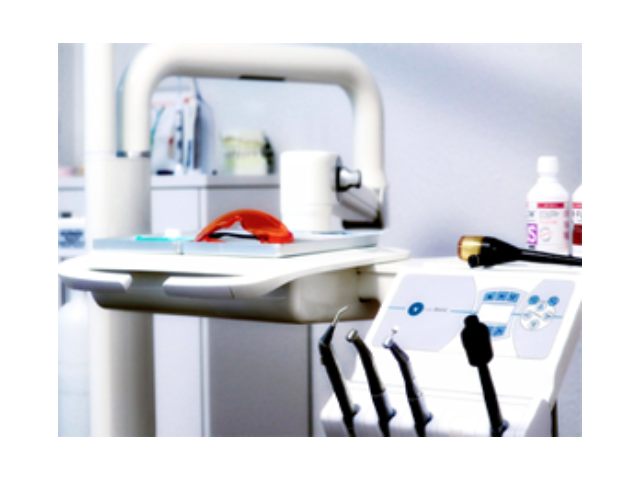
醫(yī)療設備注冊備案是指將醫(yī)療設備納入國家監(jiān)管范圍,,確保其安全有效使用的過程。以下是一般的醫(yī)療設備注冊備案流程:1.準備資料:收集相關的申請材料,,包括產品說明書,、技術文件、質量管理體系文件等,。2.選擇備案機構:根據(jù)設備的類別和規(guī)模,,選擇合適的備案機構進行備案申請。3.填寫備案申請表:根據(jù)備案機構提供的申請表格,,填寫相關信息,,包括設備的基本信息、生產商信息,、質量管理體系等,。4.提交申請材料:將填寫完整的備案申請表和相關資料提交給備案機構。5.審核評估:備案機構將對申請材料進行審核評估,,包括設備的技術性能,、安全性、有效性等方面的評估,。6.技術審查:備案機構可能會要求進行技術審查,,包括對設備的技術文件進行審查,以確保其符合相關的技術標準和法規(guī)要求。7.現(xiàn)場檢查:備案機構可能會進行現(xiàn)場檢查,,對生產廠家的生產設施,、質量管理體系進行檢查,以確保設備的質量和安全性,。8.審批備案:備案機構完成審核評估和現(xiàn)場檢查后,,根據(jù)相關法規(guī)和標準,決定是否批準備案,。9.發(fā)放備案證書:備案機構將發(fā)放備案證書,,確認該設備已經(jīng)完成注冊備案。
醫(yī)療設備注冊備案是指將醫(yī)療設備納入國家監(jiān)管范圍并獲得合法銷售和使用的過程,?;疚募ㄒ韵聨讉€方面:1.產品注冊申請表:申請人需要填寫詳細的產品信息,包括設備名稱,、型號、規(guī)格,、用途,、生產廠家等。2.產品技術資料:包括產品的技術說明書,、設計圖紙,、工藝流程、材料清單等,,以證明產品的安全性,、有效性和符合相關技術標準。3.臨床試驗報告:對于高風險類別的醫(yī)療設備,,通常需要進行臨床試驗,,申請人需要提供試驗方案、試驗結果和分析報告等,。4.生產質量管理體系文件:包括質量手冊,、程序文件、工藝文件,、檢驗記錄等,,以證明生產過程符合質量管理要求。5.注冊證明文件:包括生產許可證,、醫(yī)療器械注冊證等,,以證明申請人具備生產和銷售醫(yī)療設備的資質。6.相關認證證書:如ISO9001質量管理體系認證,、ISO13485醫(yī)療器械質量管理體系認證等,,以證明產品符合國際標準和質量要求。醫(yī)療設備注冊備案是指將醫(yī)療設備納入國家監(jiān)管范圍。

醫(yī)療設備注冊備案中的臨床試驗要求是根據(jù)國家相關法規(guī)和規(guī)范來進行的,。一般來說,,臨床試驗是為了評估醫(yī)療設備的安全性和有效性,確保其在臨床應用中的可靠性和有效性,。臨床試驗的要求包括以下幾個方面:1.試驗設計:臨床試驗應該有明確的研究目的和研究計劃,,包括試驗設計、樣本量計算,、試驗分組等,。試驗設計應該科學合理,能夠回答研究問題,。2.受試者選擇:臨床試驗應該選擇符合研究目的的受試者群體,,并進行充分的受試者知情同意。受試者的選擇應該符合倫理要求,,確保試驗的道德性和可行性,。3.試驗過程:臨床試驗應該按照試驗方案進行,包括試驗操作,、數(shù)據(jù)采集和記錄,、試驗終止等。試驗過程應該嚴格遵守相關規(guī)范和標準操作程序,,確保試驗結果的可靠性和可重復性,。4.安全監(jiān)測:臨床試驗應該進行安全監(jiān)測,及時發(fā)現(xiàn)和處理試驗中可能出現(xiàn)的不良事件和不良反應,。安全監(jiān)測應該符合相關規(guī)范和要求,,確保試驗的安全性和受試者的權益。5.數(shù)據(jù)分析:臨床試驗完成后,,應該對試驗數(shù)據(jù)進行統(tǒng)計分析和解讀,,評估醫(yī)療設備的安全性和有效性。數(shù)據(jù)分析應該符合統(tǒng)計學原理和方法,,確保分析結果的科學性和可靠性,。注冊備案過程中,需要經(jīng)過嚴格的審核和評估,,確保設備符合國家標準和法規(guī)要求,。臺州專業(yè)醫(yī)療器械注冊備案公司
注冊備案有助于規(guī)范醫(yī)療設備市場秩序,減少假冒偽劣產品,。舟山代辦醫(yī)療器械注冊備案第三方機構
醫(yī)療設備注冊備案的費用是根據(jù)不同國家和地區(qū)的法規(guī)和政策而有所不同,。一般來說,醫(yī)療設備注冊備案的費用包括申請費,、審查費,、年度費等,。申請費是指提交注冊備案申請時需要繳納的費用,用于覆蓋相關機構對申請材料的初步審查和處理,。審查費是指在申請材料通過初步審查后,,相關機構對設備進行詳細審查和評估所收取的費用。年度費是指注冊備案成功后,,每年需要繳納的費用,,用于設備的監(jiān)管和維護。具體的費用標準和計算方式需要根據(jù)不同國家和地區(qū)的法規(guī)和政策來確定,。一般來說,,費用會根據(jù)設備的類別、風險等級,、注冊備案的程序和要求等因素而有所差異,。此外,不同國家和地區(qū)的醫(yī)療設備監(jiān)管機構也可能會對費用進行調整和更新,。因此,,如果您需要了解具體的醫(yī)療設備注冊備案費用,建議您咨詢當?shù)氐尼t(yī)療設備監(jiān)管機構或專業(yè)咨詢機構,,以獲取準確和全新的信息,。他們將能夠為您提供詳細的費用說明和指導。舟山代辦醫(yī)療器械注冊備案第三方機構
- 舟山一類醫(yī)療器械注冊備案中心 2025-05-08
- 上海醫(yī)療設備注冊備案 2025-05-08
- 南京二類醫(yī)療器械注冊備案收費標準 2025-05-08
- 醫(yī)用設備注冊備案代辦 2025-05-08
- 紹興專業(yè)醫(yī)療器械注冊備案 2025-05-08
- 浙江二類醫(yī)療器械注冊備案收費標準 2025-05-08
- 蘇州醫(yī)療器械設備注冊備案第三方機構 2025-05-07
- 南京醫(yī)用設備注冊備案團隊 2025-05-07
- 常州代辦醫(yī)療器械注冊備案代辦 2025-05-07
- 常州注冊備案 2025-05-07
- 河源招工找活日結 2025-05-08
- 邢臺哪個企業(yè)進出口備案好 2025-05-08
- 長寧區(qū)專用汽車設計開發(fā)信息中心 2025-05-08
- 青海短租空壓機租賃 2025-05-08
- 紹興土壤環(huán)境檢測去哪個部門 2025-05-08
- 鎮(zhèn)江市綠色建筑咨詢 2025-05-08
- 上海農產品土壤檢測 2025-05-08
- 宿遷綜合建筑勞務分包信息中心 2025-05-08
- 南京品牌小程序怎么收費 2025-05-08
- 赤峰信息全域一站式人工智能運營活動 2025-05-08