澳大利亞的藥品電子通用技術(shù)文檔(eCTD)注冊申報(bào)體系是澳大利亞y藥品商品管理局(TGA)推動藥品審評現(xiàn)代化的重要舉措,。eCTD作為國際通行的電子化注冊申報(bào)標(biāo)準(zhǔn),,通過結(jié)構(gòu)化數(shù)據(jù)格式(如XML)整合了藥品質(zhì)量,、安全性和有效性的技術(shù)文檔,,實(shí)現(xiàn)了從傳統(tǒng)紙質(zhì)遞交向數(shù)字化流程的轉(zhuǎn)型,。根據(jù)TGA要求,eCTD需遵循通用技術(shù)文檔(CTD)框架,,分為五個模塊:模塊1包含澳洲特定的行政信息(如產(chǎn)品說明書草案和GMP證明),;模塊2為質(zhì)量、非臨床及臨床研究的綜述與總結(jié),;模塊3至模塊5則分別涵蓋藥學(xué),、非臨床和臨床的詳細(xì)數(shù)據(jù)。澳大利亞自2024年起加速推進(jìn)eCTD實(shí)施,,要求創(chuàng)新藥注冊申報(bào)優(yōu)先采用該格式,,以提升審評效率并支持全球同步申報(bào)。 申報(bào)流程上,,企業(yè)需通過TGA指定的電子提交門戶(如eSubmission Gateway)上傳eCTD序列,,并在受理后5個工作日內(nèi)同步提交紙質(zhì)版模塊1-5資料。瑞士NDA注冊申報(bào)相關(guān)技術(shù)支持,。河南歐盟eCTD

eCTD提交流程與ESG系統(tǒng):FDA要求通過電子提交網(wǎng)關(guān)(ESG)傳輸eCTD文件,,單個文件大小限制為10GB,超限需拆分或通過物理介質(zhì)(如光盤)遞交,。提交前需預(yù)分配申請?zhí)枺ㄈ鏝DA編號),,并通過ESG測試賬戶驗(yàn)證技術(shù)合規(guī)性。序列號命名規(guī)則為4位數(shù)字(如0001),,申請需從“原申請”序列開始,,補(bǔ)充資料按遞增順序編號。企業(yè)可自愿提交預(yù)審樣本(Pre-Submission),,F(xiàn)DA將反饋文檔結(jié)構(gòu),、元數(shù)據(jù)等合規(guī)性問題。驗(yàn)證標(biāo)準(zhǔn)與常見錯誤類型:FDA驗(yàn)證標(biāo)準(zhǔn)分為高(High),、中(Medium),、低(Low)三級,,高風(fēng)險錯誤(如無效XML或缺失關(guān)鍵表格)必須修復(fù),否則直接拒收,。常見問題包括:重復(fù)序列號(錯誤1034),、文件路徑超長(警告2015)、PDF加密或非標(biāo)字體(錯誤4001),。2023年統(tǒng)計(jì)顯示,,30%的提交因模塊1格式錯誤被退回,凸顯行政信息合規(guī)的重要性,。驗(yàn)證工具如LORENZ eValidator被FDA官方采用,,可自動檢測200+項(xiàng)技術(shù)指標(biāo)。江蘇電子申報(bào)eCTD是什么eCTD申報(bào)相關(guān)技術(shù)支持,。
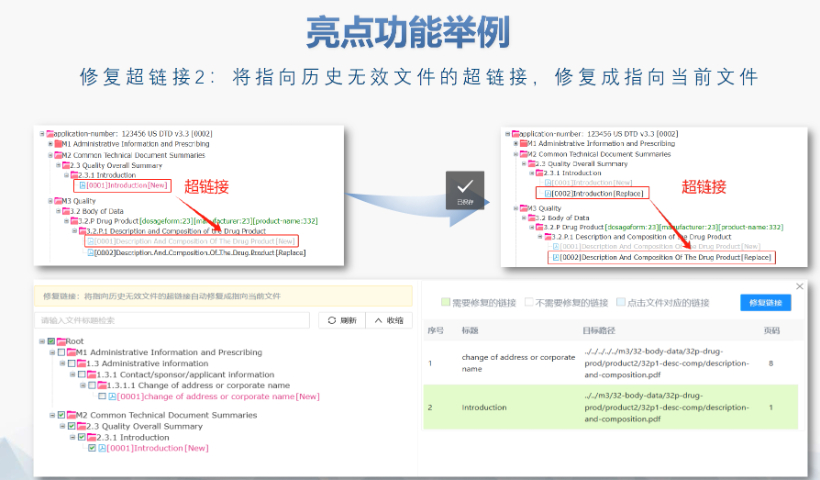
歐盟eCTD的歷史沿革與強(qiáng)制實(shí)施 歐盟自2003年逐步推進(jìn)eCTD(電子通用技術(shù)文檔)的標(biāo)準(zhǔn)化進(jìn)程,,初要求藥注冊申請(MAA)采用CTD格式。2010年,,集中審評程序(CP)率先強(qiáng)制使用eCTD,,隨后分散程序(DCP)和互認(rèn)程序(MRP)分別于2015年、2017年跟進(jìn),。至2019年,,歐盟要求所有國家程序(NP)的注冊申請均以eCTD格式提交,標(biāo)志著其電子遞交體系的成熟,。2024年,,EMA啟動eCTD4.0試點(diǎn)項(xiàng)目,,旨在提升技術(shù)兼容性與審評效率,。 eCTD驗(yàn)證標(biāo)準(zhǔn)的迭代與關(guān)鍵更 歐盟的驗(yàn)證標(biāo)準(zhǔn)歷經(jīng)多次調(diào)整,例如2025年3月啟用的eCTD3.1區(qū)域模板和驗(yàn)證規(guī)則v8.1,,對文件結(jié)構(gòu),、元數(shù)據(jù)和內(nèi)容完整性提出更嚴(yán)格的要求。標(biāo)準(zhǔn)引入的“追蹤表(Tracking Table)”強(qiáng)制校驗(yàn)規(guī)則(如15.11和15.12)曾導(dǎo)致CEP(歐洲藥典適用性證書)遞交,,后通過允許占位文件臨時解決,。與早期版本相比,v8.1強(qiáng)化了對模塊一區(qū)域信息的邏輯驗(yàn)證,,并細(xì)化了對PDF書簽,、超鏈接的規(guī)范性檢查。
申報(bào)流程與要求 資料準(zhǔn)備 內(nèi)容要求:包括產(chǎn)品描述,、生產(chǎn)工藝(原材料來源,、設(shè)備參數(shù)等)、質(zhì)量控制標(biāo)準(zhǔn)(SOP,、穩(wěn)定性數(shù)據(jù)),、安全性與毒性研究等,。 格式規(guī)范: 采用CTD(通用技術(shù)文件)格式,按模塊分章節(jié)(如模塊3為CMC數(shù)據(jù)),。 電子提交需符合eCTD標(biāo)準(zhǔn)(文件小于10GB通過ESG系統(tǒng)提交,,超過可選用CD-ROM)。 提交與注冊 預(yù)分配DMF號:需在提交前申請,,確保文件與編號綁定,。 授權(quán)書(LOA):需向引用DMF的制劑廠商提供授權(quán)信,明確可查閱的章節(jié),。 費(fèi)用:Ⅱ類原料藥DMF需繳納年費(fèi)(2024年約9,468美元),。 FDA審核流程 行政審評:2-3周內(nèi)確認(rèn)文件完整性。 完整性審評(CA):針對Ⅱ類DMF,,約60天,。 技術(shù)審評:在DMF被制劑申請(如ANDA、NDA)引用時啟動,,周期60-180天,。 結(jié)果反饋:FDA可能要求補(bǔ)充數(shù)據(jù),但DMF本身無“批準(zhǔn)”狀態(tài),,通過后可能收到“無進(jìn)一步意見函”(No Further Comment Letter),。美國eCTD驗(yàn)證標(biāo)準(zhǔn)相關(guān)技術(shù)支持。
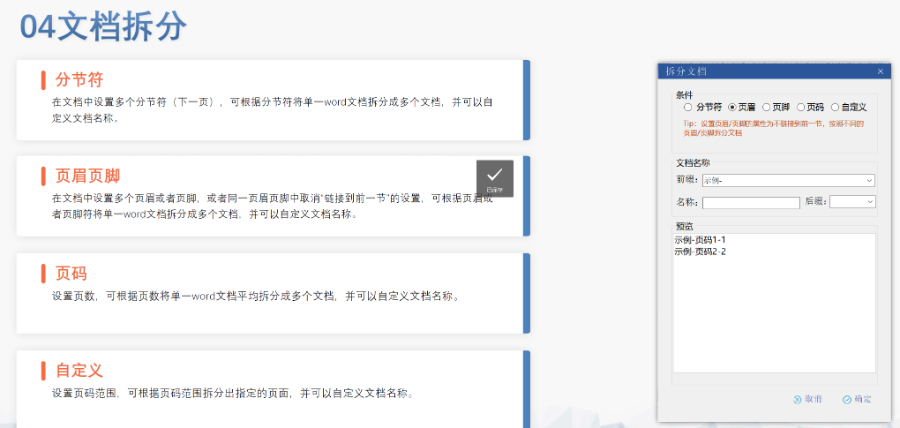
從紙質(zhì)到電子的歷史過渡 2017年前,,美國允許紙質(zhì)與eCTD并行提交,,但此后逐步淘汰紙質(zhì)通道,保留緊急情況下的例外審批,。2020年電子化后,,所有IND、NDA,、ANDA和DMF強(qiáng)制采用eCTD格式,。 系統(tǒng)平臺升級 FDA通過“藥品業(yè)務(wù)應(yīng)用系統(tǒng)”和“藥品eCTD注冊系統(tǒng)”實(shí)現(xiàn)電子資料接收、受理與審評的全流程數(shù)字化,。2022年系統(tǒng)增自動推送受理文書和短信提醒功能,,減少人工干預(yù)。 電子文檔結(jié)構(gòu)優(yōu)化 美國eCTD采用分層文件夾結(jié)構(gòu),,例如化學(xué)藥品的模塊1-5分別對應(yīng)行政文件,、總結(jié)報(bào)告、質(zhì)量數(shù)據(jù)等,。2020年后增“臨床試驗(yàn)數(shù)據(jù)庫”裝盒要求,,強(qiáng)化數(shù)據(jù)可追溯性。瑞士eCTD注冊申報(bào)相關(guān)技術(shù)支持。山東eCTD業(yè)務(wù)
歐盟eCTD注冊咨詢相關(guān)技術(shù)支持,。河南歐盟eCTD
GDUFA III框架與費(fèi)用分類 2022年更的GDUFA III將費(fèi)用分為ANDA申請費(fèi),、DMF認(rèn)證費(fèi)、項(xiàng)目費(fèi)及設(shè)施費(fèi)四類,,實(shí)施周期至2027年,。2025財(cái)年ANDA費(fèi)用漲至約22萬美元,較2024年增幅達(dá)27.5%,,反映審評成本上升,。 ANDA申請費(fèi)規(guī)則 費(fèi)用需在提交時繳納,若申請被拒可退還75%,。重提交視為申請,,需再次繳費(fèi)。關(guān)聯(lián)API的工廠數(shù)量影響總費(fèi)用,,例如某ANDA引用3個API且涉及6家工廠,,需支付6倍DMF費(fèi)用。 DMF費(fèi)用機(jī)制 II類原料藥DMF需在引用前繳費(fèi),,一次性支付約5.3萬美元(2025財(cái)年),。未繳費(fèi)DMF不得用于支持ANDA,否則觸發(fā)退審,。 項(xiàng)目費(fèi)分級管理 根據(jù)企業(yè)獲批ANDA數(shù)量分為大,、中、小型三級,,2025年大型企業(yè)年費(fèi)約34萬美元,。附屬公司ANDA數(shù)量合并計(jì)算,繳費(fèi)責(zé)任可由母公司或任一附屬公司承擔(dān),。河南歐盟eCTD
賦悅科技(杭州)有限責(zé)任公司在同行業(yè)領(lǐng)域中,,一直處在一個不斷銳意進(jìn)取,不斷制造創(chuàng)新的市場高度,,多年以來致力于發(fā)展富有創(chuàng)新價值理念的產(chǎn)品標(biāo)準(zhǔn),,在浙江省等地區(qū)的數(shù)碼,、電腦中始終保持良好的商業(yè)口碑,,成績讓我們喜悅,但不會讓我們止步,,殘酷的市場磨煉了我們堅(jiān)強(qiáng)不屈的意志,,和諧溫馨的工作環(huán)境,富有營養(yǎng)的公司土壤滋養(yǎng)著我們不斷開拓創(chuàng)新,,勇于進(jìn)取的無限潛力,,賦悅科技供應(yīng)攜手大家一起走向共同輝煌的未來,回首過去,,我們不會因?yàn)槿〉昧艘稽c(diǎn)點(diǎn)成績而沾沾自喜,,相反的是面對競爭越來越激烈的市場氛圍,,我們更要明確自己的不足,做好迎接新挑戰(zhàn)的準(zhǔn)備,,要不畏困難,,激流勇進(jìn),以一個更嶄新的精神面貌迎接大家,,共同走向輝煌回來,!