法規(guī)文檔管理系統(tǒng) 協(xié)同共享 RDMS可以讓跨區(qū)域、跨部門協(xié)同真正成為1+1>2的 工作,。讓頻繁的文檔共享傳輸,,版本管理,生命周 期審批都變得輕松簡單 安全合規(guī) 通過詳細的審計追蹤,、電子簽名,、權限管理、網 關控制,、頁面控制等技術手段,,構建安全合規(guī)的 文檔管理系統(tǒng),通過安全驗證與合規(guī)驗證 統(tǒng)一文檔來源 藥品注冊是企業(yè)經營成果的技術資料,,由多個部門 長時間匯集到法規(guī)部門,。RDMS確保多部門文檔來 源統(tǒng)一,即使人員流動也可以快速接續(xù)工作 統(tǒng)一文檔結構 根據不同申報類型,,自動生成文檔結構,,讓法規(guī) 人員與跨部門同事掌握申報需要的資料需求,降 低溝通成本,,降低經驗需求,,避免疏忽遺漏加拿大eCTD注冊外包相關技術支持。安徽賦悅科技eCTD是什么
美國藥物主文件(Drug Master File, DMF)是向FDA提交的機密技術文件,,用于支持藥品生產,、質量控制及合規(guī)性審查。以下為申報的要點和流程總結: DMF概述與類型 定義與作用 DMF是藥品生產全過程的詳細檔案,,包含原料藥,、輔料、包裝材料等的生產設施,、工藝,、質量控制等信息,供制劑廠商引用以支持其注冊申請。其意義在于保護企業(yè)機密的同時,,滿足FDA對供應鏈透明度的要求,。 DMF類型 Ⅱ類:原料藥、中間體及制劑(如微生物外泌體,、細胞株等生物制品均屬此類),。 Ⅲ類:包裝材料。 Ⅳ類:輔料,、著色劑等添加劑,。 Ⅴ類:非臨床/臨床數(shù)據等特殊信息(需FDA預先批準)。 注:Ⅰ型(生產設施與人員)已于2000年停用,。江蘇原料藥eCTD使用美國eCTD注冊外包相關技術支持,。
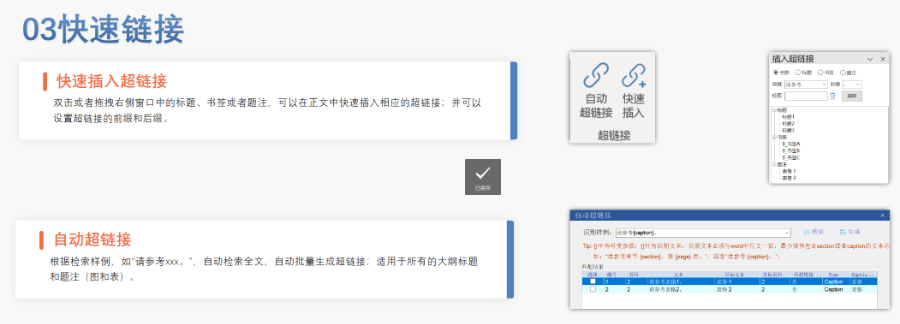
PDF工具箱 批量處理與格式修復 支持PDF合并、拆分,、提取頁面,、旋轉頁面等操作,可批量修復字體未嵌入,、超鏈接錯誤等問題,,確保文件符合藥品注冊法規(guī)要求。 智能書簽與超鏈接管理 提供書簽導入/導出,、超鏈接自動生成(支持關鍵字搜索定位鏈接),、題注超鏈接拖拽式編輯等功能,簡化復雜文檔的導航設計,。 文檔轉換與OCR識別 支持Word轉PDF(自動生成書簽,、嵌入字體),以及PDF與Word,、Excel等格式互轉,,集成OCR功能用于掃描件文字識別。 合規(guī)性驗證 自動驗證PDF的頁面布局,、頁碼連續(xù)性,、空白頁、目錄層級等屬性,,并定位具體錯誤位置,,減少人工檢查成本。 安全與協(xié)作功能 支持文檔加密,、數(shù)字簽名,、云端同步及多設備共享,滿足企業(yè)級文件安全管理需求,。
此次eCTD實施范圍的擴大對外企而言影響,。實施范圍的擴大為外企提供了更多選擇,,特別是在產品線中NDA和AND占比相當?shù)那闆r下。外企的系統(tǒng)和流程相對成熟,,因此它們對eCTD擴大范圍持積極態(tài)度,,更愿意嘗試和改變。盡管過程中可能遇到技術或法規(guī)上的問題,,但企業(yè)認為通過不斷反饋和與CDE溝通,,能夠幫助提高整體申報效率和質量。此外,,外企還面臨向更集成化法規(guī)信息管理系統(tǒng)的挑戰(zhàn),特別是當需要遷移到系統(tǒng)時,。如果盡早將產品遷移到eCTD,,無論是系統(tǒng)遷移還是后續(xù)的生命周期管理都會更加順暢。 隨著eCTD實施范圍的擴大,,供應商將擁有更多的業(yè)務機會,。然而,中國藥品注冊體系相對年輕化,,在推進eCTD實施過程中可能面臨各種問題,。短期內,中小企業(yè)可能面臨資金壓力,,需要考慮是否投入資金購買的eCTD系統(tǒng),。中長期來看,企業(yè)更關注的是如何建立一套完善的文檔管理體系,,而不是完成遞交,。這需要企業(yè)在前期投入更多時間和精力進行流程優(yōu)化和人員培訓。加拿大IND注冊申報相關技術支持,。
危機應對與應急遞交機制 在公共衛(wèi)生緊急事件(如COVID-19)中,,EMA允許簡化eCTD序列,優(yōu)先審評關鍵模塊并暫緩非數(shù)據,。申請人可通過快速通道(Fast Track)提交疫苗或藥物的eCTD資料,,審評周期可壓縮至6個月。此類申請需附風險評估報告,,并承諾后續(xù)補交完整數(shù)據,。 數(shù)據安全與長期存檔 歐盟要求eCTD資料存檔期限至少為藥品上市后30年,EMA采用分布式存儲和區(qū)塊鏈技術確保數(shù)據不可篡改,。申請人需定期備份本地副本,,并使用符合GDPR要求的加密傳輸協(xié)議(如AS2)遞交。歷史數(shù)據的遷移和格式轉換(如NeeS轉eCTD)需遵循特定技術規(guī)范,。 環(huán)保效益與可持續(xù)發(fā)展 eCTD取代紙質遞交后,,歐盟每年減少約500噸紙張消耗,,審評流程的數(shù)字化降低碳足跡約30%。虛擬審評會議和電子簽名進一步減少了差旅需求,,契合歐盟2050碳中和目標,。未來,eCTD4.0將通過數(shù)據壓縮技術進一步降低服務器能耗,。加拿大eCTD申報軟件相關技術支持,。安徽原料藥eCTD業(yè)務
瑞士eCTD注冊外包相關技術支持。安徽賦悅科技eCTD是什么
eCTD的實施為監(jiān)管機構和企業(yè)帶來了多重機遇,。電子化申報資料能夠極大地加速審評效率,,減少人為判斷錯誤和數(shù)據混淆的情況,從而提高審評的準確性和速度,。同時,,eCTD帶來的數(shù)據標準化機遇使得全球監(jiān)管機構的資料內容和電子格式得以統(tǒng)一,有助于在不同監(jiān)管機構之間進行數(shù)據傳輸和共享,。這對于提升全球監(jiān)管效率和行業(yè)研發(fā)效率具有重要意義,。 此外,eCTD的實施還促進了國際合作,,構建了全球監(jiān)管的底層大數(shù)據基礎,。對于企業(yè)而言,eCTD提供了一個規(guī)范化的研發(fā)活動模板,,有助于降低與監(jiān)管機構溝通的成本,,提高申報效率。特別是對于國內的生物技術企業(yè)而言,,eCTD的實施更是具有重要意義,,有助于這些企業(yè)更好地走向國際市場。然而,,中小企業(yè)在享受這些機遇的同時,,也面臨著技術和成本壓力。eCTD的實施需要專門的團隊進行系統(tǒng)維護和開發(fā),,這對于中小企業(yè)來說是一筆不小的開支,。同時,數(shù)據安全問題也是企業(yè)關注的焦點,。 此次CDE擴大eCTD實施范圍對行業(yè)而言是一個積極的風向標,。短期內,企業(yè)面臨的挑戰(zhàn)包括適應更高要求的技術規(guī)范并提高文件質量,、和eCTD出版系統(tǒng)的磨合以及進行eCTD知識的跨職能培訓等,。 安徽賦悅科技eCTD是什么