杭州抗體試劑進出口審批流程
全球生物試劑市場規(guī)模龐大且持續(xù)增長,。在科研領(lǐng)域,生命科學(xué)研究不斷深入,,對生物試劑需求日益旺盛,,推動市場擴張。歐美地區(qū)科研投入高,,是主要消費市場,,擁有眾多有名生物試劑企業(yè),技術(shù)先進,、產(chǎn)品線豐富,。亞洲地區(qū),隨著經(jīng)濟發(fā)展和科研實力提升,,特別是中國,、印度等國家,市場潛力巨大,,需求增速高于全球平均水平,。從產(chǎn)品類型看,分子生物學(xué)試劑,、免疫診斷試劑等細分市場占據(jù)較大份額,。在進出口貿(mào)易中,發(fā)達國家多為不錯生物試劑出口國,,憑借技術(shù)優(yōu)勢把控重心產(chǎn)品供應(yīng),;發(fā)展中國家在中低端產(chǎn)品領(lǐng)域有一定競爭力,同時也是不錯試劑重要進口市場,。企業(yè)需結(jié)合市場趨勢,,找準(zhǔn)定位,制定合適進出口策略,,開拓市場份額,。生物試劑進口要了解目的國對生物試劑廣告宣傳的限制。杭州抗體試劑進出口審批流程
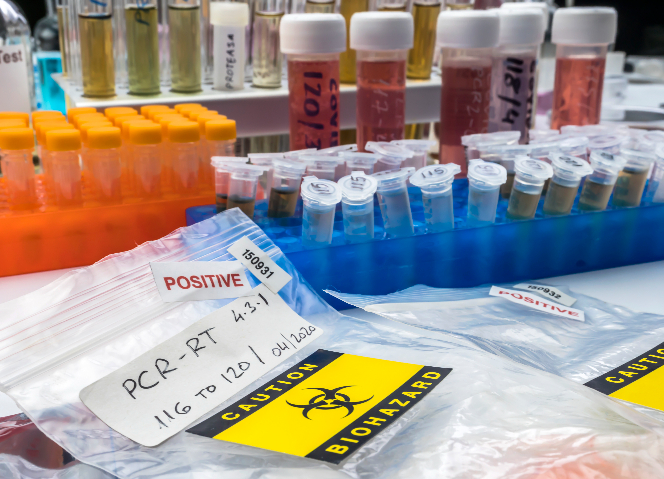
包裝和標(biāo)識在生物試劑進出口中舉足輕重,。包裝材料要堅固耐用,,且能適配試劑特性。強酸強堿類試劑要用耐腐蝕性包裝,,對光照敏感試劑需采用遮光包裝,,同時包裝要具備良好密封性,,防止泄漏。標(biāo)識方面,,必須清晰標(biāo)注產(chǎn)品名稱,、成分、規(guī)格,、生產(chǎn)企業(yè),、生產(chǎn)日期,、有效期,、儲存條件、使用說明等信息,。語言要符合目標(biāo)市場要求,,一般需用英語,在部分非英語國家,,可能還得翻譯成當(dāng)?shù)卣Z言,。對于危險生物試劑,要依據(jù)國際標(biāo)準(zhǔn)張貼危險貨物標(biāo)識,,如國際《關(guān)于危險貨物運輸?shù)慕ㄗh書》中的相關(guān)標(biāo)準(zhǔn),,以此保障運輸、儲存和使用過程中的安全,,避免因包裝標(biāo)識不當(dāng)引發(fā)安全事故或通關(guān)受阻,。上海港免疫診斷試劑進出口免費咨詢生物試劑進口需提前與目的國的代理溝通清關(guān)事宜。
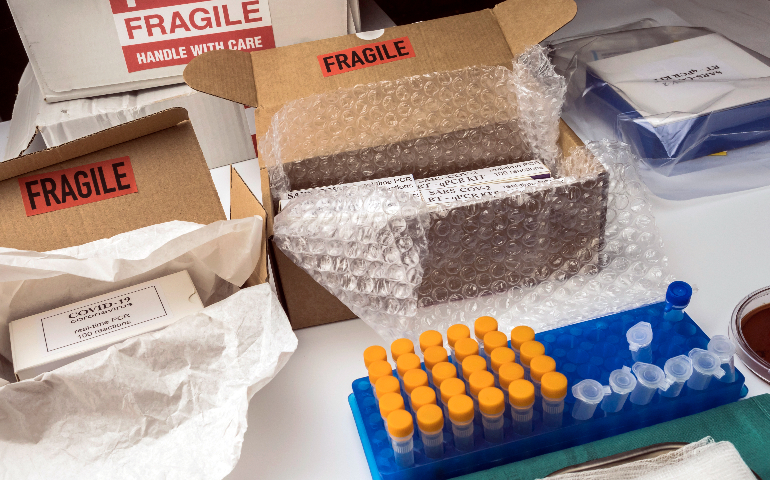
生物試劑對運輸條件要求嚴苛,。多數(shù)生物試劑具有溫度敏感性,,像酶、抗體等,,運輸中需嚴格維持特定溫度范圍,,否則易失活。常用冷鏈運輸方式,,包括干冰冷藏(適用于少量試劑短途運輸,,但要注意干冰揮發(fā)安全問題,確保包裝通風(fēng)),、低溫冷藏車(適合大量試劑長距離運輸,,車內(nèi)制冷設(shè)備需精細控溫)以及專業(yè)冷鏈物流服務(wù)。企業(yè)要挑選具備專業(yè)資質(zhì)和豐富經(jīng)驗的運輸商,,運輸前仔細檢查設(shè)備運行狀況,,運輸中實時監(jiān)控溫度并做好記錄,保證溫度符合試劑儲存要求,。對于易氧化,、潮解或需惰性氣體保護的生物試劑,,要采用適配的包裝和防護措施,防止試劑變質(zhì),。
進出口生物試劑均需通過嚴格檢驗檢疫,。出口時,企業(yè)要主動向海關(guān)與檢驗檢疫部門申報,,提供詳細產(chǎn)品信息,、生產(chǎn)批次、質(zhì)量檢測報告等資料,。檢驗檢疫部門會根據(jù)試劑特性與進口國要求,,進行質(zhì)量抽檢,檢測純度,、活性,、微生物限度等指標(biāo),對于一些傳染病診斷試劑,,對其微生物限度和特異性要求極高,。對可能攜帶病原體、有害生物因子的試劑進行生物安全檢測,,防止有害生物跨境傳播,。進口生物試劑時,同樣要接受我國檢驗檢疫部門查驗,,企業(yè)需配合做好貨物查驗,、抽樣檢測等工作,對于冷鏈生物試劑,,還要滿足冷鏈貨物檢驗檢疫要求,,如落實核酸檢測、消毒等防控措施,,確保產(chǎn)品符合國內(nèi)外檢驗檢疫標(biāo)準(zhǔn),,保障公共衛(wèi)生安全與市場秩序,為國內(nèi)科研,、醫(yī)療等領(lǐng)域提供安全可靠的生物試劑,。出口生物試劑要留意進口國對包裝材料材質(zhì)的要求。
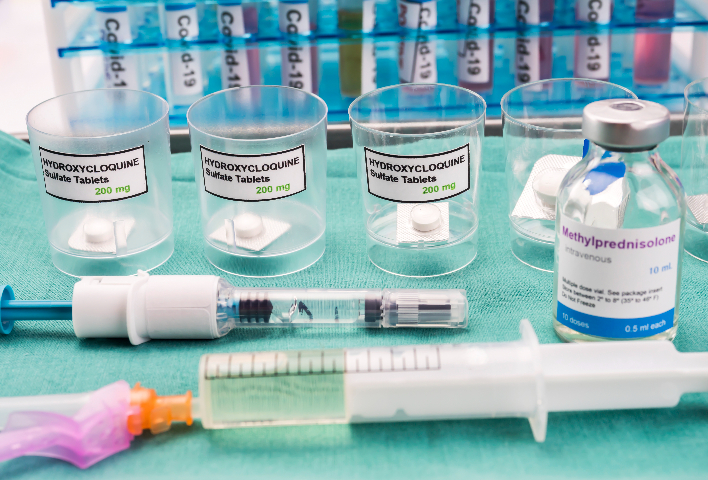
生物試劑進口的標(biāo)簽與說明書必須符合國內(nèi)政策要求,。標(biāo)簽應(yīng)清晰標(biāo)注產(chǎn)品名稱,、規(guī)格、生產(chǎn)企業(yè),、生產(chǎn)日期,、有效期、儲存條件,、批準(zhǔn)文號(注冊證編號)等關(guān)鍵信息,,且文字表述應(yīng)準(zhǔn)確,、規(guī)范,使用中文(可同時標(biāo)注外文),。說明書內(nèi)容要詳盡,,涵蓋產(chǎn)品組成、適用范圍,、使用方法,、注意事項、不良反應(yīng)等信息,,為使用者提供多方面指導(dǎo),。對于診斷類生物試劑,說明書還需明確檢測原理,、性能指標(biāo),、臨床預(yù)期用途等內(nèi)容,。標(biāo)簽與說明書的格式和內(nèi)容需經(jīng)監(jiān)管部門審核,,確保其符合《藥品說明書和標(biāo)簽管理規(guī)定》《醫(yī)療器械說明書和標(biāo)簽管理規(guī)定》等法規(guī),避免誤導(dǎo)使用者,,保障患者和消費者權(quán)益,。生物試劑進口申報時,需明確試劑的生物活性等級,。南京生物試劑進口政策
生物試劑進口需嚴格遵守目的國的生物安全相關(guān)管理規(guī)定,。杭州抗體試劑進出口審批流程
在生物試劑進出口領(lǐng)域,法規(guī)政策起著關(guān)鍵的規(guī)范作用,。不同國家和地區(qū)對生物試劑的進出口有著嚴格規(guī)定,。例如,我國依據(jù)《中華人民共和國藥品管理法》《醫(yī)療器械監(jiān)督管理條例》等法規(guī),,對作為藥品或醫(yī)療器械管理的生物試劑,,要求企業(yè)具備相應(yīng)資質(zhì),如藥品經(jīng)營許可證,、醫(yī)療器械經(jīng)營備案憑證等,。對于一些特殊生物試劑,可能還涉及《生物制品批簽發(fā)管理辦法》,,需取得批簽發(fā)證明方可進口,。美國食品藥品監(jiān)督管理局(FDA)對進口生物試劑也有詳細準(zhǔn)則,從產(chǎn)品注冊,、標(biāo)簽要求到生產(chǎn)質(zhì)量管理規(guī)范(GMP)符合性審查等,,確保產(chǎn)品安全有效。企業(yè)在開展進出口業(yè)務(wù)前,,務(wù)必深入研究目標(biāo)市場法規(guī),,完成各類許可申請與注冊流程,,避免因違規(guī)遭受處罰,影響業(yè)務(wù)開展,。杭州抗體試劑進出口審批流程
- 南京細胞培養(yǎng)試劑進出口審批備案代辦 2025-05-08
- 杭州細胞培養(yǎng)試劑進出口 2025-05-08
- 昆山國際貨運快遞企業(yè) 2025-05-08
- 杭州抗體試劑進出口審批流程 2025-05-08
- 南京食品國際快遞fedex折扣 2025-05-08
- 上海港化妝品國際快遞 2025-05-08
- 上海港生物試劑進口審批單 2025-05-08
- 無錫全球海中轉(zhuǎn)運國際快遞哪家好 2025-05-08
- 寧波酶類試劑進出口清關(guān)手續(xù) 2025-05-08
- 昆山免疫診斷試劑進出口流程 2025-05-08
- 質(zhì)量禮品組裝代發(fā) 2025-05-08
- 小包裹FBA退貨產(chǎn)品檢測優(yōu)勢 2025-05-08
- 江蘇鐵路運輸行業(yè)標(biāo)準(zhǔn) 2025-05-08
- 浙江小型貨物運輸搬遷服務(wù) 2025-05-08
- 蘇州提供道路貨物運輸銷售方法 2025-05-08
- 深圳散貨拼箱雙清到門專線物流 2025-05-08
- 江蘇高壓清洗電動環(huán)衛(wèi)車多少錢一輛 2025-05-08
- 中美手機海運航線推薦 2025-05-08
- 歐洲至中國雙向海運走哪里 2025-05-08
- 臺州滑板車控制器批發(fā) 2025-05-08