杭州酶類試劑進(jìn)出口審批備案代辦
進(jìn)出口生物試劑,,契合目標(biāo)市場(chǎng)標(biāo)準(zhǔn)是關(guān)鍵。出口時(shí),,產(chǎn)品必須滿足進(jìn)口國(guó)法規(guī)及相關(guān)國(guó)際標(biāo)準(zhǔn)。例如出口歐盟,,生物試劑需符合歐盟指令與協(xié)調(diào)標(biāo)準(zhǔn),,通過(guò) CE 認(rèn)證,涵蓋安全性,、健康影響等多方面評(píng)估,;出口美國(guó),則要符合美國(guó)食品藥品監(jiān)督管理局(FDA)要求并完成對(duì)應(yīng)注冊(cè)程序,。進(jìn)口生物試劑時(shí),,要確保符合我國(guó)藥品、醫(yī)療器械等相關(guān)法規(guī),。藥品類生物試劑需符合我國(guó)藥品注冊(cè)標(biāo)準(zhǔn),,從成分純度到穩(wěn)定性都有明確規(guī)范;醫(yī)療器械類生物試劑要完成國(guó)內(nèi)注冊(cè)或備案,,產(chǎn)品研發(fā),、生產(chǎn)、質(zhì)量控制等各環(huán)節(jié)都得達(dá)標(biāo),,否則無(wú)法順利通關(guān),,更不能進(jìn)入市場(chǎng)銷售,甚至可能面臨召回與處罰,。出口生物試劑要留意進(jìn)口國(guó)對(duì)產(chǎn)品說(shuō)明書(shū)語(yǔ)言的要求,。杭州酶類試劑進(jìn)出口審批備案代辦
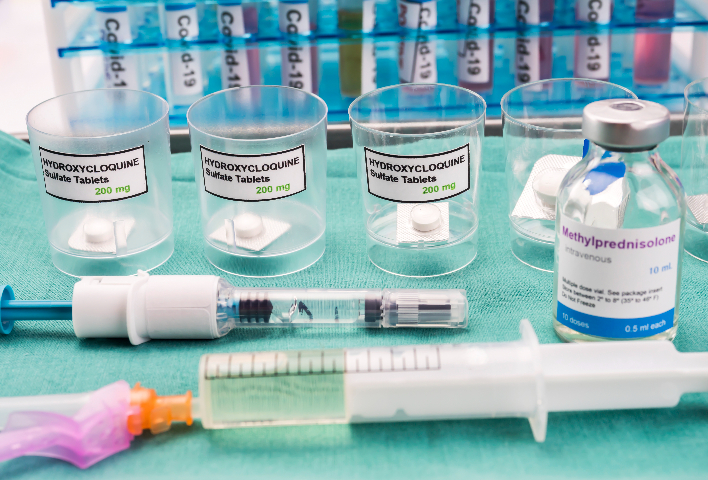
生物試劑進(jìn)口受多層面政策法規(guī)約束。在我國(guó),,國(guó)家藥品監(jiān)督管理局(NMPA)主導(dǎo)生物試劑進(jìn)口監(jiān)管,,依據(jù)《中華人民共和國(guó)藥品管理法》《醫(yī)療器械監(jiān)督管理?xiàng)l例》等重心法規(guī)構(gòu)建政策體系??傮w上,,進(jìn)口生物試劑需確保來(lái)源合法、質(zhì)量達(dá)標(biāo)且符合國(guó)內(nèi)安全,、有效及質(zhì)量可控的標(biāo)準(zhǔn),。進(jìn)口商必須遵循相關(guān)法規(guī)流程,辦理各類許可與備案手續(xù),。例如,,對(duì)于按藥品管理的生物試劑,,要嚴(yán)格執(zhí)行藥品進(jìn)口管理辦法;屬醫(yī)療器械范疇的生物試劑,,則需依照醫(yī)療器械進(jìn)口政策執(zhí)行,,從產(chǎn)品準(zhǔn)入到流通各環(huán)節(jié)均有明確規(guī)范,以保障國(guó)內(nèi)市場(chǎng)生物試劑的安全有序供應(yīng),。上海抗體試劑進(jìn)出口許可證辦理出口生物試劑時(shí),,運(yùn)輸包裝需符合國(guó)際生物運(yùn)輸?shù)陌踩珮?biāo)準(zhǔn),。
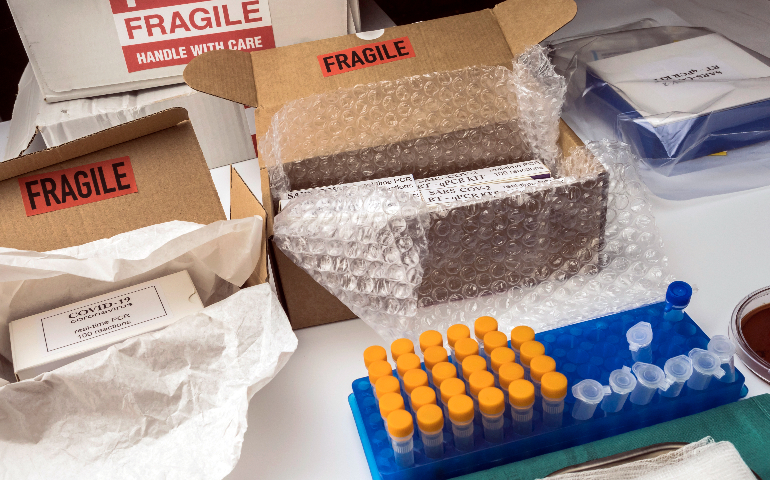
進(jìn)出口生物試劑均需通過(guò)嚴(yán)格檢驗(yàn)檢疫。出口時(shí),,企業(yè)要主動(dòng)向海關(guān)與檢驗(yàn)檢疫部門申報(bào),,提供詳細(xì)產(chǎn)品信息、生產(chǎn)批次,、質(zhì)量檢測(cè)報(bào)告等資料,。檢驗(yàn)檢疫部門會(huì)根據(jù)試劑特性與進(jìn)口國(guó)要求,進(jìn)行質(zhì)量抽檢,,檢測(cè)純度,、活性、微生物限度等指標(biāo),,對(duì)于一些傳染病診斷試劑,,對(duì)其微生物限度和特異性要求極高。對(duì)可能攜帶病原體,、有害生物因子的試劑進(jìn)行生物安全檢測(cè),,防止有害生物跨境傳播。進(jìn)口生物試劑時(shí),,同樣要接受我國(guó)檢驗(yàn)檢疫部門查驗(yàn),,企業(yè)需配合做好貨物查驗(yàn)、抽樣檢測(cè)等工作,,對(duì)于冷鏈生物試劑,,還要滿足冷鏈貨物檢驗(yàn)檢疫要求,如落實(shí)核酸檢測(cè),、消毒等防控措施,,確保產(chǎn)品符合國(guó)內(nèi)外檢驗(yàn)檢疫標(biāo)準(zhǔn),保障公共衛(wèi)生安全與市場(chǎng)秩序,,為國(guó)內(nèi)科研,、醫(yī)療等領(lǐng)域提供安全可靠的生物試劑。
生物試劑進(jìn)口前,,產(chǎn)品注冊(cè)是關(guān)鍵環(huán)節(jié),。按藥品管理的生物試劑,,需向 NMPA 提交注冊(cè)申請(qǐng),包含產(chǎn)品研發(fā),、生產(chǎn)工藝,、質(zhì)量標(biāo)準(zhǔn)、臨床試驗(yàn)數(shù)據(jù)(如適用)等詳細(xì)資料,,經(jīng)嚴(yán)格審評(píng)審批流程,,審評(píng)中心評(píng)估產(chǎn)品安全性、有效性和質(zhì)量可控性,,審批通過(guò)后方可獲得進(jìn)口藥品注冊(cè)證,。醫(yī)療器械類生物試劑注冊(cè)同樣嚴(yán)謹(jǐn),依據(jù)風(fēng)險(xiǎn)程度分為不同類別管理,。低風(fēng)險(xiǎn)產(chǎn)品實(shí)行備案管理,,進(jìn)口商向所在地設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門提交備案資料;中,、高風(fēng)險(xiǎn)產(chǎn)品則需向 NMPA 申請(qǐng)注冊(cè),,經(jīng)技術(shù)審評(píng)、臨床試驗(yàn)核查(若有)等程序,,取得醫(yī)療器械注冊(cè)證后才能進(jìn)口,,確保進(jìn)口產(chǎn)品符合國(guó)內(nèi)質(zhì)量與安全要求。對(duì)于生物試劑出口,,要提前掌握進(jìn)口國(guó)的檢疫程序,。

若生物試劑含有毒有害物質(zhì),進(jìn)口前需通過(guò)環(huán)保部門的審批,。企業(yè)要向當(dāng)?shù)厣鷳B(tài)環(huán)境部門提交進(jìn)口申請(qǐng),,說(shuō)明生物試劑所含毒有害物質(zhì)的種類、含量,、用途,、處理方式等信息。生態(tài)環(huán)境部門會(huì)依據(jù)相關(guān)環(huán)保法規(guī),,評(píng)估試劑進(jìn)口對(duì)環(huán)境的潛在影響,,如是否符合污染物排放標(biāo)準(zhǔn)、是否具備妥善的廢棄物處理方案等,。只有在獲得環(huán)保部門許可后,,企業(yè)才能進(jìn)行后續(xù)進(jìn)口操作,確保生物試劑進(jìn)口不會(huì)對(duì)國(guó)內(nèi)生態(tài)環(huán)境造成危害,。涉及人類遺傳資源的生物試劑進(jìn)口,,受《中華人民共和國(guó)人類遺傳資源管理?xiàng)l例》約束。進(jìn)口單位必須向有關(guān)部門科學(xué)技術(shù)行政部門申請(qǐng)人類遺傳資源許可。申請(qǐng)過(guò)程中,,需詳細(xì)說(shuō)明試劑來(lái)源,、涉及的人類遺傳資源種類與數(shù)量、使用目的,、合作方信息等,。有關(guān)部門科學(xué)技術(shù)行政部門會(huì)對(duì)申請(qǐng)進(jìn)行嚴(yán)格審查,考量是否符合保護(hù)我國(guó)人類遺傳資源安全,、促進(jìn)合理利用等要求,,獲批后企業(yè)方可進(jìn)口,避免我國(guó)人類遺傳資源非法外流及不當(dāng)使用,。出口生物試劑要注意進(jìn)口國(guó)對(duì)不同品牌的市場(chǎng)準(zhǔn)入情況,。昆山核酸試劑進(jìn)出口清關(guān)手續(xù)
生物試劑進(jìn)口申報(bào)需準(zhǔn)確填報(bào)產(chǎn)品的原產(chǎn)國(guó)信息。杭州酶類試劑進(jìn)出口審批備案代辦
我國(guó)生物試劑出口政策旨在規(guī)范出口秩序,,推動(dòng)產(chǎn)業(yè)健康發(fā)展,同時(shí)保障生物安全與公共衛(wèi)生安全,。國(guó)家相關(guān)部門,,如商務(wù)部、國(guó)家藥品監(jiān)督管理局等協(xié)同監(jiān)管,,依據(jù)一系列法規(guī)構(gòu)建政策體系,。出口生物試劑必須確保質(zhì)量符合國(guó)際標(biāo)準(zhǔn)以及目標(biāo)市場(chǎng)要求,生產(chǎn)過(guò)程遵循良好生產(chǎn)規(guī)范(GMP)等準(zhǔn)則,。企業(yè)需在合法合規(guī)前提下開(kāi)展出口業(yè)務(wù),,履行各類申報(bào)與備案手續(xù)。對(duì)于不同類型生物試劑,,依據(jù)其風(fēng)險(xiǎn)程度與應(yīng)用領(lǐng)域,,制定差異化出口管理措施,既助力不錯(cuò)生物試劑拓展國(guó)際市場(chǎng),,又嚴(yán)格把控可能存在的風(fēng)險(xiǎn),,維護(hù)國(guó)家利益與國(guó)際聲譽(yù)。杭州酶類試劑進(jìn)出口審批備案代辦
- 寧波生物試劑進(jìn)出口前置審批代辦 2025-06-11
- 上海海關(guān)監(jiān)管倉(cāng)儲(chǔ)配送 2025-06-11
- 上海自動(dòng)化倉(cāng)儲(chǔ)有哪些 2025-06-11
- 上海港出口監(jiān)管倉(cāng)儲(chǔ)配送 2025-06-11
- 上海出口監(jiān)管倉(cāng)庫(kù)怎么樣 2025-06-11
- 上海港貨物監(jiān)管倉(cāng)庫(kù)放行時(shí)間 2025-06-11
- 上海保稅區(qū)倉(cāng)庫(kù) 2025-06-11
- 保稅監(jiān)管倉(cāng)庫(kù)哪家好 2025-06-11
- 蘇州特殊物品進(jìn)口許可證辦理 2025-06-11
- 上海港海關(guān)監(jiān)管倉(cāng)儲(chǔ)如何收費(fèi) 2025-06-11
- 南通重型貨架價(jià)格 2025-06-11
- 南京國(guó)內(nèi)專線運(yùn)輸價(jià)格多少 2025-06-11
- 浦東新區(qū)配送服務(wù)行業(yè) 2025-06-11
- 宜興附近道路貨物運(yùn)輸大概價(jià)格 2025-06-11
- 甘肅輸送帶滾筒批發(fā) 2025-06-11
- 歐洲到中國(guó)網(wǎng)購(gòu)空運(yùn)時(shí)效 2025-06-11
- 河北產(chǎn)品出口木箱 2025-06-11
- 天津服裝出口托盤 2025-06-11
- 嘉興立體倉(cāng)儲(chǔ)貨架批發(fā) 2025-06-11
- 浙江塑料手推車什么價(jià)格 2025-06-11