無錫酶類試劑進出口審批流程
在生物試劑進出口領域,,法規(guī)政策起著關鍵的規(guī)范作用。不同國家和地區(qū)對生物試劑的進出口有著嚴格規(guī)定,。例如,,我國依據(jù)《中華人民共和國藥品管理法》《醫(yī)療器械監(jiān)督管理條例》等法規(guī),對作為藥品或醫(yī)療器械管理的生物試劑,,要求企業(yè)具備相應資質,,如藥品經(jīng)營許可證、醫(yī)療器械經(jīng)營備案憑證等,。對于一些特殊生物試劑,,可能還涉及《生物制品批簽發(fā)管理辦法》,需取得批簽發(fā)證明方可進口,。美國食品藥品監(jiān)督管理局(FDA)對進口生物試劑也有詳細準則,,從產(chǎn)品注冊、標簽要求到生產(chǎn)質量管理規(guī)范(GMP)符合性審查等,,確保產(chǎn)品安全有效,。企業(yè)在開展進出口業(yè)務前,務必深入研究目標市場法規(guī),,完成各類許可申請與注冊流程,,避免因違規(guī)遭受處罰,影響業(yè)務開展,。出口生物試劑要注意進口國對其有效期的相關限定規(guī)則,。無錫酶類試劑進出口審批流程

生物試劑進出口企業(yè),資質許可至關重要,。進口企業(yè)需先完成對外貿(mào)易經(jīng)營者備案登記,,獲取合法進出口權。若涉及藥品類生物試劑進口,,必須持有藥品經(jīng)營許可證,,此證對倉儲條件、人員資質等有嚴格要求,,如倉庫要分區(qū)域存儲,且質量管理人員需有藥學專業(yè)背景及從業(yè)經(jīng)驗,。對于醫(yī)療器械類生物試劑,,依據(jù)風險等級,低風險的需辦理醫(yī)療器械經(jīng)營備案憑證,中高風險的則要取得醫(yī)療器械經(jīng)營許可證 ,。出口企業(yè)也得完成對外貿(mào)易經(jīng)營者備案,,生產(chǎn)企業(yè)還需持有相應的藥品生產(chǎn)許可證或醫(yī)療器械生產(chǎn)許可證。此外,,針對高風險生物制品或涉及兩用物項的生物試劑,,進出口都要提前申請?zhí)貏e許可,像生物制品批簽發(fā)證明,、兩用物項和技術進出口許可證等,。企業(yè)務必嚴格按規(guī)定流程申請,杜絕無證經(jīng)營,,否則將面臨嚴重法律處罰,,阻礙業(yè)務開展。無錫酶類試劑進出口審批流程生物試劑進口申報文件必須真實有效,,避免清關受阻,。

全球生物試劑市場規(guī)模龐大且持續(xù)增長。在科研領域,,生命科學研究不斷深入,,對生物試劑需求日益旺盛,推動市場擴張,。歐美地區(qū)科研投入高,,是主要消費市場,擁有眾多有名生物試劑企業(yè),,技術先進,、產(chǎn)品線豐富。亞洲地區(qū),,隨著經(jīng)濟發(fā)展和科研實力提升,,特別是中國、印度等國家,,市場潛力巨大,,需求增速高于全球平均水平。從產(chǎn)品類型看,,分子生物學試劑,、免疫診斷試劑等細分市場占據(jù)較大份額。在進出口貿(mào)易中,,發(fā)達國家多為不錯生物試劑出口國,,憑借技術優(yōu)勢把控重心產(chǎn)品供應;發(fā)展中國家在中低端產(chǎn)品領域有一定競爭力,,同時也是不錯試劑重要進口市場,。企業(yè)需結合市場趨勢,,找準定位,制定合適進出口策略,,開拓市場份額,。
進出口生物試劑均需通過嚴格檢驗檢疫。出口時,,企業(yè)要主動向海關與檢驗檢疫部門申報,,提供詳細產(chǎn)品信息、生產(chǎn)批次,、質量檢測報告等資料,。檢驗檢疫部門會根據(jù)試劑特性與進口國要求,進行質量抽檢,,檢測純度,、活性、微生物限度等指標,,對于一些傳染病診斷試劑,,對其微生物限度和特異性要求極高。對可能攜帶病原體,、有害生物因子的試劑進行生物安全檢測,,防止有害生物跨境傳播。進口生物試劑時,,同樣要接受我國檢驗檢疫部門查驗,,企業(yè)需配合做好貨物查驗、抽樣檢測等工作,,對于冷鏈生物試劑,,還要滿足冷鏈貨物檢驗檢疫要求,如落實核酸檢測,、消毒等防控措施,,確保產(chǎn)品符合國內外檢驗檢疫標準,保障公共衛(wèi)生安全與市場秩序,,為國內科研,、醫(yī)療等領域提供安全可靠的生物試劑。出口生物試劑要重視進口國對產(chǎn)品追溯體系的要求,。
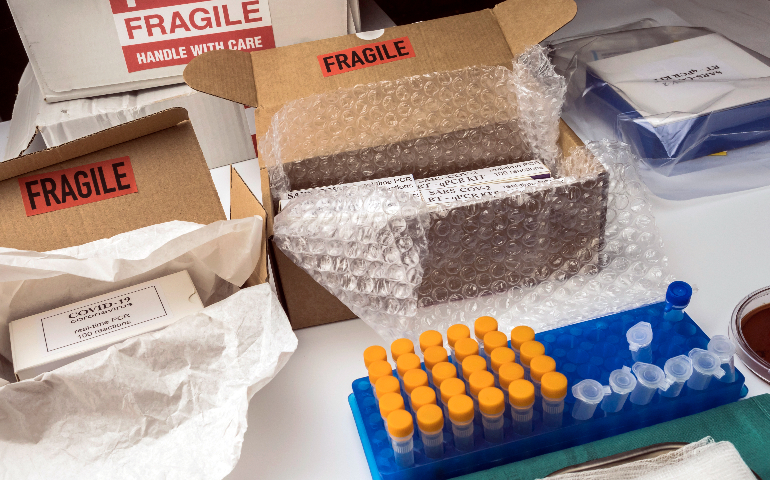
包裝和標識在生物試劑進出口中舉足輕重,。包裝材料要堅固耐用,且能適配試劑特性,。強酸強堿類試劑要用耐腐蝕性包裝,,對光照敏感試劑需采用遮光包裝,同時包裝要具備良好密封性,,防止泄漏,。標識方面,,必須清晰標注產(chǎn)品名稱,、成分,、規(guī)格、生產(chǎn)企業(yè),、生產(chǎn)日期,、有效期、儲存條件,、使用說明等信息,。語言要符合目標市場要求,一般需用英語,,在部分非英語國家,,可能還得翻譯成當?shù)卣Z言。對于危險生物試劑,,要依據(jù)國際標準張貼危險貨物標識,,如國際《關于危險貨物運輸?shù)慕ㄗh書》中的相關標準,以此保障運輸,、儲存和使用過程中的安全,,避免因包裝標識不當引發(fā)安全事故或通關受阻。出口生物試劑要重視進口國對產(chǎn)品質量認證的要求,。昆山抗體試劑進出口審批代辦
生物試劑進口申報需準確填報產(chǎn)品的原產(chǎn)國信息,。無錫酶類試劑進出口審批流程
我國生物試劑出口政策旨在規(guī)范出口秩序,推動產(chǎn)業(yè)健康發(fā)展,,同時保障生物安全與公共衛(wèi)生安全,。國家相關部門,如商務部,、國家藥品監(jiān)督管理局等協(xié)同監(jiān)管,,依據(jù)一系列法規(guī)構建政策體系。出口生物試劑必須確保質量符合國際標準以及目標市場要求,,生產(chǎn)過程遵循良好生產(chǎn)規(guī)范(GMP)等準則,。企業(yè)需在合法合規(guī)前提下開展出口業(yè)務,履行各類申報與備案手續(xù),。對于不同類型生物試劑,,依據(jù)其風險程度與應用領域,制定差異化出口管理措施,,既助力不錯生物試劑拓展國際市場,,又嚴格把控可能存在的風險,維護國家利益與國際聲譽,。無錫酶類試劑進出口審批流程
- 上海港自動化倉儲怎么樣 2025-06-09
- 寧波生物試劑進出口前置審批備案 2025-06-09
- 保稅監(jiān)管倉儲申請條件 2025-06-09
- 上海港食品藥品監(jiān)管倉庫有哪些 2025-06-09
- 上海危險品監(jiān)管倉儲要求 2025-06-09
- 上海倉庫放行時間 2025-06-09
- 無錫酶類試劑進出口審批流程 2025-06-09
- 上海海關監(jiān)管倉儲哪家靠譜 2025-06-09
- 蘇州酶類試劑進出口運輸 2025-06-08
- 酶類試劑進出口許可證辦理 2025-06-08
- 深圳云倉代發(fā)無憂 2025-06-10
- 湖南定制立體倉庫批發(fā)價 2025-06-10
- 奉賢區(qū)運輸倉儲公司報價 2025-06-10
- 國際配送服務一般多少錢 2025-06-10
- 徐匯區(qū)大型倉庫報價 2025-06-10
- 倉儲外包服務哪家服務好 2025-06-10
- 威海有哪些危險品運輸車隊車隊 2025-06-10
- 便宜的物流配送發(fā)展對比 2025-06-10
- 四川靜音塑料手推車推薦廠家 2025-06-10
- 湖北倉儲服務客服電話 2025-06-10