-
 廣東吸收塔電極設(shè)備
廣東吸收塔電極設(shè)備電解槽中的電極同樣至關(guān)重要,,它是電流進入或離開電解液的導(dǎo)體,,電解過程就在電極相界面上發(fā)生氧化還原反應(yīng)。電極分為陰極和陽極,,與電源正極相連的是陽極,,陽極上發(fā)生氧化反應(yīng);與電源負極相連的是陰極,,陰極上發(fā)生還原反應(yīng),。電解材料種類繁多,碳電極是常用材料之一,,因其具有良好的導(dǎo)電性和化學(xué)穩(wěn)定性,,在許多電解過程中表現(xiàn)出色。此外,,鈦等金屬也可作為電極材料,,尤其在一些對電極耐腐蝕性要求較高的特殊電解應(yīng)用中。在電鍍工藝里,,含有鍍層金屬的金屬常作為陽極,,待鍍制品則作為陰極。光電協(xié)同催化使有機物降解速率提升3倍,。廣東吸收塔電極設(shè)備隨著全球?qū)η鍧嵞茉吹男枨蟛粩嘣黾?,電解水制氫作為一種高效、環(huán)保的制氫方式,,受到關(guān)注,。鈦電...
-
 寧夏電極除硬
寧夏電極除硬微電極的工作面積十分微小,其電極面積大小界限雖不十分嚴格,,但這種小尺寸特性賦予了它獨特優(yōu)勢,。一方面,微電極實現(xiàn)了電極的微型化,,在一些對空間要求極高的微納器件或生物體內(nèi)檢測場景中,,能輕松適配。另一方面,,在電化學(xué)分析中,盡管整個電極并非微型化,,但其極小的工作面積可使電極反應(yīng)時發(fā)生明顯的極化作用,。通過微電極指示出的擴散電流與離子濃度存在線性關(guān)系,借此可精確測知溶液中離子的濃度,,在痕量分析等方面表現(xiàn)出色,。電化學(xué)pH調(diào)控精度達±0.3。寧夏電極除硬熱分解法是制備鈦電極常用的方法之一,。該方法首先將含有活性金屬元素的有機鹽或無機鹽溶液涂覆在鈦基體表面,,然后通過高溫?zé)崽幚硎雇繉影l(fā)生分解反應(yīng),形成具有電催化活性...
-
 海水淡化電極除硬
海水淡化電極除硬難溶鹽電極的氧化還原對中有一個組分為難溶鹽或其他固相,,它包含三個物相,、兩個界面,,且在每一相界面上存在著單一的快速遷越過程,甘汞電極(Hg|Hg?Cl?|Cl?)便是典型,。在甘汞電極中,,甘汞與電解液的溶解平衡受電液中濃度較高的 Cl?所控制,Cl?在 Hg?Cl?| 電液界面上的交換速率很快,,這使得甘汞電極的電極電勢極為穩(wěn)定,,因此它成為常用的參比電極之一。部分書刊將這類電極稱為第二類電極,,在電化學(xué)測量等領(lǐng)域有著不可或缺的地位,。電化學(xué)氧化分解PFOA脫氟率>99%。海水淡化電極除硬 電極作為電化學(xué)反應(yīng)的關(guān)鍵部件,,其工作原理基于與電解質(zhì)或反應(yīng)物間的相互作用,。在電池里,電極通過與電解質(zhì)中的離子進行氧...
-
 湖南海水淡化電極需求
湖南海水淡化電極需求氯離子對電極氧化的影響主要體現(xiàn)在:①競爭吸附破壞鈍化膜(Cl?與O2?競爭金屬表面位點),;②形成可溶性金屬氯配合物(如FeCl?),;③形成酸性微環(huán)境。當Cl?濃度超過300mg/L時,,316不銹鋼的點蝕電位會從+0.35V驟降至+0.05V,。值得注意的是,Cl?/SO?2?比值超過0.5時,,協(xié)同效應(yīng)會明顯加劇腐蝕,,這解釋了為何海水冷卻系統(tǒng)需要特種合金電極。 硫酸鹽還原菌(SRB)等微生物可通過獨特機制加速電極氧化:①分泌酸性代謝物,;②形成差異通氣電池,;③直接參與電子轉(zhuǎn)移。研究發(fā)現(xiàn)SRB存在時,,碳鋼腐蝕速率可達無菌環(huán)境的5-10倍,。更復(fù)雜的是,微生物生物膜會導(dǎo)致電極表面pH梯度變化,,某...
-
 寧夏循壞水電極需求
寧夏循壞水電極需求電極可分為陽極和陰極,,在電化學(xué)電池中,發(fā)生氧化作用的電極是陽極,,該過程中物質(zhì)失去電子,;發(fā)生還原作用的電極是陰極,物質(zhì)在這一過程中得到電子,。例如在常見的鋰離子電池中,,充電時,鋰離子從正極脫出,通過電解質(zhì)嵌入負極,,此時正極是陽極,,負極是陰極;放電時則相反,,鋰離子從負極脫出,,通過電解質(zhì)嵌入正極,電極的陰陽極角色發(fā)生轉(zhuǎn)換,,正是這種陰陽極之間的氧化還原反應(yīng),,實現(xiàn)了電池的充放電過程。 參比電極在電化學(xué)測量中扮演著不可或缺的角色,,它為其他電極提供穩(wěn)定的參考電位,。在復(fù)雜的電化學(xué)體系中,由于各種因素的影響,,單個電極的電位難以直接準確測量,,而參比電極的電位具有高度的穩(wěn)定性和重現(xiàn)性。將參比電極與待測電極組...
-
 河南工業(yè)電極除硬系統(tǒng)
河南工業(yè)電極除硬系統(tǒng)難溶鹽電極的氧化還原對中有一個組分為難溶鹽或其他固相,,它包含三個物相,、兩個界面,且在每一相界面上存在著單一的快速遷越過程,,甘汞電極(Hg|Hg?Cl?|Cl?)便是典型,。在甘汞電極中,甘汞與電解液的溶解平衡受電液中濃度較高的 Cl?所控制,,Cl?在 Hg?Cl?| 電液界面上的交換速率很快,,這使得甘汞電極的電極電勢極為穩(wěn)定,因此它成為常用的參比電極之一,。部分書刊將這類電極稱為第二類電極,,在電化學(xué)測量等領(lǐng)域有著不可或缺的地位。電化學(xué)阻垢劑再生復(fù)用次數(shù)達10次,。河南工業(yè)電極除硬系統(tǒng)電極氧化反應(yīng)遵循電化學(xué)熱力學(xué)原理,,可用能斯特方程描述電極電位與反應(yīng)物濃度的關(guān)系。以鐵電極為例,,其氧化反應(yīng)Fe→Fe2?...
-
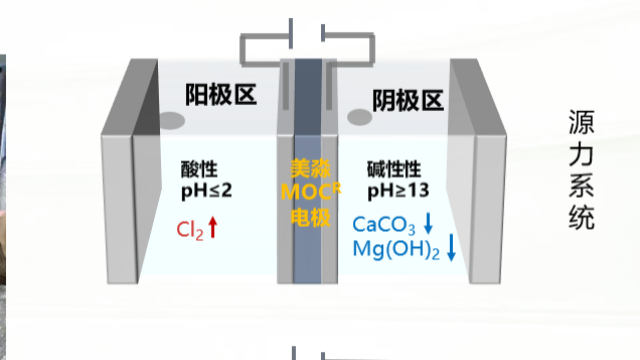 河南源力循壞水電極設(shè)施
河南源力循壞水電極設(shè)施電極材料的選擇至關(guān)重要,,它直接影響電極的性能和應(yīng)用范圍。金屬材料如銅,、銀、鉑等,,因具有良好的導(dǎo)電性,,在許多電極應(yīng)用中備受青睞。銅的導(dǎo)電性優(yōu)良且成本相對較低,常用于一般的導(dǎo)電電極,;銀的導(dǎo)電率更高,,在一些對導(dǎo)電性要求極高的電子器件電極中有所應(yīng)用;鉑則因其出色的化學(xué)穩(wěn)定性和生物相容性,,常用于醫(yī)療設(shè)備電極以及一些高精度的電化學(xué)檢測電極,。此外,碳材料如石墨,,也因其獨特的導(dǎo)電性能和化學(xué)穩(wěn)定性,,在電池電極等領(lǐng)域使用。電化學(xué)方法使色度從500倍降至10倍以下,。河南源力循壞水電極設(shè)施難溶鹽電極的氧化還原對中有一個組分為難溶鹽或其他固相,,它包含三個物相、兩個界面,,且在每一相界面上存在著單一的快速遷越過程,,甘汞電極...
-
 新疆電極設(shè)施
新疆電極設(shè)施電極作為電化學(xué)反應(yīng)的關(guān)鍵部件,其工作原理基于與電解質(zhì)或反應(yīng)物間的相互作用,。在電池里,,電極通過與電解質(zhì)中的離子進行氧化還原反應(yīng),實現(xiàn)電子的釋放與接收,,進而產(chǎn)生電能,。像是常見的干電池,鋅皮作為負極,,發(fā)生氧化反應(yīng)釋放電子,;碳棒為正極,接受電子促使還原反應(yīng)發(fā)生,。在電化學(xué)過程中,,電極表面的活性位點能催化反應(yīng),極大地提升反應(yīng)速率,,降低反應(yīng)所需的活化能,,使原本難以發(fā)生的反應(yīng)得以順利進行。 電極的命名方式豐富多樣,。部分依據(jù)電極的金屬部分來命名,,如銅電極、銀電極,,簡單直觀地表明了電極的主要材質(zhì),。有些根據(jù)電極活性的氧化還原對中的特征物質(zhì)命名,像甘汞電極,,因其氧化還原對涉及甘汞這一特征物質(zhì),。還有根據(jù)電極金...