���K�Ї�eCTD�ļҺ� ��Ϣ���] �x���Ƽ�����
�l(f��)؛���c���㽭ʡ������
�l(f��)���r�g��2025-04-21
�l(f��)؛���c���㽭ʡ������
�l(f��)���r�g��2025-04-21
eCTD 4.0�汾���^���c������FDA��2023�ꆢ��eCTD 4.0���gԇ�c,��2024��9����ʽ������Ո,��Ӌ��2029�����ȫ�^��,��4.0�汾����HL7 RPS�˜����XML,��֧���p��ͨ�źͿ���Ո�ļ�����,������ͬһStudy ID����IND��NDA����ģ�K1��У�a��MD5������SHA-256,�������ļ���index.xml�Ğ�submissionunit.xml,������̖ȡ��ǰ���㣨�硰1�����ǡ�0001��������I(y��)��ͬ����ܛ��ϵ�y(t��ng)���m���ܘ�,��DMF�cIND��������Ҫ��ᘌ�Type II��ԭ��ˎ����Type IV���o�ϣ�DMF,��eCTDģ�K3��Ԕ���������a��ˇ����(w��n)���Ԕ�(sh��)��(j��),�����������C����COA��,��FDAҪ��DMF������ָ���������ȴ����ˣ��_����ͨЧ��,����LOA���ڙ����������_���÷���,��IND��ȫ�Ԉ�棨��SUSAR����ͨ�^eCTDģ�K5.3.5�ύ��15������,����Ƕ��CIOMS��MedWatch����,��2024��ָ�Ϗ��{���R����(sh��)��(j��)������SAS XPORT��ʽ�ύ,�����ļ����^4GB���ֲ��f��Ҏ(gu��)�t,������INDע��������P���g֧��,�����K�Ї�eCTD�ļҺ�
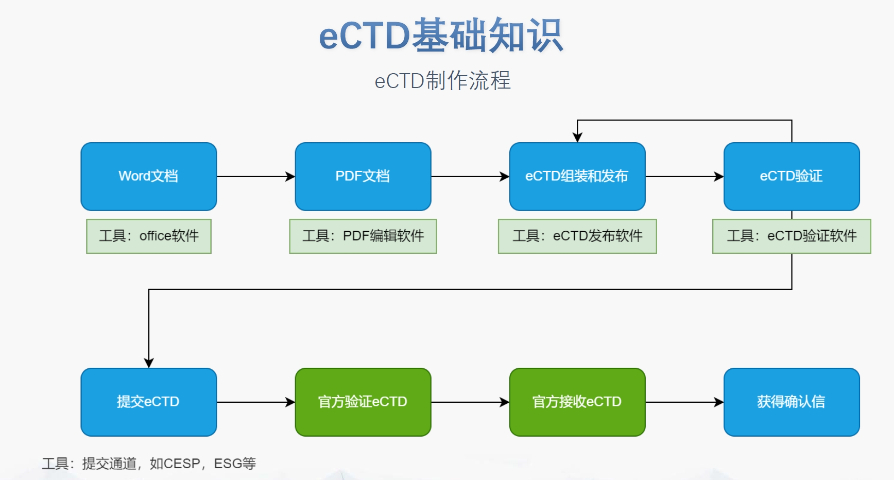
�˴�eCTD��ʩ�����ĔU���������Ӱ푡���ʩ�����ĔU��������ṩ�˸����x��,���e���ڮaƷ����NDA��ANDռ���ஔ?sh��)���r��,�������ϵ�y(t��ng)�������������죬���������eCTD�U���ַe�O�B(t��i)��,����Ը��Lԇ��׃,���M���^���п����������g��Ҏ(gu��)�ϵĆ��}������I(y��)�J��ͨ�^���෴�����cCDE��ͨ,���܉����������w���Ч�ʺ��|��,�����⣬����߀���R������ɻ���Ҏ(gu��)��Ϣ����ϵ�y(t��ng)������(zh��n),���e�Ǯ���Ҫ�w�Ƶ�ϵ�y(t��ng)�r,������M�猢�aƷ�w�Ƶ�eCTD���oՓ��ϵ�y(t��ng)�w��߀�Ǻ��m(x��)���������ڹ�����������형�,�� �S��eCTD��ʩ�����ĔU��,�������̌����и���ĘI(y��)�ՙC����Ȼ��,���Ї�ˎƷע���wϵ�������p��,�������MeCTD��ʩ�^���п������R���N���}�����ڃ�,����С��I(y��)�������R�Y������,����Ҫ���]�Ƿ�Ͷ���Y��ُ�I��eCTDϵ�y(t��ng)�����L�ځ���,����I(y��)���Pע������ν���һ�����Ƶ��ęn�����wϵ,������������f�����@��Ҫ��I(y��)��ǰ��Ͷ������r�g�;����M�����̃�(y��u)�����ˆT��Ӗ,��ɽ�|�x���Ƽ�eCTD����ESG����ύͨ����Ո���P���g֧��,��

GDUFA III����c�M�÷�� 2022�����GDUFA III���M�÷֞�ANDA��Ո�M��DMF�J�C�M,���Ŀ�M���Oʩ�M���,����ʩ������2027�ꡣ2025ؔ��ANDA�M�Ýq���s22�f��Ԫ,���^2024�������_27.5%,����ӳ���u�ɱ������� ANDA��Ո�MҎ(gu��)�t �M�������ύ�r�U�{,������Ո���ܿ���߀75%,�����ύҕ����Ո�����ٴ��U�M���P(li��n)API�Ĺ��S��(sh��)��Ӱ푿��M��,������ijANDA����3��API���漰6�ҹ��S,����֧��6��DMF�M�á� DMF�M�ÙC�� II�ԭ��ˎDMF��������ǰ�U�M,��һ����֧���s5.3�f��Ԫ��2025ؔ�꣩��δ�U�MDMF��������֧��ANDA,����t�|�l(f��)�ˌ�,�� �Ŀ�M�ּ����� ����(j��)��I(y��)�@��ANDA��(sh��)���֞����,��С������,��2025�������I(y��)���M�s34�f��Ԫ�����ٹ�˾ANDA��(sh��)���ϲ�Ӌ��,���U�M؟�ο���ĸ��˾����һ���ٹ�˾�Г�,��
�W��eCTD��ʩ��(j��ng)��S�����Ї��ɽ��b�Լ����M��,���Ї����ܕ���(j��ng)�v����I(y��)��ԸeCTD�ύ������eCTD�ύ���^��,���Ҍ��o�SICH������������CMC�Y����������,��ȫ������eCTD 4.0�^��,���Ї�Ҳ�����⣬���S�ձ�,���W��,�������ȏ��ƌ�ʩ�������M�� �Ї���������ȫ�����C��,��eCTD��ʩ�������Ї���I(y��)��������,�����g�M��������eCTD��ʩ����I(y��)�������Pע���g�ӑB(t��i),���{����(zh��n)��,���S�����Ⱦ͘I(y��)�����������I(y��)�����������ӣ��˽�eCTD�ȇ��H�˜ʌ��ɞ��I(y��)�l(f��)չ����Ҫ������,�� �Ї����MeCTD���挦��ɫ���},�������к���Ո�Y��ƥ�䣬����I(y��)�c�O(ji��n)�ܙC����ͬ��Q,�,�����Ҫ�����P�I���Ї����ƶ��m�χ����Ҫ��,���ڴ�δ���(zh��)��ָ�ϼȾ���ɫ���c���H��܉,����eCTD��ʩ�ṩ֧�֡����ô�INDע��������P���g֧��,��
2020�걩�l(f��)��,��F(xi��n)DA�Mһ���Ƅ���ӻ��M��,���������S�h����Ӻ��º��R�r�Ō����ָ�ʽҪ����C�˜ʣ���PDF�汾,������朽���Ч�ԣ���δ����,���@һ�r�ڵČ��`��eCTD�ھo�������е��`�����ṩ�˰�����Ҳ�@��������Σ�C�������ߵărֵ,�� �M��������δ����eCTD V4.0,�����似�g���������_��֧���t(y��)����е�ͱ���Ʒ���������(sh��)��(j��)�ɏ�����,����(y��u)�����uϵ�y(t��ng)�c�˹����ܵļ���,�����⣬�^(q��)�K朼��g����Ӻ��º͔�(sh��)��(j��)��Դ�еđ���̽��,�����ܳɞ���һ�A�����������c���ô�eCTD������P���g֧��,�����KˎƷע��eCTD��ʽ
�Ĵ�����eCTDע��������P���g֧�֡����K�Ї�eCTD�ļҺ�
PDF������ ����̎���c��ʽ�ޏ� ֧��PDF�ϲ�,�����,����ȡ��桢���D���Ȳ���,���������ޏ����wδǶ��,����朽��e�`�Ȇ��}���_���ļ�����ˎƷע�Է�Ҏ(gu��)Ҫ��,�� ���ܕ����c��朽ӹ��� �ṩ��������/����,����朽��Ԅ����ɣ�֧���P�I��������λ朽ӣ����}ע��朽���קʽ���ȹ���,���������s�ęn�Č����OӋ,�� �ęn�D�Q�cOCR�R�e ֧��Word�DPDF���Ԅ����ɕ�����Ƕ�����w��,���Լ�PDF�cWord,��Excel�ȸ�ʽ���D������OCR�������ڒ���������R�e,�� ��Ҏ(gu��)����C �Ԅ���CPDF����沼��,��퓴a�B�m(x��)�ԡ��հ��,��Ŀ䛌Ӽ��Ȍ���,������λ���w�e�`λ�ã��p���˹��z��ɱ�,�� ��ȫ�c�f(xi��)������ ֧���ęn����,����(sh��)�ֺ������ƶ�ͬ�������O�乲�����M����I(y��)���ļ���ȫ��������,�����K�Ї�eCTD�ļҺ�