寧波抗體試劑進出口前置審批代辦
生物試劑進出口業(yè)務與可持續(xù)發(fā)展緊密相連,。從生產角度,,企業(yè)越來越注重綠色生產工藝,采用環(huán)保型原材料和節(jié)能生產設備,,減少生產過程中的能源消耗和污染物排放,。例如,一些生物試劑生產企業(yè)優(yōu)化發(fā)酵工藝,,提高原料利用率,,降低廢水廢氣產生量。在包裝方面,,推行可回收,、可降解包裝材料,減少塑料等一次性包裝的使用,,像紙質包裝逐漸替代部分塑料包裝用于生物試劑運輸,。在運輸環(huán)節(jié),運輸企業(yè)采用優(yōu)化的物流路線規(guī)劃,,提高運輸效率,,降低能源消耗。同時,,國際上也在推動生物試劑進出口行業(yè)的可持續(xù)發(fā)展標準制定,,促使企業(yè)在追求經濟效益的同時,積極履行社會責任,,實現行業(yè)的長期可持續(xù)發(fā)展,。出口生物試劑前,要明確進口國對包裝標識的具體規(guī)范要求,。寧波抗體試劑進出口前置審批代辦
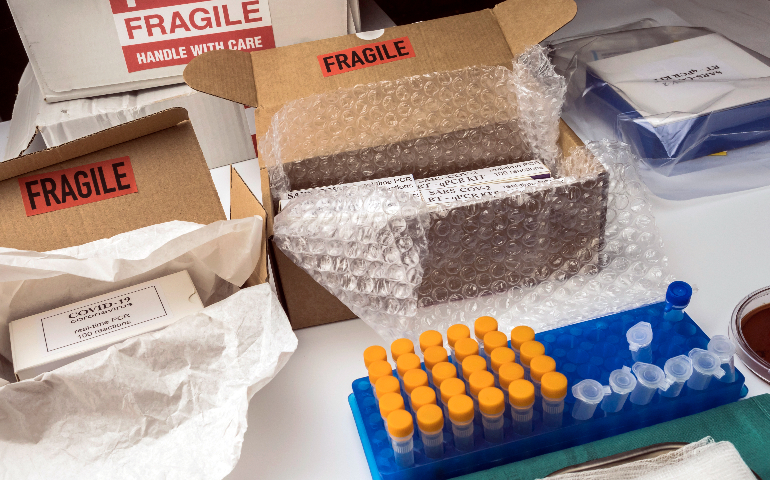
我國生物試劑出口政策旨在規(guī)范出口秩序,,推動產業(yè)健康發(fā)展,同時保障生物安全與公共衛(wèi)生安全,。國家相關部門,,如商務部、國家藥品監(jiān)督管理局等協(xié)同監(jiān)管,,依據一系列法規(guī)構建政策體系,。出口生物試劑必須確保質量符合國際標準以及目標市場要求,生產過程遵循良好生產規(guī)范(GMP)等準則,。企業(yè)需在合法合規(guī)前提下開展出口業(yè)務,,履行各類申報與備案手續(xù)。對于不同類型生物試劑,,依據其風險程度與應用領域,,制定差異化出口管理措施,既助力不錯生物試劑拓展國際市場,,又嚴格把控可能存在的風險,,維護國家利益與國際聲譽,。上海酶類試劑進出口審批流程生物試劑進口申報需提供產品的第三方檢測報告。

生物試劑運輸有其特殊要求,。多數生物試劑對溫度敏感,,如酶類試劑在高溫下易失活,需冷鏈運輸,。常見冷鏈運輸方式包括干冰冷藏、低溫冷藏車等,。干冰運輸適用于少量試劑,,能維持低溫環(huán)境,但要注意干冰揮發(fā)帶來的安全問題,,確保包裝有良好通風,。低溫冷藏車可用于大量試劑長距離運輸,車內配備制冷設備,,能精細控制溫度在規(guī)定范圍,。對于一些易氧化或需惰性氣體保護的生物試劑,包裝時會充入氮氣等惰性氣體,。同時,,運輸過程中的震動也可能影響試劑穩(wěn)定性,需采用減震材料妥善包裝,。運輸企業(yè)必須具備專業(yè)資質,,其人員經過培訓,熟悉生物試劑特性與運輸應急處理,,保障試劑在運輸環(huán)節(jié)質量不受損,。
醫(yī)療器械類生物試劑進口前,需依據風險等級完成注冊審批,。低風險的一類醫(yī)療器械生物試劑,,進口商需向所在地設區(qū)的市級藥品監(jiān)督管理部門辦理備案手續(xù),提交產品風險分析資料,、產品技術要求,、產品檢驗報告等備案資料。對于中風險的二類和高風險的三類醫(yī)療器械生物試劑,,則要向國家藥品監(jiān)督管理局申請注冊,。企業(yè)需準備詳細的產品研發(fā)、生產制造,、臨床評價等資料,,經技術審評、臨床試驗核查(如適用)等嚴格程序,,獲得醫(yī)療器械注冊證后,,方可開展進口業(yè)務,,保障進口醫(yī)療器械類生物試劑的安全性與有效性。出口生物試劑需對產品的儲存條件進行明確標注,。

進口生物試劑的企業(yè)必須具備特定資質,。首先,企業(yè)需完成對外貿易經營者備案登記,,獲得合法進出口經營權,。若進口藥品類生物試劑,應持有有效的藥品經營許可證,,其倉儲,、運輸等設施要符合藥品經營質量管理規(guī)范(GSP),確保試劑儲存與流通環(huán)節(jié)質量可控,。對于醫(yī)療器械類生物試劑進口,,企業(yè)需依據試劑風險等級,完成醫(yī)療器械經營備案或取得醫(yī)療器械經營許可證,。企業(yè)還應配備專業(yè)人員,,包括熟悉生物試劑法規(guī)、質量控制及進口業(yè)務流程的管理人員與技術人員,,以滿足進口業(yè)務的專業(yè)操作與合規(guī)管理需求,。生物試劑進口申報需準確填報產品的原產國信息??贵w試劑進出口審批流程
生物試劑進口需關注目的國對生物試劑銷售渠道的限制,。寧波抗體試劑進出口前置審批代辦
生物試劑出口前,產品認證是重要環(huán)節(jié),。對于出口到歐美等發(fā)達國家市場的生物試劑,,通常需獲得當地認可的認證。如出口歐盟,,多數生物試劑要依據歐盟相關指令與協(xié)調標準,,完成 CE 認證,涵蓋產品安全性,、健康影響,、環(huán)保等多方面評估,通過認證機構檢測與審核后獲得認證證書,。出口美國則需關注美國食品藥品監(jiān)督管理局(FDA)要求,,按照不同產品類別完成相應注冊、列名等程序,,如醫(yī)療器械類生物試劑可能需進行 510 (k) 申請或上市前批準(PMA)等,。通過這些認證流程,使出口生物試劑符合目標市場準入標準,。寧波抗體試劑進出口前置審批代辦
- 上海貨物監(jiān)管倉儲派送 2025-06-02
- 上海保稅區(qū)倉庫代發(fā) 2025-06-02
- 上海港出口監(jiān)管倉儲派送 2025-06-02
- 上海港保稅監(jiān)管倉儲哪家專業(yè) 2025-06-02
- 貨物監(jiān)管倉儲費用標準 2025-06-02
- 無錫生物試劑出口監(jiān)管法規(guī) 2025-06-02
- 上海出口監(jiān)管倉儲哪家專業(yè) 2025-06-02
- 保稅監(jiān)管倉庫在哪里 2025-06-02
- 寧波抗體試劑進出口免費咨詢 2025-06-02
- 食品藥品監(jiān)管倉儲流程 2025-06-02
- 河南被動滾筒批發(fā) 2025-06-03
- 崇明區(qū)特色道路貨物運輸業(yè)務供應 2025-06-03
- 黃浦區(qū)多樣國內配送流程 2025-06-03
- 本地化工品運輸服務電話 2025-06-03
- 服裝鞋靴襪FBA補倉供應商 2025-06-03
- 電子產品加拿大卡派聯系方式 2025-06-03
- 湖南全國通精密儀器運輸價格 2025-06-03
- 小件倉庫服務 2025-06-03
- 上海電商倉庫服務 2025-06-02
- 棗莊危險化學品危險品運輸車隊常見問題 2025-06-02