-
航瑞智能助力維尚家具打造自動(dòng)倉(cāng)儲(chǔ)系統(tǒng),,實(shí)現(xiàn)成品物流智能化升級(jí)
-
航瑞智能:準(zhǔn)確把握倉(cāng)儲(chǔ)痛點(diǎn),,打造多樣化智能倉(cāng)儲(chǔ)方案
-
高度集成化自動(dòng)化立體倉(cāng)庫:開啟高效物流新時(shí)代_航瑞智能
-
探秘倉(cāng)儲(chǔ)物流中心:輸送機(jī)與RGV打造高效智能物流體系
-
共享裝備攜手航瑞智能打造砂芯智能倉(cāng)儲(chǔ),,實(shí)現(xiàn)倉(cāng)儲(chǔ)物流智能化升級(jí)
-
桁架機(jī)械手與輸送機(jī):打造高效智能流水線
-
?采用WMS倉(cāng)庫管理系統(tǒng)能夠給企業(yè)帶來哪些好處,?
-
?航瑞智能:精細(xì)把握倉(cāng)儲(chǔ)痛點(diǎn),,打造多樣化智能倉(cāng)儲(chǔ)方案
-
往復(fù)式提升機(jī):垂直輸送系統(tǒng)的智能化解決方案
-
航瑞智能:準(zhǔn)確把握倉(cāng)儲(chǔ)痛點(diǎn),,打造多樣化智能倉(cāng)儲(chǔ)方案
浙江高質(zhì)量藥物安全性評(píng)價(jià)實(shí)驗(yàn)
特殊安全性試驗(yàn)包含:過敏性(局部,、全身和光敏毒性),、溶血性和局部(血管,、皮膚,、黏膜、肌肉等)刺激性等主要與局部,、全身給藥相關(guān)的特殊安全性試驗(yàn),;復(fù)方制劑中多種成分毒性相互影響的試驗(yàn);致突變?cè)囼?yàn),;生殖毒性試驗(yàn),;致*試驗(yàn),;依賴性試驗(yàn)。藥物安全性評(píng)價(jià)主要數(shù)據(jù)指標(biāo)包含以下幾類:比較大耐受劑量(MTD)是指在急性毒性試驗(yàn)中,,受試物不引起受試對(duì)象(實(shí)驗(yàn)動(dòng)物)出現(xiàn)死亡的比較大劑量,。比較大無毒性反應(yīng)劑量(NOAEL),指藥物在一定時(shí)間內(nèi),,按一定方式與機(jī)體接觸,,按一定的檢測(cè)方法或觀察指標(biāo),不能觀察到任何損害作用的比較高劑量,。**小致死劑量(MLD),,引起個(gè)別動(dòng)物死亡的**小劑量。藥物安全性評(píng)價(jià)研究是藥物研發(fā)的基礎(chǔ)性工作,,應(yīng)當(dāng)確保行為規(guī)范,,數(shù)據(jù)真實(shí)、準(zhǔn)確,、完整,。浙江高質(zhì)量藥物安全性評(píng)價(jià)實(shí)驗(yàn)
藥物安全評(píng)價(jià)又稱非臨床藥物安全性評(píng)價(jià),是指通過實(shí)驗(yàn)室研究和動(dòng)物體外系統(tǒng)對(duì)***藥物的安全性,,進(jìn)行評(píng)估,,是新藥品進(jìn)入**終臨床試驗(yàn)和**終的批準(zhǔn)前的必要程序和重要步驟。藥物安全性必須先起草方案和協(xié)議,。這些研究,,如一般急性慢性毒性研究,病理組織學(xué)研究,,生殖毒性試驗(yàn),,遺傳毒性研究,安全藥理學(xué)研究,,調(diào)查研究,,毒性和安全性生物標(biāo)志物的研究。由于在分子生物學(xué)系列的體積非常成功的方法,,包括章節(jié)簡(jiǎn)要介紹各自的學(xué)科,,所需的材料清單,一步一步的,,隨手可重復(fù)的協(xié)議,,并在故障排除和避免已知的陷阱提示。廣西值得信賴藥物安全性評(píng)價(jià)價(jià)格藥物安全性評(píng)價(jià)是新藥研發(fā)的必需組成部分,。

加速引進(jìn)批準(zhǔn)上市新藥重視科學(xué)的管理程序建設(shè),,需要考慮臨床***需求品種,注重科學(xué)選擇品種特性和優(yōu)勢(shì)對(duì)國(guó)內(nèi)患者的新藥的相對(duì)安全,、有效和可及可用的范圍,;注重與藥物有效性和安全性相關(guān)的藥物代謝特異性和種屬遺傳差異性,。需要科學(xué)分析計(jì)劃進(jìn)口品種的臨床前和臨床研究資料、臨床療效的金指標(biāo),?;趪?guó)外上市所處現(xiàn)狀,分析處于IV期臨床的藥物安全性評(píng)價(jià),。對(duì)優(yōu)先審評(píng)、加速批準(zhǔn),、孤兒藥的引進(jìn),,考慮接近監(jiān)管期限批準(zhǔn)和監(jiān)管審查時(shí)間的狀況和安全監(jiān)管的國(guó)內(nèi)銜接。
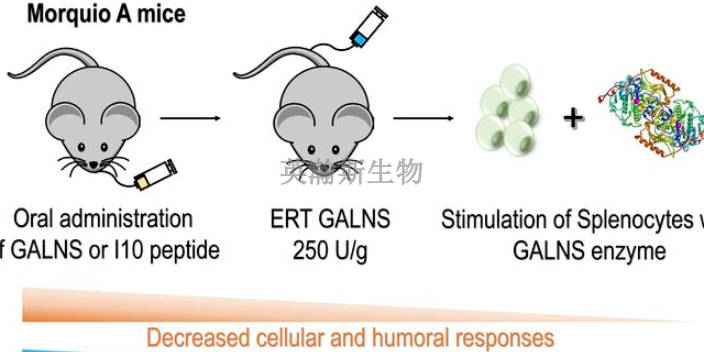
藥物安全性評(píng)價(jià)的重復(fù)給藥毒性試驗(yàn)可以:預(yù)測(cè)受試物可能引起的臨床不良反應(yīng),,包括不良反應(yīng)的性質(zhì),、程度、量效和時(shí)效關(guān)系,、以及可逆性等,;判斷受試物重復(fù)給藥的毒性靶組織或靶組織;如果可能,,確定未觀察到臨床不良反應(yīng)的劑量水平(NoObservedAdverseEffectLevel,,NOAEL);推測(cè)***次臨床試驗(yàn)(FirstinHuman,FIH)的起始劑量,,為后續(xù)臨床試驗(yàn)提供安全劑量范圍,;為臨床不良反應(yīng)監(jiān)測(cè)及防治提供參考。藥物安全性評(píng)價(jià)就找南京英瀚斯生物,。藥物安全性評(píng)價(jià)在哪做比較好,?
疫苗新藥臨床前研究中藥物安全性評(píng)價(jià)的難點(diǎn)在于疫苗本身并不直接發(fā)揮預(yù)防或***作用,而是通過誘導(dǎo)免疫系統(tǒng)產(chǎn)生抗體或活化T細(xì)胞發(fā)揮作用,。在疫苗研發(fā)中需要考慮疫苗可能會(huì)產(chǎn)生的安全問題,。(1)疫苗成分本身作為毒性物質(zhì)對(duì)機(jī)體的直接損傷。(2)疫苗誘導(dǎo)免疫系統(tǒng)引起的與免疫相關(guān)的毒性,。(3)污染物和殘余雜質(zhì)引起的毒性,。疫苗制備的過程中的各個(gè)環(huán)節(jié)具有可能帶入污染物或?qū)е職堄嚯s質(zhì)的存在,控制此類毒性也是質(zhì)量控制研究的主要目的,。(4)若疫苗載體在體內(nèi)變異,,將威脅患者的生命。(5)其它未知的毒***物安全性評(píng)價(jià)中的統(tǒng)計(jì)學(xué)應(yīng)用都有哪些,?廣西值得信賴藥物安全性評(píng)價(jià)價(jià)格
藥物安全性評(píng)價(jià)要求藥物的基本要求,、安全、有效,、質(zhì)量可控 ,。浙江高質(zhì)量藥物安全性評(píng)價(jià)實(shí)驗(yàn)
初步的臨床藥理學(xué)及藥物安全性評(píng)價(jià)試驗(yàn),,為新藥人體試驗(yàn)的起始期,又稱為早期人體試驗(yàn),。I期臨床試驗(yàn)包括耐受性試驗(yàn)和藥代動(dòng)力學(xué)研究,,一般在健康受試者中進(jìn)行。其目的是研究人體對(duì)藥物的耐受程度,,并通過藥物代謝動(dòng)力學(xué)研究,,了解藥物在人體內(nèi)的吸收、分布,、消除的規(guī)律,,為制定給***案提供依據(jù),以便進(jìn)一步進(jìn)行***試驗(yàn),。人體耐受性試驗(yàn)(clinicaltolerancetest)是在經(jīng)過詳細(xì)的動(dòng)物實(shí)驗(yàn)研究的基礎(chǔ)上,,觀察人體對(duì)該藥的耐受程度,找出人體對(duì)新藥的比較大耐受劑量及其產(chǎn)生的不良反應(yīng),,是人體的安全性試驗(yàn),,為確定II期臨床試驗(yàn)用藥劑量提供重要的科學(xué)依據(jù)。浙江高質(zhì)量藥物安全性評(píng)價(jià)實(shí)驗(yàn)
南京英瀚斯生物科技有限公司一直專注于醫(yī)學(xué)實(shí)驗(yàn)外包,、動(dòng)物實(shí)驗(yàn)外包,、細(xì)胞實(shí)驗(yàn)外包、分子實(shí)驗(yàn)檢測(cè),、病理染色檢測(cè),、科研實(shí)驗(yàn)外包、動(dòng)物模型構(gòu)建,、第三方檢測(cè),、病理組織切片、細(xì)胞培養(yǎng),、電生理檢測(cè),、醫(yī)學(xué)研究和試驗(yàn)發(fā)展、生物醫(yī)藥技術(shù)研發(fā),、技術(shù)轉(zhuǎn)讓,、技術(shù)咨詢及技術(shù)服務(wù),是一家醫(yī)藥健康的企業(yè),,擁有自己**的技術(shù)體系,。一批專業(yè)的技術(shù)團(tuán)隊(duì),是實(shí)現(xiàn)企業(yè)戰(zhàn)略目標(biāo)的基礎(chǔ),,是企業(yè)持續(xù)發(fā)展的動(dòng)力,。公司以誠(chéng)信為本,業(yè)務(wù)領(lǐng)域涵蓋實(shí)驗(yàn)外包,動(dòng)物模型構(gòu)建,,細(xì)胞分子實(shí)驗(yàn),,病理檢測(cè),我們本著對(duì)客戶負(fù)責(zé),,對(duì)員工負(fù)責(zé),,更是對(duì)公司發(fā)展負(fù)責(zé)的態(tài)度,爭(zhēng)取做到讓每位客戶滿意,。公司深耕實(shí)驗(yàn)外包,,動(dòng)物模型構(gòu)建,細(xì)胞分子實(shí)驗(yàn),,病理檢測(cè),,正積蓄著更大的能量,向更廣闊的空間,、更寬泛的領(lǐng)域拓展。
- 湖北靠譜的HE染色報(bào)告 2025-06-03
- 云南HE染色價(jià)格 2025-06-03
- 河南肺纖維化模型有哪些 2025-06-03
- 內(nèi)蒙古專業(yè)的HE染色服務(wù) 2025-06-03
- 甘肅病理HE染色報(bào)告 2025-06-03
- 湖南結(jié)果客觀的HE染色檢測(cè) 2025-06-03
- 江蘇質(zhì)量好的HE染色 2025-06-02
- 四川病理HE染色價(jià)格 2025-06-02
- 吉林病理HE染色服務(wù) 2025-06-02
- 浙江質(zhì)量好的HE染色多少錢 2025-06-02
- 采購(gòu)卵磷脂使用注意事項(xiàng) 2025-06-04
- 國(guó)產(chǎn)小型集中供水系統(tǒng) 2025-06-04
- 新疆卵磷脂 2025-06-04
- 西北國(guó)產(chǎn)牙托粉多少錢 2025-06-04
- 吉林國(guó)產(chǎn)分析試劑 2025-06-04
- 黑龍江干細(xì)胞外泌體 2025-06-04
- 甘肅假肢哪家好 2025-06-04
- 廣東包含什么ELISA試劑盒進(jìn)貨價(jià) 2025-06-04
- 普通牛血清白蛋白(BSA)ELISA試劑盒 2025-06-04
- 廣州吖啶酸丙磺酸鹽 2025-06-04