安徽化學(xué)藥品eCTD供應(yīng)商
ANDA遞交: 按照ICH M4的CTD格式整理資料,并以eCTD格式遞交,; 通過(guò)ESG通道遞交資料; 收到CDER的letter,,說(shuō)明資料已經(jīng)進(jìn)入FDA數(shù)據(jù)庫(kù),; 付GDUFA費(fèi),,在資料遞交后的10日內(nèi)到賬; ANDA接收: 繳費(fèi)后,,F(xiàn)DA初步審查資料的完整性,,并會(huì)在60天給答復(fù)。 第一種情況是ANDA無(wú)缺陷,,F(xiàn)DA給申請(qǐng)人發(fā)受理信(Acceptance Letter),; 第二種情況是ANDA包含少于10個(gè)小缺陷,F(xiàn)DA將會(huì)通過(guò)電話(huà),、傳真,、電子郵件等方式通知發(fā)布IR (信息請(qǐng)求函),,讓申請(qǐng)人在7個(gè)日歷日內(nèi)改正,,若未按時(shí)補(bǔ)充所有需要的資料,F(xiàn)DA將拒收該ANDA,; 第三種情況是ANDA包含1個(gè)或者多個(gè)重大缺陷,,或10個(gè)以上的小缺陷,F(xiàn)DA將拒收該ANDA,; 注:如果這邊被拒收,,只退75%的費(fèi)用。加拿大eCTD申報(bào)軟件相關(guān)技術(shù)支持,。安徽化學(xué)藥品eCTD供應(yīng)商
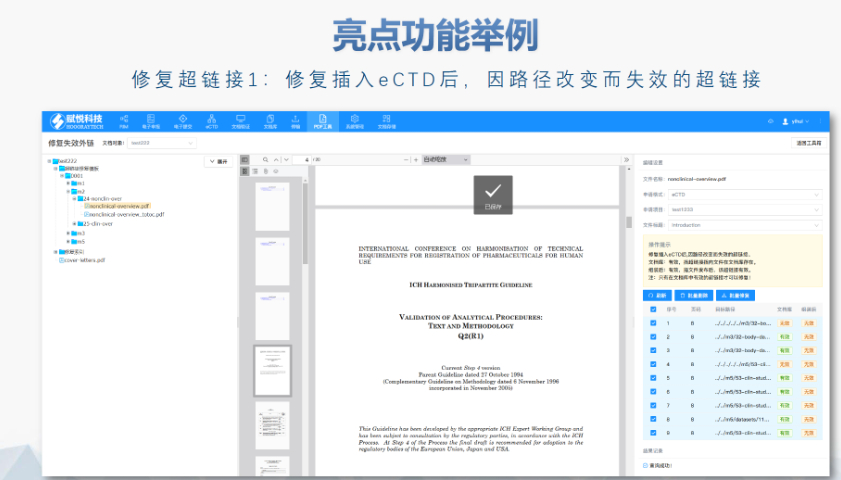
eCTD在歐盟藥品監(jiān)管中的歷史背景:歐盟eCTD(電子通用技術(shù)文檔)的發(fā)展始于對(duì)臨床試驗(yàn)和藥品審評(píng)流程標(biāo)準(zhǔn)化的需求,。2001年,歐盟引入《臨床試驗(yàn)指令》(CTD)作為統(tǒng)一的法律框架,,但其分散的成員國(guó)申報(bào)機(jī)制導(dǎo)致效率低下,。2014年,歐盟通過(guò)《臨床試驗(yàn)法規(guī)》(CTR, Regulation EU No. 536/2014),,要求通過(guò)CTIS平臺(tái)(臨床試驗(yàn)信息系統(tǒng))集中提交臨床試驗(yàn)申請(qǐng)(CTA),,并逐步推動(dòng)eCTD作為電子化申報(bào)的工具。這一旨在解決傳統(tǒng)CTD模式下審評(píng)周期長(zhǎng),、多國(guó)協(xié)調(diào)成本高的問(wèn)題,,為eCTD的實(shí)施奠定了基礎(chǔ)。合肥生物制品eCTD使用美國(guó)eCTD注冊(cè)咨詢(xún)相關(guān)技術(shù)支持,。
生命周期管理與變更遞交 eCTD支持全生命周期管理,,申請(qǐng)人需通過(guò)序列更(Sequence)反映藥品變更信息。例如CEP證書(shū)的更需提交“變更說(shuō)明表”,,對(duì)比已批準(zhǔn)和擬修改內(nèi)容,,并附修訂版技術(shù)文檔,。重大變更(如生產(chǎn)工藝調(diào)整)可能觸發(fā)GMP現(xiàn)場(chǎng)檢查,EDQM將根據(jù)風(fēng)險(xiǎn)評(píng)估決定是否啟動(dòng)核查,。 電子簽名與法律效力 歐盟接受符合《電子簽名法》的數(shù)字簽名,,手寫(xiě)簽名的掃描件需嵌入PDF并加密保護(hù)。模塊1的申請(qǐng)表和承諾書(shū)必須包含有效簽名,,且XML文件需通過(guò)MD5校驗(yàn)確保完整性,。若使用第三方簽署工具,需提前向監(jiān)管機(jī)構(gòu)報(bào)備并獲取技術(shù)認(rèn)可,。 中小企業(yè)支持與資源獲取 EMA和EDQM為中小企業(yè)提供eCTD實(shí)施指南,、驗(yàn)證工具及培訓(xùn)研討會(huì)。例如,,EDQM官網(wǎng)發(fā)布CEP遞交模板和案例庫(kù),,EMA則定期更Q&A文檔以解答常見(jiàn)問(wèn)題。此外,,歐盟設(shè)立專(zhuān)項(xiàng)基金,,資助中小企業(yè)完成eCTD轉(zhuǎn)換和系統(tǒng)部署。
中國(guó)將進(jìn)一步與國(guó)際接軌,,推進(jìn)eCTD等標(biāo)準(zhǔn)應(yīng)用,,提高藥品注冊(cè)效率和質(zhì)量。AI技術(shù)可能在藥品注冊(cè)領(lǐng)域廣泛應(yīng)用,,如輔助審評(píng)人員工作,。未來(lái)藥品注冊(cè)資料將更注重結(jié)構(gòu)化數(shù)據(jù),有助于監(jiān)管機(jī)構(gòu)高效獲取和利用數(shù)據(jù),。 eCTD等數(shù)字化工具將推動(dòng)藥品監(jiān)管向智慧監(jiān)管和全生命周期監(jiān)管發(fā)展,,提高監(jiān)管效率和質(zhì)量。區(qū)塊鏈技術(shù)具有應(yīng)用前景,,可構(gòu)建全球統(tǒng)一的藥品申報(bào)數(shù)據(jù)平臺(tái),。數(shù)據(jù)化時(shí)代,藥品注冊(cè)領(lǐng)域?qū)⒏⒅財(cái)?shù)據(jù)收集,、分析和利用,,為監(jiān)管機(jī)構(gòu)和企業(yè)提供決策支持。 總而言之,,展望未來(lái),,隨著eCTD在藥品注冊(cè)領(lǐng)域的廣泛應(yīng)用和不斷發(fā)展,中國(guó)將逐步建立起與國(guó)際接軌的藥品注冊(cè)體系,。這將有助于提高中國(guó)藥品注冊(cè)的效率和質(zhì)量,,推動(dòng)中國(guó)藥品走向世界舞臺(tái)。同時(shí),企業(yè)也需要密切關(guān)注技術(shù)發(fā)展動(dòng)態(tài)和監(jiān)管政策變化,,及時(shí)調(diào)整自身戰(zhàn)略和規(guī)劃,,以適應(yīng)未來(lái)的市場(chǎng)競(jìng)爭(zhēng)和監(jiān)管要求。中NDA注冊(cè)申報(bào)相關(guān)技術(shù)支持,。
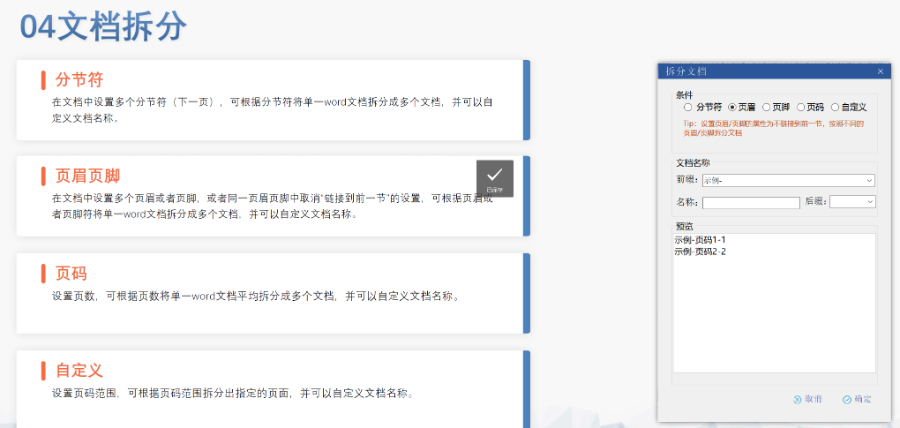
技術(shù)壁壘與興市場(chǎng)挑戰(zhàn) 非洲和東南亞國(guó)家逐步采納eCTD,,但其IT基礎(chǔ)設(shè)施薄弱導(dǎo)致實(shí)施進(jìn)度滯后。歐盟通過(guò)“eCTD全球化倡議”提供技術(shù)援助,,幫助興市場(chǎng)建立驗(yàn)證體系和培訓(xùn)中心,。跨國(guó)藥企需針對(duì)不同區(qū)域定制遞交策略,,例如在模塊1附加本地穩(wěn)定性數(shù)據(jù),。 監(jiān)管科學(xué)與創(chuàng)激勵(lì) eCTD支持真實(shí)世界證據(jù)(RWE)和適應(yīng)性臨床試驗(yàn)設(shè)計(jì)的整合,加速創(chuàng)藥上市,。EMA的PRIME計(jì)劃為突破性療法提供eCTD快速通道,,允許分階段提交模塊數(shù)據(jù)。孤兒藥和兒科藥的eCTD序列可享受費(fèi)用減免和優(yōu)先審評(píng),。 供應(yīng)鏈安全與審計(jì)追蹤 eCTD的XML主干文件記錄所有提交版本,,支持供應(yīng)鏈問(wèn)題的追溯分析。原料藥CEP持有者需及時(shí)更變更信息,,確保下游制劑廠(chǎng)商獲取數(shù)據(jù),。區(qū)塊鏈技術(shù)試點(diǎn)用于追蹤eCTD數(shù)據(jù)流,防止篡改和未授權(quán)訪(fǎng)問(wèn),。 文化差異與實(shí)施障礙 部分南歐國(guó)家偏好傳統(tǒng)紙質(zhì)流程,導(dǎo)致eCTD推廣阻力較大,。EMA通過(guò)多語(yǔ)種培訓(xùn)材料和區(qū)域協(xié)調(diào)員制度促進(jìn)文化適應(yīng),。行業(yè)需調(diào)整管理思維,將eCTD從“合規(guī)負(fù)擔(dān)”轉(zhuǎn)化為“競(jìng)爭(zhēng)優(yōu)勢(shì)”,。瑞士ANDA注冊(cè)申報(bào)相關(guān)技術(shù)支持,。楊浦區(qū)國(guó)內(nèi)注冊(cè)eCTD銷(xiāo)售電話(huà)
加拿大IND注冊(cè)申報(bào)相關(guān)技術(shù)支持。安徽化學(xué)藥品eCTD供應(yīng)商
2020年暴發(fā)后,,F(xiàn)DA進(jìn)一步推動(dòng)電子化進(jìn)程,,例如允許遠(yuǎn)程電子簽章和臨時(shí)放寬部分格式要求,但驗(yàn)證標(biāo)準(zhǔn)(如PDF版本,、書(shū)簽鏈接有效性)并未降低,。這一時(shí)期的實(shí)踐為eCTD在緊急審批中的靈活性提供了案例,也凸顯了其作為危機(jī)應(yīng)對(duì)工具的價(jià)值,。 盡管美國(guó)尚未部署eCTD V4.0,,但其技術(shù)方向已明確:支持醫(yī)療器械和保健品申報(bào)、增強(qiáng)數(shù)據(jù)可復(fù)用性,、優(yōu)化審評(píng)系統(tǒng)與人工智能的集成,。此外,,區(qū)塊鏈技術(shù)在電子簽章和數(shù)據(jù)溯源中的應(yīng)用探索,可能成為下一階段升級(jí)的重點(diǎn)安徽化學(xué)藥品eCTD供應(yīng)商
賦悅科技(杭州)有限責(zé)任公司是一家有著先進(jìn)的發(fā)展理念,,先進(jìn)的管理經(jīng)驗(yàn),,在發(fā)展過(guò)程中不斷完善自己,要求自己,,不斷創(chuàng)新,,時(shí)刻準(zhǔn)備著迎接更多挑戰(zhàn)的活力公司,在浙江省等地區(qū)的數(shù)碼,、電腦中匯聚了大量的人脈以及**,,在業(yè)界也收獲了很多良好的評(píng)價(jià),這些都源自于自身的努力和大家共同進(jìn)步的結(jié)果,,這些評(píng)價(jià)對(duì)我們而言是比較好的前進(jìn)動(dòng)力,,也促使我們?cè)谝院蟮牡缆飞媳3謯^發(fā)圖強(qiáng)、一往無(wú)前的進(jìn)取創(chuàng)新精神,,努力把公司發(fā)展戰(zhàn)略推向一個(gè)新高度,,在全體員工共同努力之下,全力拼搏將共同賦悅科技供應(yīng)和您一起攜手走向更好的未來(lái),,創(chuàng)造更有價(jià)值的產(chǎn)品,,我們將以更好的狀態(tài),更認(rèn)真的態(tài)度,,更飽滿(mǎn)的精力去創(chuàng)造,,去拼搏,去努力,,讓我們一起更好更快的成長(zhǎng),!
- 高新區(qū)中國(guó)eCTD歡迎選購(gòu) 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊(cè)系統(tǒng) 2025-05-14
- 上海化學(xué)藥品eCTD格式 2025-05-09
- 南京電子申報(bào)eCTD哪個(gè)品牌好 2025-05-09
- 太倉(cāng)NDAeCTD服務(wù)價(jià)格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 云浮檔案數(shù)字化加工系統(tǒng)哪家好 2025-06-06
- 銷(xiāo)售管理系統(tǒng)T+軟件服務(wù)財(cái)務(wù)業(yè)務(wù)一體化 2025-06-06
- 遵義高效轉(zhuǎn)化率提升價(jià)格 2025-06-06
- solarflare X2522 或X2541PLUS超頻服務(wù)器哪里好 2025-06-06
- 黑龍江高性能手持平板哪家強(qiáng) 2025-06-06
- 數(shù)智家庭農(nóng)場(chǎng)erp哪個(gè)好 2025-06-06
- 重慶碳鋼矩陣柔性?shī)A具廠(chǎng)家直銷(xiāo) 2025-06-06
- 蘇州購(gòu)買(mǎi)智慧醫(yī)療設(shè)計(jì) 2025-06-06
- 長(zhǎng)沙藍(lán)牙超高頻讀寫(xiě)器工作原理 2025-06-06
- 天津移動(dòng)硬盤(pán)價(jià)格 2025-06-06