無錫電子申報(bào)eCTD服務(wù)放心可靠
技術(shù)壁壘與興市場挑戰(zhàn) 非洲和東南亞國家逐步采納eCTD,,但其IT基礎(chǔ)設(shè)施薄弱導(dǎo)致實(shí)施進(jìn)度滯后,。歐盟通過“eCTD全球化倡議”提供技術(shù)援助,,幫助興市場建立驗(yàn)證體系和培訓(xùn)中心,??鐕幤笮栳槍Σ煌瑓^(qū)域定制遞交策略,,例如在模塊1附加本地穩(wěn)定性數(shù)據(jù),。 監(jiān)管科學(xué)與創(chuàng)激勵 eCTD支持真實(shí)世界證據(jù)(RWE)和適應(yīng)性臨床試驗(yàn)設(shè)計(jì)的整合,,加速創(chuàng)藥上市,。EMA的PRIME計(jì)劃為突破性療法提供eCTD快速通道,,允許分階段提交模塊數(shù)據(jù)。孤兒藥和兒科藥的eCTD序列可享受費(fèi)用減免和優(yōu)先審評,。 供應(yīng)鏈安全與審計(jì)追蹤 eCTD的XML主干文件記錄所有提交版本,,支持供應(yīng)鏈問題的追溯分析。原料藥CEP持有者需及時更變更信息,,確保下游制劑廠商獲取數(shù)據(jù),。區(qū)塊鏈技術(shù)試點(diǎn)用于追蹤eCTD數(shù)據(jù)流,防止篡改和未授權(quán)訪問,。 文化差異與實(shí)施障礙 部分南歐國家偏好傳統(tǒng)紙質(zhì)流程,,導(dǎo)致eCTD推廣阻力較大。EMA通過多語種培訓(xùn)材料和區(qū)域協(xié)調(diào)員制度促進(jìn)文化適應(yīng),。行業(yè)需調(diào)整管理思維,,將eCTD從“合規(guī)負(fù)擔(dān)”轉(zhuǎn)化為“競爭優(yōu)勢”。澳大利亞eCTD注冊外包相關(guān)技術(shù)支持,。無錫電子申報(bào)eCTD服務(wù)放心可靠
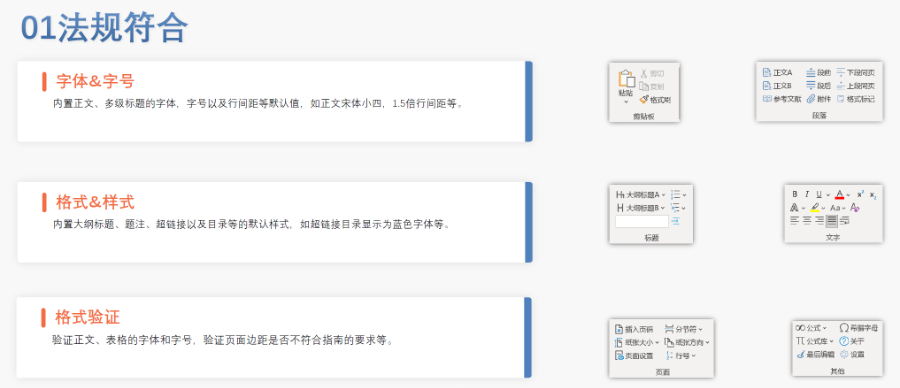
eCTD文件制作需遵循嚴(yán)格的法規(guī)要求和標(biāo)準(zhǔn)化流程,,以下是關(guān)鍵要點(diǎn)整理:eCTD采用模塊化結(jié)構(gòu),包含模塊1(行政信息)至模塊5(臨床報(bào)告),,需按ICH和監(jiān)機(jī)構(gòu)要求構(gòu)建目錄樹,。顆粒度選擇:文件提交層級需在***申報(bào)時確定并沿用,例如原料和制劑的章節(jié)(如,、)需按比較低顆粒度拆分,,輔料單獨(dú)成章。PDF需添加書簽(導(dǎo)航目錄)和超鏈接(跨網(wǎng)頁跳轉(zhuǎn)),,超過5頁的文件必須包含目錄(TOC/LOT/LOF),。技術(shù)參數(shù):初始視圖需設(shè)置默認(rèn)縮放級別和頁面布局,書簽展開層級不超過三級,,單文件大小需符合申報(bào)系統(tǒng)限制,。驗(yàn)證工具:使用軟件(如BXeCTD)自動生成書簽和超鏈接,并通過序列校驗(yàn)和PDF校驗(yàn)功能確保合規(guī)性。 浙江電子申報(bào)eCTD哪家好美國eCTD注冊外包相關(guān)技術(shù)支持,。

區(qū)域化差異與多國協(xié)作挑戰(zhàn) 歐盟eCTD需兼容成員國特定要求,,例如模塊一的行政信息需符合各國語言和法規(guī)差異?;フJ(rèn)程序(MRP)中,,參考成員國(RMS)的評估報(bào)告需被其他成員國認(rèn)可,若出現(xiàn)分歧需由CMDh協(xié)調(diào)或提交EMA仲裁,。這種多層級審評機(jī)制要求申請人在文件準(zhǔn)備階段即考慮區(qū)域兼容性,,避免后續(xù)流程延誤,。 eCTD4.0的探索與未來方向 ICH于2015年發(fā)布的eCTD4.0版本旨在簡化目錄結(jié)構(gòu),、支持多產(chǎn)品類型(如醫(yī)療器械)申報(bào),并增強(qiáng)生命周期管理功能,。歐盟計(jì)劃通過2024年試點(diǎn)逐步過渡至4.0,,其扁平化文件組織方式有望減少重復(fù)提交并提升審評效率。然而,,實(shí)施需解決現(xiàn)有系統(tǒng)兼容性及行業(yè)適應(yīng)性問題,。
美國eCTD驗(yàn)證采用三級分類:“錯誤”(必須修正)、“警告”(建議修正),、“提示信息”(參考),。例如,PDF文件版本不符或加密保護(hù)屬于“錯誤”,,而書簽路徑非相對性則可能列為“警告”,。驗(yàn)證失敗將直接導(dǎo)致退審,企業(yè)需通過LORENZ Validator等工具預(yù)檢,,確保提交前合規(guī),。 ?技術(shù)驗(yàn)證點(diǎn) 驗(yàn)證涵蓋XML結(jié)構(gòu)合規(guī)性、文件命名規(guī)則,、生命周期管理(如序列號連續(xù)性)及PDF屬性(如字體嵌入,、可搜索性)。臨床試驗(yàn)數(shù)據(jù)需額外滿足CDISC標(biāo)準(zhǔn),,包括SDTM和ADaM數(shù)據(jù)集的結(jié)構(gòu)驗(yàn)證歐盟CESP提交通道相關(guān)技術(shù)支持,。
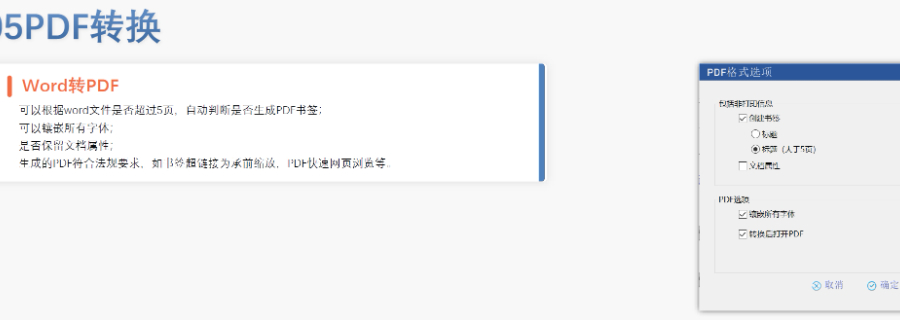
歐洲藥品管理局:集中審評程序由歐洲藥品管理局(European Medicines Agency, EMA)負(fù)責(zé)協(xié)調(diào)。 人用藥品委員會:人用藥品委員會(Committee for Medicinal Products for Human Use, CHMP)負(fù)責(zé)提供科學(xué)意見,。 歐盟委員會:CHMP的意見隨后被提交給歐盟委員會(European Commission, EC),,由歐盟委員會做出是否授權(quán)的終決定。這個決定在整個歐盟都是具有法律約束力的,。 審批過程: 申請人向EMA提交申請,,包括eCTD(電子通用技術(shù)文檔)格式的藥品注冊文檔。 EMA的CHMP分配一個科學(xué)評估團(tuán)隊(duì)(Rapporteur和Co-Rapporteur),負(fù)責(zé)初步評估,。 CHMP基于評估團(tuán)隊(duì)的報(bào)告提供科學(xué)意見,。 歐盟委員會根據(jù)CHMP的意見做出終決定,批準(zhǔn)或拒絕藥品上市,。 授權(quán)范圍 如果藥品獲得批準(zhǔn),,將獲得在整個歐盟、冰島,、列支敦士登和挪威有效的上市許可(Central Marketing Authorisation, CMA),。瑞士eCTD申報(bào)軟件相關(guān)技術(shù)支持。吳江區(qū)藥品注冊eCTD便宜
美國eCTD申報(bào)軟件相關(guān)技術(shù)支持,。無錫電子申報(bào)eCTD服務(wù)放心可靠
爭議解決與法律救濟(jì) 若申請人對審評結(jié)果有異議,,可向EMA的CHMP申請重審查,或在歐盟法院提起行政訴訟,。eCTD的完整提交記錄可作為法律證據(jù),,證明申請人已履行合規(guī)義務(wù)。EDQM設(shè)立仲裁委員會,,處理CEP程序中的技術(shù)爭議,。 行業(yè)趨勢與競爭格局 全球eCTD服務(wù)市場年增長率達(dá)12%,歐盟占據(jù)35%份額,,主要服務(wù)商包括PharmaLex,、Certara等。頭部藥企通過自建IT團(tuán)隊(duì)降低成本,,而中小型企業(yè)依賴外包以專注研發(fā),。人工智能(AI)在文件自動生成和審評意見預(yù)測中的應(yīng)用逐漸增多。 患者參與與透明度提升 EMA通過公開eCTD摘要(如模塊2.5臨床概要)增強(qiáng)審評透明度,,患者組織可提交意見影響審評決策,。部分成員國要求模塊1包含患者語言版本說明書,以提升用藥依從性,。未來,,eCTD4.0或支持直接鏈接患者反饋平臺,實(shí)現(xiàn)全生命周期互動,。無錫電子申報(bào)eCTD服務(wù)放心可靠
賦悅科技(杭州)有限責(zé)任公司是一家有著雄厚實(shí)力背景,、信譽(yù)可靠、勵精圖治,、展望未來,、有夢想有目標(biāo),有組織有體系的公司,,堅(jiān)持于帶領(lǐng)員工在未來的道路上大放光明,,攜手共畫藍(lán)圖,,在浙江省等地區(qū)的數(shù)碼、電腦行業(yè)中積累了大批忠誠的客戶粉絲源,,也收獲了良好的用戶口碑,,為公司的發(fā)展奠定的良好的行業(yè)基礎(chǔ),也希望未來公司能成為*****,,努力為行業(yè)領(lǐng)域的發(fā)展奉獻(xiàn)出自己的一份力量,,我們相信精益求精的工作態(tài)度和不斷的完善創(chuàng)新理念以及自強(qiáng)不息,斗志昂揚(yáng)的的企業(yè)精神將**賦悅科技供應(yīng)和您一起攜手步入輝煌,,共創(chuàng)佳績,,一直以來,公司貫徹執(zhí)行科學(xué)管理,、創(chuàng)新發(fā)展,、誠實(shí)守信的方針,員工精誠努力,,協(xié)同奮取,,以品質(zhì),、服務(wù)來贏得市場,,我們一直在路上!
- 高新區(qū)中國eCTD歡迎選購 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊系統(tǒng) 2025-05-14
- 上?;瘜W(xué)藥品eCTD格式 2025-05-09
- 南京電子申報(bào)eCTD哪個品牌好 2025-05-09
- 太倉NDAeCTD服務(wù)價(jià)格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 云浮檔案數(shù)字化加工系統(tǒng)哪家好 2025-06-06
- 銷售管理系統(tǒng)T+軟件服務(wù)財(cái)務(wù)業(yè)務(wù)一體化 2025-06-06
- 遵義高效轉(zhuǎn)化率提升價(jià)格 2025-06-06
- solarflare X2522 或X2541PLUS超頻服務(wù)器哪里好 2025-06-06
- 黑龍江高性能手持平板哪家強(qiáng) 2025-06-06
- 數(shù)智家庭農(nóng)場erp哪個好 2025-06-06
- 重慶碳鋼矩陣柔性夾具廠家直銷 2025-06-06
- 蘇州購買智慧醫(yī)療設(shè)計(jì) 2025-06-06
- 長沙藍(lán)牙超高頻讀寫器工作原理 2025-06-06
- 天津移動硬盤價(jià)格 2025-06-06