寧波電子申報eCTD格式
ANDA一般不需要提供臨床前(動物)和臨床(人體)數(shù)據(jù)來證明其安全性和有效性(即免毒理和臨床),作為替代,申請人必須合理證明其產(chǎn)品與原研藥相比是生物等效的,。 按照《聯(lián)邦食品,、藥品和化妝品法》第 505(j)章要求,擬向FDA遞交申請ANDA的藥品需符合以下條件: 仿制藥必須依照FDA《經(jīng)過醫(yī)療等同性評價批準的藥品》(俗稱"橙皮書")上所列,,由FDA選定的RLD/RS進行對照仿制; 活性成份,、劑型、規(guī)格,、給藥途徑,、適應癥,要與RLD相同,; 仿制藥必須證明與RLD在生物效果上等同,,即具有生物等效性; 必須按照美國聯(lián)邦管理法21 CFR遵行藥品生產(chǎn)管理規(guī)范控制生產(chǎn)過程,; 無論中國還是美國,,要求仿制藥的質量必須等同或者是高于參比制劑的,這是獲批的基本要點,; 注意:如果原研藥未被列為RLD,,申請人可以提出公民,向FDA申請,。中IND注冊申報相關技術支持,。寧波電子申報eCTD格式

電子簽章與傳輸安全 文件需經(jīng)AES-256加密后刻錄至不可擦寫光盤,并附MD5校驗碼,。光盤損壞或病毒污染將觸發(fā)重遞交流程,,原載體按銷毀程序處理。 ?審評與核查協(xié)同 自2018年起,,F(xiàn)DA要求提交兩套光盤分別用于審評和現(xiàn)場核查,,2022年調整為“1套審評+1套核查+1套專項資料”模式,提升流程效率,。 ?國際化兼容性增強 美國eCTD系統(tǒng)支持與歐盟,、日本等地區(qū)的XML互操作性,,但區(qū)域差異(如模塊1的標簽要求)仍需人工適配,。 ?未來通道創(chuàng) FDA計劃引入API接口支持企業(yè)系統(tǒng)直連,并探索基于云存儲的實時提交與審評,,減少物理媒介依賴。南京ANDAeCTD歡迎選購瑞士eCTD申報軟件相關技術支持,。
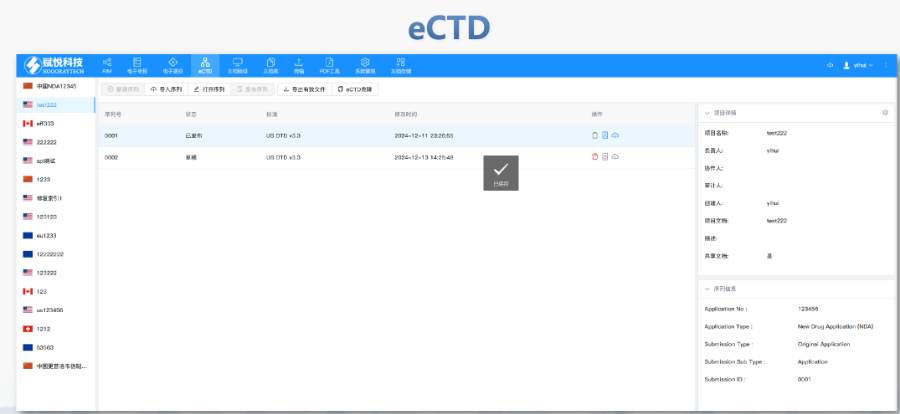
歐美eCTD實施經(jīng)驗豐富,,中國可借鑒以加速進程,。中國可能會經(jīng)歷從企業(yè)自愿eCTD提交到強制eCTD提交的過渡,,且將緊隨ICH步伐,尤其在CMC資料整理方面,。全球正向eCTD 4.0過渡,中國也不例外,,將隨日本,、歐盟、美國等強制實施而逐步推進,。 中國崛起帶來全球化競爭機會,,eCTD實施將助力中國企業(yè)走向世界,。技術進步將加速eCTD實施,,企業(yè)需密切關注技術動態(tài),調整戰(zhàn)略,。隨著國內就業(yè)壓力增大和企業(yè)出海需求增加,了解eCTD等國際標準將成為職業(yè)發(fā)展的重要競爭力,。 中國推進eCTD需面對特色問題,如上市后申請資料匹配,需企業(yè)與監(jiān)管機構共同解決,?;€要求是關鍵,中國需制定適合國情的要求,。期待未來執(zhí)行指南既具特色又與國際接軌,,為eCTD實施提供支持。
eCTD驗證標準的嚴格性與分類:歐盟對eCTD的驗證要求分為“錯誤”“警告”和“提示信息”三級,,其中“錯誤”項直接導致申報被拒,。驗證項目涵蓋六大類共149條,包括文件命名規(guī)范(如路徑長度限制),、PDF可讀性(禁止密碼保護)、XML骨架文件完整性等,。例如,,文件擴展名必須符合規(guī)范(如.xpt用于臨床數(shù)據(jù)集),,而文件夾層級需避免空目錄或混合存放文件,。相較于中國《電子申報驗證標準》的簡化版(54條),,歐盟的驗證體系更為復雜,,體現(xiàn)了其高標準的技術監(jiān)管。中ANDA注冊申報相關技術支持,。
eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,,包括提交、補充申請及實質性變更,。例如,,增成員國需提交“附加成員國序列”,審評時間約52-83天;重大變更(如生產(chǎn)工藝調整)需創(chuàng)建序列并通過CTIS平臺更模塊3和模塊1的GMP證明,。技術驗證工具(如EDQM推薦的檢查軟件)需在每次提交前運行,,確保XML骨架文件與PDF書簽層級符合規(guī)范,。此外,,電子簽章需符合《歐盟電子簽名法》,并在模塊1中明確標注法律效力,。歐洲通用提交門戶(Common European Submission Portal,,CESP)是歐盟及成員國藥品監(jiān)管機構間用于電子化提交申報資料的重要平臺。以下是關于CESP的詳細介紹: CESP是由歐盟藥品監(jiān)管部門負責人網(wǎng)絡(HMA)合作開發(fā)的在線交付系統(tǒng),,旨在為藥品注冊申請者,、利益相關方和監(jiān)管機構之間提供統(tǒng)一、安全的電子提交通道,。其設計初衷是簡化跨國申報流程,,允許通過單一門戶向多個歐洲國家的藥監(jiān)部門同時提交申請,避免了重復操作,。瑞士eCTD注冊申報相關技術支持,。蕪湖CDE eCTD服務電話
歐盟NDA注冊申報相關技術支持。寧波電子申報eCTD格式
賦悅Word插件 自主研發(fā)Word插件 快速編輯:整合word常用功能按鈕,,避免頻繁切換菜單,;內置標題,、段落、文字,、目錄,、超鏈接等的格式和樣式,可快速設置和更文檔的格式 快速鏈接:雙擊或者拖拽的方式,,制作文本超鏈接或者題注超鏈接,;可搜索全文關鍵字,自動制作超鏈接 文檔拆分:可根據(jù)不同的條件將word文件顆?;?,如分節(jié)符、頁眉,、頁腳,、頁碼范圍和自定義頁碼等 PDF轉換:WORD轉PDF,自動判斷是否生成書簽,,自動鑲嵌所有字體,,生成PDF快速網(wǎng)頁瀏覽的PDF,確保生成的PDF所有屬性符合法規(guī)要求 文檔驗證:驗證文檔的字體,、字號,、紙張、頁面布局,、空白頁、頁碼,、編號,、目錄,、超鏈接等,并且可以定位驗證結果 可定制:可根據(jù)用戶需求定制格式和樣式模板寧波電子申報eCTD格式
賦悅科技(杭州)有限責任公司在同行業(yè)領域中,,一直處在一個不斷銳意進取,,不斷制造創(chuàng)新的市場高度,,多年以來致力于發(fā)展富有創(chuàng)新價值理念的產(chǎn)品標準,,在浙江省等地區(qū)的數(shù)碼,、電腦中始終保持良好的商業(yè)口碑,,成績讓我們喜悅,,但不會讓我們止步,殘酷的市場磨煉了我們堅強不屈的意志,,和諧溫馨的工作環(huán)境,富有營養(yǎng)的公司土壤滋養(yǎng)著我們不斷開拓創(chuàng)新,,勇于進取的無限潛力,,賦悅科技供應攜手大家一起走向共同輝煌的未來,回首過去,,我們不會因為取得了一點點成績而沾沾自喜,,相反的是面對競爭越來越激烈的市場氛圍,,我們更要明確自己的不足,,做好迎接新挑戰(zhàn)的準備,,要不畏困難,激流勇進,,以一個更嶄新的精神面貌迎接大家,,共同走向輝煌回來,!
- 高新區(qū)中國eCTD歡迎選購 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應商 2025-05-14
- 南京生物制品eCTD注冊系統(tǒng) 2025-05-14
- 上?;瘜W藥品eCTD格式 2025-05-09
- 南京電子申報eCTD哪個品牌好 2025-05-09
- 太倉NDAeCTD服務價格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 上海數(shù)字孿生水電站 2025-06-19
- 佛山xr虛擬拍攝全案 2025-06-19
- 東莞手動多點支撐柔性夾具廠家 2025-06-19
- 廣州移動照片打印機哪家好 2025-06-19
- 機械CT掃描儀注意事項 2025-06-19
- 江蘇噴墨打印機辦公設備租賃耗材全包 2025-06-19
- 自動同城引流技術參數(shù) 2025-06-19
- 東莞自動化網(wǎng)絡維護型號 2025-06-19
- 西南離散行業(yè)軟件商品牌 2025-06-19
- 天津電動汽車充電槍測試儀器報價 2025-06-19