蕪湖ANDAeCTD醫(yī)療科技
仿制藥作為提高藥物可及性與可負(fù)擔(dān)性的一類藥物,,2012年以前,,注冊(cè)審評(píng)是不收取任何費(fèi)用的,但當(dāng)時(shí)仿制藥申請(qǐng)積壓嚴(yán)重,,從申報(bào)到獲批需要3~5年的時(shí)間,。 美國國會(huì)于2012年頒布了仿制藥使用者費(fèi)用修正案(Generic Drug User Fee Amendments, GDUFA),,該法律要求制藥行業(yè)支付一定的用戶費(fèi)用,以補(bǔ)充仿制藥申請(qǐng)的審評(píng)以及現(xiàn)場(chǎng)檢查的費(fèi)用,,減少仿制藥申請(qǐng)積壓,,縮短審評(píng)時(shí)間,增加基于風(fēng)險(xiǎn)的現(xiàn)場(chǎng)檢查等,,其目的是加快公眾獲得安全有效的仿制藥,,并降低行業(yè)成本。 GDUFA必須每五年重授權(quán)一次,于2017年更(GDUFA II),,于2022年更(GDUFA III),; 目前收費(fèi)種類分為以下四種:ANDA審評(píng)費(fèi)、DMF審評(píng)費(fèi),,在審評(píng)時(shí)一次性繳納,;項(xiàng)目費(fèi)(Program fee)、設(shè)施費(fèi)(Facility fee),,是上市后每年繳納一次,。澳大利亞DMF注冊(cè)申報(bào)相關(guān)技術(shù)支持。蕪湖ANDAeCTD醫(yī)療科技

eCTD 4.0版本的過渡與升級(jí):FDA于2023年啟動(dòng)eCTD 4.0技術(shù)試點(diǎn),,2024年9月正式接收申請(qǐng),,計(jì)劃2029年完成全過渡。4.0版本改用HL7 RPS標(biāo)準(zhǔn)替代XML,,支持雙向通信和跨申請(qǐng)文件復(fù)用,,例如同一Study ID可在IND和NDA享。模塊1的校驗(yàn)碼從MD5升級(jí)為SHA-256,,主干文件由改為,,序列號(hào)取消前導(dǎo)零(如“1”而非“0001”)。企業(yè)需同步更軟件系統(tǒng)以適應(yīng)架構(gòu),。DMF與IND申報(bào)的特殊要求:針對(duì)Type II(原料藥)和Type IV(輔料)DMF,,eCTD模塊3需詳細(xì)描述生產(chǎn)工藝,、穩(wěn)定性數(shù)據(jù),,并附分析證書(COA),。FDA要求DMF持有人指定美國境內(nèi)代理人,,確保溝通效率,且LOA(授權(quán)書)需明確引用范圍,。IND安全性報(bào)告(如SUSAR)需通過eCTD模塊5.3.5提交,,15天內(nèi)完成,,并嵌入CIOMS或MedWatch表格,。2024年指南強(qiáng)調(diào),,臨床數(shù)據(jù)庫需以SAS XPORT格式提交,單個(gè)文件超過4GB需拆分并說明規(guī)則,。安徽NDAeCTD瑞士eCTD注冊(cè)申報(bào)相關(guān)技術(shù)支持。
ANDA遞交: 按照ICH M4的CTD格式整理資料,,并以eCTD格式遞交,; 通過ESG通道遞交資料; 收到CDER的letter,,說明資料已經(jīng)進(jìn)入FDA數(shù)據(jù)庫,; 付GDUFA費(fèi),在資料遞交后的10日內(nèi)到賬; ANDA接收: 繳費(fèi)后,,F(xiàn)DA初步審查資料的完整性,,并會(huì)在60天給答復(fù)。 第一種情況是ANDA無缺陷,,F(xiàn)DA給申請(qǐng)人發(fā)受理信(Acceptance Letter),; 第二種情況是ANDA包含少于10個(gè)小缺陷,F(xiàn)DA將會(huì)通過電話,、傳真,、電子郵件等方式通知發(fā)布IR (信息請(qǐng)求函),讓申請(qǐng)人在7個(gè)日歷日內(nèi)改正,,若未按時(shí)補(bǔ)充所有需要的資料,,F(xiàn)DA將拒收該ANDA; 第三種情況是ANDA包含1個(gè)或者多個(gè)重大缺陷,,或10個(gè)以上的小缺陷,,F(xiàn)DA將拒收該ANDA; 注:如果這邊被拒收,,只退75%的費(fèi)用,。
eCTD的法規(guī)框架與技術(shù)規(guī)范:歐盟eCTD的法規(guī)層級(jí)包括指南(Guidelines)、指令(Directive)和法規(guī)(Regulation),。其中,,法規(guī)(如CTR)具有直接法律效力,而指南(如ICH eCTD規(guī)范)則為技術(shù)操作提供參考,。eCTD的結(jié)構(gòu)需符合歐盟模塊1規(guī)范(DTD 3.0+),,包含行政文件(模塊1)、質(zhì)量數(shù)據(jù)(模塊3)及臨床研究報(bào)告(模塊5)等內(nèi)容,,并通過XML文件實(shí)現(xiàn)數(shù)據(jù)互聯(lián),。例如,CEP(歐洲藥典適用性證書)的eCTD申報(bào)需單獨(dú)構(gòu)建信封(Envelope)和模塊1,,并指定標(biāo)識(shí)符(UUID)以確保技術(shù)合規(guī)性,。eCTD申報(bào)軟件相關(guān)技術(shù)支持。
美國eCTD的強(qiáng)制實(shí)施時(shí)間與范圍:美國自2017年5月5日起要求藥申請(qǐng)(NDA),、仿制藥申請(qǐng)(ANDA)和生物制品許可申請(qǐng)(BLA)必須通過eCTD格式提交,,2018年5月5日進(jìn)一步擴(kuò)展至臨床試驗(yàn)申請(qǐng)(IND)和藥品主文件(DMF)。FDA通過《聯(lián)邦食品,、藥品和化妝品法案》第745A條明確電子提交的強(qiáng)制性,,豁免非商業(yè)化IND和部分DMF類型(如Ⅲ類)。2023年數(shù)據(jù)顯示,,F(xiàn)DA接收的eCTD申請(qǐng)占比已達(dá)92%,,標(biāo)志著電子化審評(píng)體系的成熟,。企業(yè)若未按規(guī)范提交(如缺少文件或重復(fù)序列號(hào)),將直接被拒收,。澳大利亞IND注冊(cè)申報(bào)相關(guān)技術(shù)支持,。浙江CDE eCTD發(fā)布系統(tǒng)
瑞士IND注冊(cè)申報(bào)相關(guān)技術(shù)支持。蕪湖ANDAeCTD醫(yī)療科技
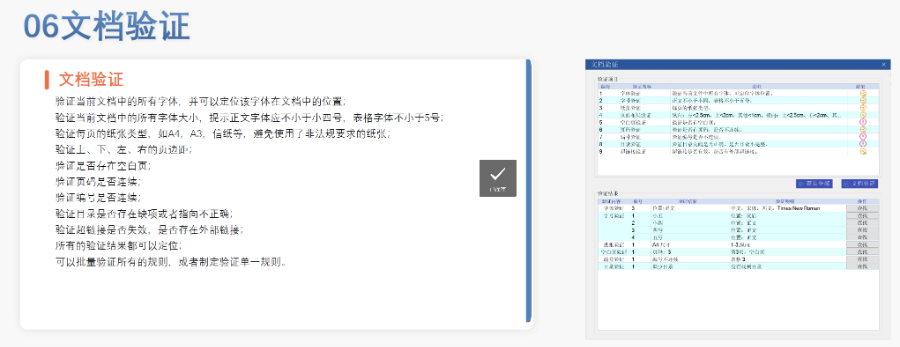
eCTD驗(yàn)證標(biāo)準(zhǔn)的嚴(yán)格性與分類:歐盟對(duì)eCTD的驗(yàn)證要求分為“錯(cuò)誤”“警告”和“提示信息”三級(jí),,其中“錯(cuò)誤”項(xiàng)直接導(dǎo)致申報(bào)被拒,。驗(yàn)證項(xiàng)目涵蓋六大類共149條,包括文件命名規(guī)范(如路徑長度限制),、PDF可讀性(禁止密碼保護(hù)),、XML骨架文件完整性等。例如,,文件擴(kuò)展名必須符合規(guī)范(如.xpt用于臨床數(shù)據(jù)集),,而文件夾層級(jí)需避免空目錄或混合存放文件。相較于中國《電子申報(bào)驗(yàn)證標(biāo)準(zhǔn)》的簡(jiǎn)化版(54條),,歐盟的驗(yàn)證體系更為復(fù)雜,,體現(xiàn)了其高標(biāo)準(zhǔn)的技術(shù)監(jiān)管。蕪湖ANDAeCTD醫(yī)療科技
- 高新區(qū)中國eCTD歡迎選購 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊(cè)系統(tǒng) 2025-05-14
- 上?;瘜W(xué)藥品eCTD格式 2025-05-09
- 南京電子申報(bào)eCTD哪個(gè)品牌好 2025-05-09
- 太倉NDAeCTD服務(wù)價(jià)格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 通州區(qū)社交平臺(tái)代運(yùn)營費(fèi)用 2025-06-08
- 天津高性價(jià)比工控機(jī)供應(yīng)商 2025-06-08
- 陜西工業(yè)攝像頭模組詢價(jià) 2025-06-08
- 長沙企業(yè)網(wǎng)絡(luò)安全應(yīng)急預(yù)案 2025-06-08
- 西湖區(qū)打印機(jī)租賃有幾種套餐 2025-06-08
- 轉(zhuǎn)化私域流量運(yùn)營常見問題 2025-06-08
- 黑龍江能源系統(tǒng)子母鐘生產(chǎn)廠家 2025-06-08
- 玄武區(qū)新型企業(yè)管理服務(wù) 2025-06-08
- 淮安怎樣智慧消防設(shè)計(jì) 2025-06-08
- 上?;瘜W(xué)發(fā)光線束加工 2025-06-08