-
航瑞智能助力維尚家具打造自動倉儲系統(tǒng),,實(shí)現(xiàn)成品物流智能化升級
-
航瑞智能:準(zhǔn)確把握倉儲痛點(diǎn),,打造多樣化智能倉儲方案
-
高度集成化自動化立體倉庫:開啟高效物流新時代_航瑞智能
-
探秘倉儲物流中心:輸送機(jī)與RGV打造高效智能物流體系
-
共享裝備攜手航瑞智能打造砂芯智能倉儲,實(shí)現(xiàn)倉儲物流智能化升級
-
桁架機(jī)械手與輸送機(jī):打造高效智能流水線
-
?采用WMS倉庫管理系統(tǒng)能夠給企業(yè)帶來哪些好處,?
-
?航瑞智能:精細(xì)把握倉儲痛點(diǎn),,打造多樣化智能倉儲方案
-
往復(fù)式提升機(jī):垂直輸送系統(tǒng)的智能化解決方案
-
航瑞智能:準(zhǔn)確把握倉儲痛點(diǎn),,打造多樣化智能倉儲方案
安徽國際注冊eCTD銷售電話
歐盟eCTD的遞交途徑與技術(shù)要求 不同審評程序?qū)?yīng)不同遞交渠道:集中程序(CP)通過EMA的eSubmission Gateway或Web Client提交,分散程序(DCP)和互認(rèn)程序(MRP)則需使用歐盟通用提交門戶(CESP)。文件結(jié)構(gòu)需嚴(yán)格遵循模塊化要求,,例如CEP申請需包含模塊1(行政文件),、模塊2(質(zhì)量概述)和模塊3(技術(shù)文檔),且XML主干文件須符合EDQM的特定命名規(guī)則,。此外,,所有PDF文件需無密碼保護(hù)、可全文檢索,,并嵌入層級書簽以支持快速審閱,。 CEP申請的eCTD遞交特殊性 CEP程序自2018年起強(qiáng)制采用eCTD格式,重點(diǎn)評估原料藥是否符合歐洲藥典標(biāo)準(zhǔn),。其模塊1需包含EDQM申請表,、簡歷及變更說明表,模塊2需使用EDQM提供的質(zhì)量概述模板,,模塊3則按CTD格式組織3.2.S章節(jié)內(nèi)容,。CEP與ASMF(活性物質(zhì)主文件)的主要區(qū)別在于性:CEP無需關(guān)聯(lián)上市許可,且審評由EDQM完成,。美國eCTD注冊咨詢相關(guān)技術(shù)支持,。安徽國際注冊eCTD銷售電話
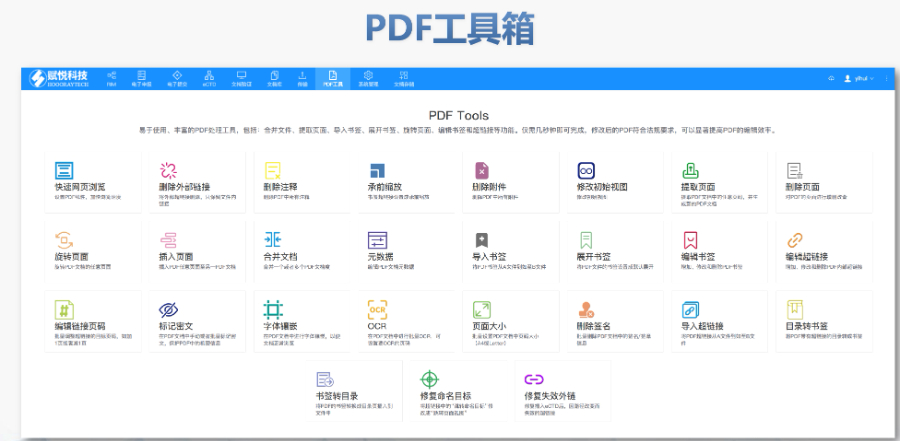
DMF維護(hù)與合規(guī) ?年度更 即使無變更,每年需提交聲明,;重大工藝/設(shè)施變更需及時通知客戶并更文件,。 ?現(xiàn)場檢查 原料藥企業(yè)需通過FDA現(xiàn)場檢查,驗證是否符合ICH Q7 GMP標(biāo)準(zhǔn),,并與DMF內(nèi)容一致,。 ?轉(zhuǎn)讓與關(guān)閉 ?轉(zhuǎn)讓:需書面通知FDA并提供持有者信息。 ?關(guān)閉:未提交年度報告或持有人主動申請,,需說明原因并通知所有授權(quán)方,。 關(guān)鍵注意事項 ?數(shù)據(jù)質(zhì)量:所有資料需準(zhǔn)確、完整,,減少審核延遲風(fēng)險,。 ?合規(guī)性:遵循FDA指南(如21 CFR Part 207)及USP標(biāo)準(zhǔn)(如培養(yǎng)基物料來源級別)。 ?溝通機(jī)制:建議通過專業(yè)機(jī)構(gòu)(如瑞歐佰藥)協(xié)助,,定期提交周報并制定計劃表以提高效率,。 常見問題解答 ?生物制品分類:培養(yǎng)基、外泌體等均屬Ⅱ類DMF,。 ?質(zhì)量標(biāo)準(zhǔn):參考USP及同行標(biāo)準(zhǔn),,需提供分析方法驗證及雜質(zhì)對比研究。 ?周期估算:資料準(zhǔn)備約5-50個工作日,,總周期受缺陷回復(fù)影響,。工業(yè)園區(qū)NDAeCTD品牌瑞士eCTD驗證標(biāo)準(zhǔn)相關(guān)技術(shù)支持,。

爭議解決與法律救濟(jì) 若申請人對審評結(jié)果有異議,可向EMA的CHMP申請重審查,,或在歐盟法院提起行政訴訟,。eCTD的完整提交記錄可作為法律證據(jù),證明申請人已履行合規(guī)義務(wù),。EDQM設(shè)立仲裁委員會,處理CEP程序中的技術(shù)爭議,。 行業(yè)趨勢與競爭格局 全球eCTD服務(wù)市場年增長率達(dá)12%,,歐盟占據(jù)35%份額,主要服務(wù)商包括PharmaLex,、Certara等,。頭部藥企通過自建IT團(tuán)隊降低成本,而中小型企業(yè)依賴外包以專注研發(fā),。人工智能(AI)在文件自動生成和審評意見預(yù)測中的應(yīng)用逐漸增多,。 患者參與與透明度提升 EMA通過公開eCTD摘要(如模塊2.5臨床概要)增強(qiáng)審評透明度,患者組織可提交意見影響審評決策,。部分成員國要求模塊1包含患者語言版本說明書,,以提升用藥依從性。未來,,eCTD4.0或支持直接鏈接患者反饋平臺,,實(shí)現(xiàn)全生命周期互動。
eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,,包括提交,、補(bǔ)充申請及實(shí)質(zhì)性變更。例如,,增成員國需提交“附加成員國序列”,,審評時間約52-83天;重大變更(如生產(chǎn)工藝調(diào)整)需創(chuàng)建序列并通過CTIS平臺更模塊3和模塊1的GMP證明,。技術(shù)驗證工具(如EDQM推薦的檢查軟件)需在每次提交前運(yùn)行,,確保XML骨架文件與PDF書簽層級符合規(guī)范。此外,,電子簽章需符合《歐盟電子簽名法》,,并在模塊1中明確標(biāo)注法律效力。歐洲通用提交門戶(Common European Submission Portal,,CESP)是歐盟及成員國藥品監(jiān)管機(jī)構(gòu)間用于電子化提交申報資料的重要平臺,。以下是關(guān)于CESP的詳細(xì)介紹: CESP是由歐盟藥品監(jiān)管部門負(fù)責(zé)人網(wǎng)絡(luò)(HMA)合作開發(fā)的在線交付系統(tǒng),旨在為藥品注冊申請者,、利益相關(guān)方和監(jiān)管機(jī)構(gòu)之間提供統(tǒng)一,、安全的電子提交通道,。其設(shè)計初衷是簡化跨國申報流程,允許通過單一門戶向多個歐洲國家的藥監(jiān)部門同時提交申請,,避免了重復(fù)操作,。加拿大eCTD驗證標(biāo)準(zhǔn)相關(guān)技術(shù)支持。
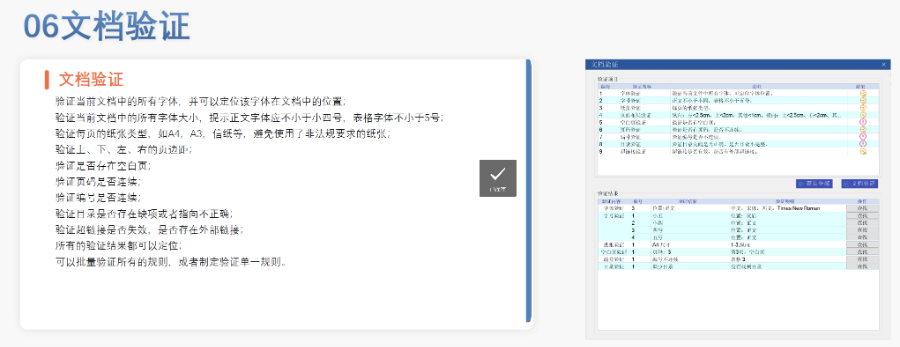
電子遞交的合規(guī)性與風(fēng)險管理 歐盟要求申請人確保電子資料與紙質(zhì)版本完全一致,,若未在規(guī)定時間提交紙質(zhì)文件可能導(dǎo)致注冊終止,。驗證過程中,“錯誤”級別問題(如文件命名不規(guī)范,、XML邏輯錯誤)必須修正,,而“警告”和“提示信息”則建議優(yōu)化以提升審評體驗。EDQM和EMA均提供驗證工具,,申請人需在遞交前完成內(nèi)部預(yù)驗證,。 官方費(fèi)用結(jié)構(gòu)與支付流程 歐盟eCTD遞交費(fèi)用因?qū)徳u程序類型而異:集中程序費(fèi)用較高,涵蓋科學(xué)評估和合規(guī)審查成本,;國家程序費(fèi)用由各成員國自行設(shè)定,。CEP申請需向EDQM支付評審費(fèi),具體金額根據(jù)原料藥類型和變更復(fù)雜度分級,。繳費(fèi)需通過官方指定渠道完成,,并附上付款憑證作為模塊1的組成部分。 多語言支持與翻譯要求 盡管歐盟允許使用英語提交,,但部分成員國要求模塊一的行政文件翻譯為本地語言,。臨床試驗數(shù)據(jù)庫(如SDTM和ADaM)需以英語呈現(xiàn),同時提供雙語標(biāo)簽以支持多國審閱,。專業(yè)翻譯服務(wù)在確保技術(shù)術(shù)語準(zhǔn)確性方面至關(guān)重要,,尤其針對復(fù)雜藥學(xué)和非臨床數(shù)據(jù)。歐盟NDA注冊申報相關(guān)技術(shù)支持,。新疆eCTD供應(yīng)商
加拿大IND注冊申報相關(guān)技術(shù)支持,。安徽國際注冊eCTD銷售電話
危機(jī)應(yīng)對與應(yīng)急遞交機(jī)制 在公共衛(wèi)生緊急事件(如COVID-19)中,EMA允許簡化eCTD序列,,優(yōu)先審評關(guān)鍵模塊并暫緩非數(shù)據(jù),。申請人可通過快速通道(Fast Track)提交疫苗或藥物的eCTD資料,審評周期可壓縮至6個月,。此類申請需附風(fēng)險評估報告,,并承諾后續(xù)補(bǔ)交完整數(shù)據(jù)。 數(shù)據(jù)安全與長期存檔 歐盟要求eCTD資料存檔期限至少為藥品上市后30年,,EMA采用分布式存儲和區(qū)塊鏈技術(shù)確保數(shù)據(jù)不可篡改,。申請人需定期備份本地副本,并使用符合GDPR要求的加密傳輸協(xié)議(如AS2)遞交,。歷史數(shù)據(jù)的遷移和格式轉(zhuǎn)換(如NeeS轉(zhuǎn)eCTD)需遵循特定技術(shù)規(guī)范,。 環(huán)保效益與可持續(xù)發(fā)展 eCTD取代紙質(zhì)遞交后,,歐盟每年減少約500噸紙張消耗,審評流程的數(shù)字化降低碳足跡約30%,。虛擬審評會議和電子簽名進(jìn)一步減少了差旅需求,,契合歐盟2050碳中和目標(biāo)。未來,,eCTD4.0將通過數(shù)據(jù)壓縮技術(shù)進(jìn)一步降低服務(wù)器能耗,。安徽國際注冊eCTD銷售電話
- 高新區(qū)中國eCTD歡迎選購 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊系統(tǒng) 2025-05-14
- 上海化學(xué)藥品eCTD格式 2025-05-09
- 南京電子申報eCTD哪個品牌好 2025-05-09
- 太倉NDAeCTD服務(wù)價格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 寧波儲能線束定制 2025-06-04
- ??谖臅浵駧?shù)據(jù)轉(zhuǎn)換 2025-06-04
- 惠州硬盤報價 2025-06-04
- 安防監(jiān)控識別價格 2025-06-04
- 楊浦區(qū)品牌搜索引擎代運(yùn)營 2025-06-04
- 成都醫(yī)療內(nèi)窺鏡攝像頭模組聯(lián)系方式 2025-06-04
- 共享無線充開發(fā) 2025-06-04
- 沈陽直流充電槍測試儀廠商 2025-06-04
- 自動化銷售云T云銷售公司 2025-06-04
- 衡陽定制商用電腦設(shè)備租賃方案 2025-06-04