楊浦區(qū)賦悅科技eCTD推薦
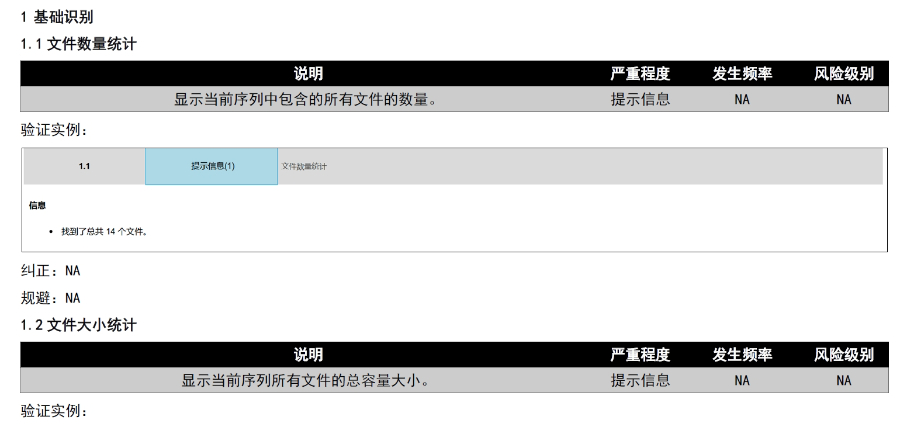
eCTD驗(yàn)證標(biāo)準(zhǔn)的嚴(yán)格性與分類:歐盟對eCTD的驗(yàn)證要求分為“錯(cuò)誤”“警告”和“提示信息”三級,,其中“錯(cuò)誤”項(xiàng)直接導(dǎo)致申報(bào)被拒,。驗(yàn)證項(xiàng)目涵蓋六大類共149條,包括文件命名規(guī)范(如路徑長度限制),、PDF可讀性(禁止密碼保護(hù)),、XML骨架文件完整性等。例如,,文件擴(kuò)展名必須符合規(guī)范(如.xpt用于臨床數(shù)據(jù)集),,而文件夾層級需避免空目錄或混合存放文件。相較于中國《電子申報(bào)驗(yàn)證標(biāo)準(zhǔn)》的簡化版(54條),,歐盟的驗(yàn)證體系更為復(fù)雜,,體現(xiàn)了其高標(biāo)準(zhǔn)的技術(shù)監(jiān)管。eCTD驗(yàn)證實(shí)踐手冊相關(guān)技術(shù)支持,。楊浦區(qū)賦悅科技eCTD推薦

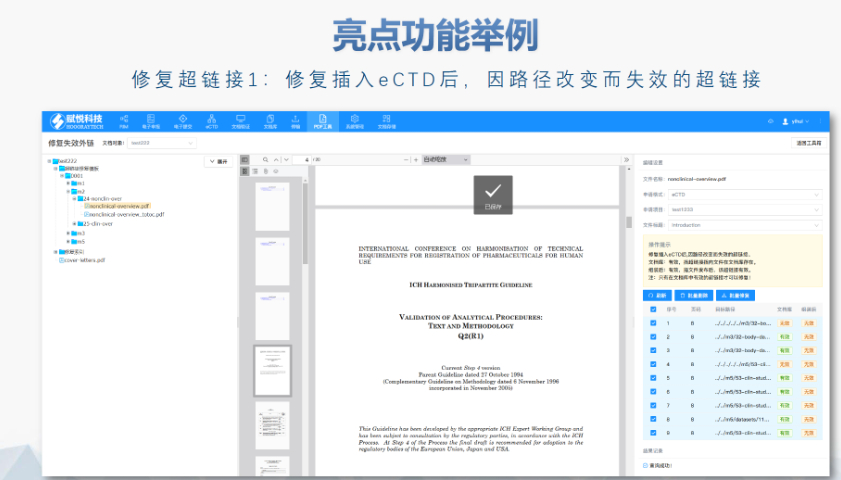
PDF工具箱 ?批量處理與格式修復(fù) 支持PDF合并,、拆分、提取頁面,、旋轉(zhuǎn)頁面等操作,可批量修復(fù)字體未嵌入,、超鏈接錯(cuò)誤等問題,,確保文件符合藥品注冊法規(guī)要求。 ?智能書簽與超鏈接管理 提供書簽導(dǎo)入/導(dǎo)出,、超鏈接自動生成(支持關(guān)鍵字搜索定位鏈接),、題注超鏈接拖拽式編輯等功能,簡化復(fù)雜文檔的導(dǎo)航設(shè)計(jì),。 ?文檔轉(zhuǎn)換與OCR識別 支持Word轉(zhuǎn)PDF(自動生成書簽,、嵌入字體),以及PDF與Word,、Excel等格式互轉(zhuǎn),,集成OCR功能用于掃描件文字識別。 ?合規(guī)性驗(yàn)證 自動驗(yàn)證PDF的頁面布局,、頁碼連續(xù)性,、空白頁、目錄層級等屬性,,并定位具體錯(cuò)誤位置,,減少人工檢查成本,。 ?安全與協(xié)作功能 支持文檔加密、數(shù)字簽名,、云端同步及多設(shè)備共享,,滿足企業(yè)級文件安全管理需求。閔行區(qū)原料藥eCTD服務(wù)商中DMF注冊申報(bào)相關(guān)技術(shù)支持,。
區(qū)域化差異與多國協(xié)作挑戰(zhàn) 歐盟eCTD需兼容成員國特定要求,,例如模塊一的行政信息需符合各國語言和法規(guī)差異?;フJ(rèn)程序(MRP)中,,參考成員國(RMS)的評估報(bào)告需被其他成員國認(rèn)可,若出現(xiàn)分歧需由CMDh協(xié)調(diào)或提交EMA仲裁,。這種多層級審評機(jī)制要求申請人在文件準(zhǔn)備階段即考慮區(qū)域兼容性,,避免后續(xù)流程延誤。 eCTD4.0的探索與未來方向 ICH于2015年發(fā)布的eCTD4.0版本旨在簡化目錄結(jié)構(gòu),、支持多產(chǎn)品類型(如醫(yī)療器械)申報(bào),,并增強(qiáng)生命周期管理功能。歐盟計(jì)劃通過2024年試點(diǎn)逐步過渡至4.0,,其扁平化文件組織方式有望減少重復(fù)提交并提升審評效率,。然而,實(shí)施需解決現(xiàn)有系統(tǒng)兼容性及行業(yè)適應(yīng)性問題,。
賦悅Word插件 自主研發(fā)Word插件 快速編輯:整合word常用功能按鈕,,避免頻繁切換菜單;內(nèi)置標(biāo)題,、段落,、文字、目錄,、超鏈接等的格式和樣式,,可快速設(shè)置和更文檔的格式 快速鏈接:雙擊或者拖拽的方式,制作文本超鏈接或者題注超鏈接,;可搜索全文關(guān)鍵字,,自動制作超鏈接 文檔拆分:可根據(jù)不同的條件將word文件顆粒化,,如分節(jié)符,、頁眉、頁腳,、頁碼范圍和自定義頁碼等 PDF轉(zhuǎn)換:WORD轉(zhuǎn)PDF,,自動判斷是否生成書簽,自動鑲嵌所有字體,生成PDF快速網(wǎng)頁瀏覽的PDF,,確保生成的PDF所有屬性符合法規(guī)要求 文檔驗(yàn)證:驗(yàn)證文檔的字體,、字號、紙張,、頁面布局,、空白頁、頁碼,、編號,、目錄、超鏈接等,,并且可以定位驗(yàn)證結(jié)果 可定制:可根據(jù)用戶需求定制格式和樣式模板加拿大eCTD申報(bào)軟件相關(guān)技術(shù)支持,。
爭議解決與法律救濟(jì) 若申請人對審評結(jié)果有異議,可向EMA的CHMP申請重審查,,或在歐盟法院提起行政訴訟,。eCTD的完整提交記錄可作為法律證據(jù),證明申請人已履行合規(guī)義務(wù),。EDQM設(shè)立仲裁委員會,,處理CEP程序中的技術(shù)爭議。 行業(yè)趨勢與競爭格局 全球eCTD服務(wù)市場年增長率達(dá)12%,,歐盟占據(jù)35%份額,,主要服務(wù)商包括PharmaLex、Certara等,。頭部藥企通過自建IT團(tuán)隊(duì)降低成本,,而中小型企業(yè)依賴外包以專注研發(fā)。人工智能(AI)在文件自動生成和審評意見預(yù)測中的應(yīng)用逐漸增多,。 患者參與與透明度提升 EMA通過公開eCTD摘要(如模塊2.5臨床概要)增強(qiáng)審評透明度,,患者組織可提交意見影響審評決策。部分成員國要求模塊1包含患者語言版本說明書,,以提升用藥依從性。未來,,eCTD4.0或支持直接鏈接患者反饋平臺,,實(shí)現(xiàn)全生命周期互動。美國eCTD注冊咨詢相關(guān)技術(shù)支持,。浙江INDeCTD常用解決方案
加拿大ANDA注冊申報(bào)相關(guān)技術(shù)支持,。楊浦區(qū)賦悅科技eCTD推薦
電子遞交的合規(guī)性與風(fēng)險(xiǎn)管理 歐盟要求申請人確保電子資料與紙質(zhì)版本完全一致,若未在規(guī)定時(shí)間提交紙質(zhì)文件可能導(dǎo)致注冊終止,。驗(yàn)證過程中,,“錯(cuò)誤”級別問題(如文件命名不規(guī)范、XML邏輯錯(cuò)誤)必須修正,而“警告”和“提示信息”則建議優(yōu)化以提升審評體驗(yàn),。EDQM和EMA均提供驗(yàn)證工具,,申請人需在遞交前完成內(nèi)部預(yù)驗(yàn)證。 官方費(fèi)用結(jié)構(gòu)與支付流程 歐盟eCTD遞交費(fèi)用因?qū)徳u程序類型而異:集中程序費(fèi)用較高,,涵蓋科學(xué)評估和合規(guī)審查成本,;國家程序費(fèi)用由各成員國自行設(shè)定。CEP申請需向EDQM支付評審費(fèi),,具體金額根據(jù)原料藥類型和變更復(fù)雜度分級,。繳費(fèi)需通過官方指定渠道完成,并附上付款憑證作為模塊1的組成部分,。 多語言支持與翻譯要求 盡管歐盟允許使用英語提交,,但部分成員國要求模塊一的行政文件翻譯為本地語言。臨床試驗(yàn)數(shù)據(jù)庫(如SDTM和ADaM)需以英語呈現(xiàn),,同時(shí)提供雙語標(biāo)簽以支持多國審閱,。專業(yè)翻譯服務(wù)在確保技術(shù)術(shù)語準(zhǔn)確性方面至關(guān)重要,尤其針對復(fù)雜藥學(xué)和非臨床數(shù)據(jù),。楊浦區(qū)賦悅科技eCTD推薦
- 吳江區(qū)國際注冊eCTD 2025-04-20
- 杭州原料藥eCTD 2025-04-19
- 吳江區(qū)生物制品eCTD名稱 2025-04-19
- 河南eCTD注冊系統(tǒng) 2025-04-19
- 山東國內(nèi)注冊eCTD是什么 2025-04-19
- 南京電子申報(bào)eCTD推薦 2025-04-19
- 河北eCTD軟件 2025-04-19
- 寧波國產(chǎn)eCTD服務(wù)電話 2025-04-19
- 杭州電子申報(bào)eCTD注冊系統(tǒng) 2025-04-19
- 閔行區(qū)生物制品eCTD服務(wù)放心可靠 2025-04-19
- 上海智慧城市數(shù)字化生產(chǎn)企業(yè) 2025-04-20
- 嘉定區(qū)品牌軟件服務(wù)風(fēng)格 2025-04-20
- 武漢什么是手機(jī)維修價(jià)格實(shí)惠 2025-04-20
- 國產(chǎn)整合營銷管理模式 2025-04-20
- Exablaze ExaNIC X10或X25超頻服務(wù)器銷售廠家 2025-04-20
- 甘肅站臺入侵激光雷達(dá) 2025-04-20
- 廣東拍照打印機(jī)廠家 2025-04-20
- 宿遷超薄鼓風(fēng)機(jī)品牌 2025-04-20
- 徐州特殊光解膜規(guī)格尺寸 2025-04-20
- 山西特色軟件開發(fā) 2025-04-20