-
提供成都市四川批發(fā)膩?zhàn)痈嗯l(fā)成都市叁零叁建材供應(yīng)
-
銷售成都市成都膩?zhàn)臃圻x購(gòu)報(bào)價(jià)成都市叁零叁建材供應(yīng)
-
銷售成都市四川膩?zhàn)痈嗯l(fā)價(jià)價(jià)格成都市叁零叁建材供應(yīng)
-
提供成都市山林山界面劑行情成都市叁零叁建材供應(yīng)
-
供應(yīng)成都市如何挑選找平石膏價(jià)格成都市叁零叁建材供應(yīng)
-
銷售成都市界面劑的采購(gòu)廠家成都市叁零叁建材供應(yīng)
-
提供成都市如何選擇兒童膩?zhàn)痈嘈星槌啥际腥闳ú墓?yīng)
-
銷售成都市平石膏使用量報(bào)價(jià)成都市叁零叁建材供應(yīng)
-
銷售成都市找平石膏使用量多少錢成都市叁零叁建材供應(yīng)
-
銷售成都市膩?zhàn)臃鄣暮锰幹变N成都市叁零叁建材供應(yīng)
安徽INDeCTD找哪家
DMF維護(hù)與合規(guī) ?年度更 即使無(wú)變更,,每年需提交聲明,;重大工藝/設(shè)施變更需及時(shí)通知客戶并更文件。 ?現(xiàn)場(chǎng)檢查 原料藥企業(yè)需通過(guò)FDA現(xiàn)場(chǎng)檢查,,驗(yàn)證是否符合ICH Q7 GMP標(biāo)準(zhǔn),,并與DMF內(nèi)容一致,。 ?轉(zhuǎn)讓與關(guān)閉 ?轉(zhuǎn)讓:需書面通知FDA并提供持有者信息。 ?關(guān)閉:未提交年度報(bào)告或持有人主動(dòng)申請(qǐng),,需說(shuō)明原因并通知所有授權(quán)方,。 關(guān)鍵注意事項(xiàng) ?數(shù)據(jù)質(zhì)量:所有資料需準(zhǔn)確、完整,,減少審核延遲風(fēng)險(xiǎn),。 ?合規(guī)性:遵循FDA指南(如21 CFR Part 207)及USP標(biāo)準(zhǔn)(如培養(yǎng)基物料來(lái)源級(jí)別)。 ?溝通機(jī)制:建議通過(guò)專業(yè)機(jī)構(gòu)(如瑞歐佰藥)協(xié)助,,定期提交周報(bào)并制定計(jì)劃表以提高效率,。 常見(jiàn)問(wèn)題解答 ?生物制品分類:培養(yǎng)基、外泌體等均屬Ⅱ類DMF,。 ?質(zhì)量標(biāo)準(zhǔn):參考USP及同行標(biāo)準(zhǔn),,需提供分析方法驗(yàn)證及雜質(zhì)對(duì)比研究,。 ?周期估算:資料準(zhǔn)備約5-50個(gè)工作日,,總周期受缺陷回復(fù)影響。美國(guó)eCTD申報(bào)軟件相關(guān)技術(shù)支持,。安徽INDeCTD找哪家
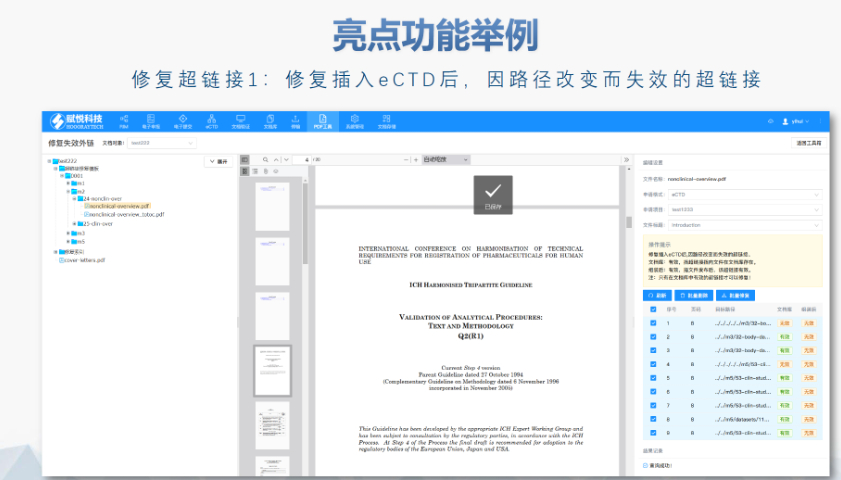
生命周期管理與變更遞交 eCTD支持全生命周期管理,,申請(qǐng)人需通過(guò)序列更(Sequence)反映藥品變更信息。例如CEP證書的更需提交“變更說(shuō)明表”,對(duì)比已批準(zhǔn)和擬修改內(nèi)容,,并附修訂版技術(shù)文檔,。重大變更(如生產(chǎn)工藝調(diào)整)可能觸發(fā)GMP現(xiàn)場(chǎng)檢查,EDQM將根據(jù)風(fēng)險(xiǎn)評(píng)估決定是否啟動(dòng)核查,。 電子簽名與法律效力 歐盟接受符合《電子簽名法》的數(shù)字簽名,,手寫簽名的掃描件需嵌入PDF并加密保護(hù)。模塊1的申請(qǐng)表和承諾書必須包含有效簽名,,且XML文件需通過(guò)MD5校驗(yàn)確保完整性,。若使用第三方簽署工具,需提前向監(jiān)管機(jī)構(gòu)報(bào)備并獲取技術(shù)認(rèn)可,。 中小企業(yè)支持與資源獲取 EMA和EDQM為中小企業(yè)提供eCTD實(shí)施指南,、驗(yàn)證工具及培訓(xùn)研討會(huì)。例如,,EDQM官網(wǎng)發(fā)布CEP遞交模板和案例庫(kù),,EMA則定期更Q&A文檔以解答常見(jiàn)問(wèn)題。此外,,歐盟設(shè)立專項(xiàng)基金,,資助中小企業(yè)完成eCTD轉(zhuǎn)換和系統(tǒng)部署。工業(yè)園區(qū)中國(guó)eCTD服務(wù)電話美國(guó)eCTD注冊(cè)咨詢相關(guān)技術(shù)支持,。

eCTD的技術(shù)架構(gòu)與模塊要求:美國(guó)eCTD基于XML技術(shù),,嚴(yán)格遵循ICH M4框架,分為5個(gè)模塊:模塊1(地區(qū)行政信息),、模塊2(技術(shù)總結(jié)),、模塊3-5(質(zhì)量、非臨床與臨床數(shù)據(jù)),。其中,,模塊1需包含F(xiàn)DA特定的文件,涵蓋申請(qǐng)編號(hào),、聯(lián)系人和DMF授權(quán)書等行政信息,。模塊2-5需與ICH CTD全球統(tǒng)一標(biāo)準(zhǔn)一致,但FDA對(duì)文件顆粒度要求更細(xì),,例如非臨床研究報(bào)告需拆分并標(biāo)記Study ID,。PDF文件需符合FDA v4.1格式規(guī)范,包括字體嵌入,、書簽層級(jí)和超鏈接功能,。
2015年發(fā)布《關(guān)于藥品醫(yī)療器械審評(píng)審批制度的意見(jiàn)》,提出藥監(jiān)五大目標(biāo),,將eCTD納入國(guó)家藥監(jiān)數(shù)字化戰(zhàn)略,。2017年,,中國(guó)加入ICH(國(guó)際人用藥品注冊(cè)技術(shù)協(xié)調(diào)會(huì)),成為全球第八個(gè)監(jiān)管機(jī)構(gòu)成員,,加速與國(guó)際標(biāo)準(zhǔn)接軌,。2018年,國(guó)家藥監(jiān)局(NMPA)完成eCTD文檔管理系統(tǒng)招標(biāo),,由上海寶信與德國(guó)LORENZ合作搭建技術(shù)平臺(tái),,標(biāo)志著技術(shù)基礎(chǔ)設(shè)施的落地。 ?規(guī)范制定與試點(diǎn)階段(2019-2023年)? 2019-2020年,,CDE(藥品審評(píng)中心)發(fā)布《eCTD技術(shù)規(guī)范》《驗(yàn)證標(biāo)準(zhǔn)》等征求意見(jiàn)稿,,并組織兩輪企業(yè)測(cè)試。2021年,,NMPA明確化學(xué)藥1類,、5.1類及生物制品1類上市申請(qǐng)適用eCTD。2022年實(shí)施電子申報(bào)(非eCTD格式),,2023年取消紙質(zhì)資料提交,,為eCTD鋪開(kāi)奠定基礎(chǔ)。 ?實(shí)施與擴(kuò)展階段(2024-2025年)? 2024年3月更電子申報(bào)技術(shù)要求,,7月啟動(dòng)網(wǎng)絡(luò)傳輸試點(diǎn),。2025年1月27日,NMPA將eCTD適用范圍擴(kuò)大至化藥1-5類臨床試驗(yàn)及上市申請(qǐng),、生物制品1-3類全流程,,覆蓋藥、仿制藥及生物類似藥,,實(shí)現(xiàn)與國(guó)際主流申報(bào)模式同步,。瑞士eCTD驗(yàn)證標(biāo)準(zhǔn)相關(guān)技術(shù)支持。
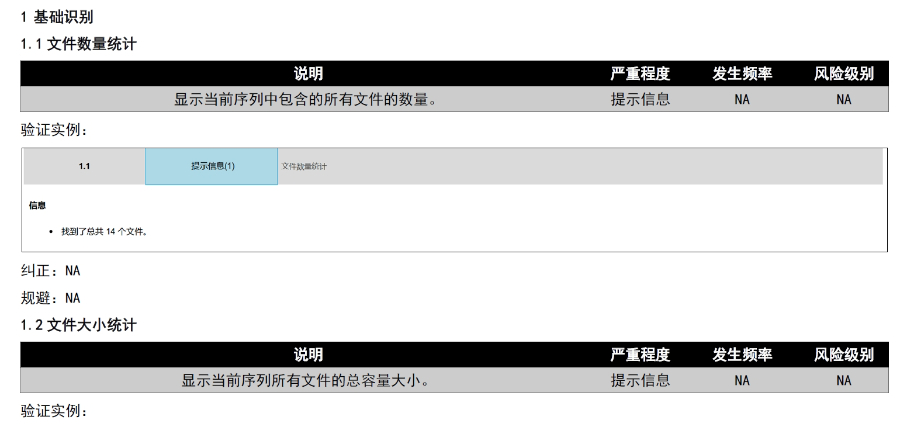
文件生命周期管理:eCTD支持文件替換(Replace),、刪除(Delete)等操作,,而非增文件。例如,,更臨床研究方案時(shí)需用Replace操作覆蓋舊版本,。基線提交(Baseline Submission)可用于補(bǔ)充歷史紙質(zhì)資料,,但需在封面函中聲明無(wú)內(nèi)容變更,。 臨床數(shù)據(jù)與研究標(biāo)簽文件(STF):模塊4和5中的研究數(shù)據(jù)需通過(guò)STF(Study Tagging Files)引用,確保數(shù)據(jù)與文檔關(guān)聯(lián),。FDA要求數(shù)據(jù)集(如SAS XPORT格式)能置于模塊3-5,,且單個(gè)文件超過(guò)4GB需拆分。2022年統(tǒng)計(jì)顯示,,58%的ANDA因研究數(shù)據(jù)技術(shù)拒絕標(biāo)準(zhǔn)(TRC)錯(cuò)誤被拒,。 電子簽名與表格要求:FDA表格(如356h、1571)需使用數(shù)字簽名,,PDF文件禁止加密或設(shè)置編輯限制,。電子簽名需符合21 CFR Part 11規(guī)范,確保身份驗(yàn)證,、不可否認(rèn)性和數(shù)據(jù)完整性,。 外包服務(wù)與系統(tǒng)解決方案:賦悅科技累計(jì)提交超2000份eCTD申請(qǐng),外包可降低40%人工錯(cuò)誤率,。美國(guó)NDA注冊(cè)申報(bào)相關(guān)技術(shù)支持,。閔行區(qū)NDAeCTD常用解決方案
澳大利亞eCTD注冊(cè)外包相關(guān)技術(shù)支持。安徽INDeCTD找哪家
FDA圍繞eCTD發(fā)布了10余項(xiàng)法規(guī)指南,,涵蓋格式要求,、文件生命周期、數(shù)據(jù)安全等細(xì)節(jié),,其中《ICH M2 EWG》作為綜合性技術(shù)文件,,成為企業(yè)申報(bào)的參考。eCTD的實(shí)施提升了審評(píng)效率,,通過(guò)標(biāo)準(zhǔn)化XML結(jié)構(gòu)和電子簽章技術(shù),,減少了紙質(zhì)遞交的物流與時(shí)間成本,同時(shí)支持全生命周期管理,,便于后續(xù)變更和補(bǔ)充資料的動(dòng)態(tài)更,。 美國(guó)在eCTD實(shí)施中注重與ICH國(guó)際標(biāo)準(zhǔn)的兼容性,例如采用統(tǒng)一的CTD模塊化結(jié)構(gòu)和PDF技術(shù)規(guī)范,。然而,,其區(qū)域性要求(如信封信息中的Application ID、Submission Subtype)仍體現(xiàn)本土化特色,。這種“國(guó)際框架+本地適配”的模式,,既保障了跨國(guó)藥企的申報(bào)便利,又滿足了FDA的監(jiān)管需求,。安徽INDeCTD找哪家
- 高新區(qū)中國(guó)eCTD歡迎選購(gòu) 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊(cè)系統(tǒng) 2025-05-14
- 上?;瘜W(xué)藥品eCTD格式 2025-05-09
- 南京電子申報(bào)eCTD哪個(gè)品牌好 2025-05-09
- 太倉(cāng)NDAeCTD服務(wù)價(jià)格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 佛山xr虛擬拍攝 2025-06-14
- 常見(jiàn)互聯(lián)網(wǎng)數(shù)據(jù)服務(wù)共同合作 2025-06-14
- 東城區(qū)機(jī)架式服務(wù)器機(jī)箱 2025-06-14
- 南京教育電子白板價(jià)格 2025-06-14
- 北京靠譜的蜂蜜制品價(jià)格 2025-06-14
- 陽(yáng)江單位數(shù)據(jù)安全防護(hù)軟件 2025-06-14
- 新疆智慧工地咨詢報(bào)價(jià) 2025-06-14
- 虹口區(qū)在線式翹曲檢測(cè)操作 2025-06-14
- 無(wú)錫購(gòu)買智慧消防操作 2025-06-14
- 北京硬盤價(jià)格 2025-06-14