山西SAN HQ TF高鹽核酸酶70921
殘留的宿主DNA是生產(chǎn)中產(chǎn)生的雜質,,其存在潛在的致瘤性、傳染性和免疫原性等風險,。相關研究表明,,基因的大小普遍在200bp以上,因此大于200bp有可能會有一定的致病性,,而且殘留DNA片段越大,,生物制品的風險等級越高。因此,,各國監(jiān)管機構對其提出了嚴格要求,。美國食品藥品監(jiān)督管理局(FDA)在《關于人類基因zhiliao新產(chǎn)品生產(chǎn)指導文件》中明確指出HCD的片段要小于200bp。2022年5月,,國家藥品監(jiān)督管理局藥品評審中心(CDE)發(fā)布的《體內(nèi)基因藥物產(chǎn)品藥學研究與評價技術指導原則(試行)》中也明確指出需對DNA殘留量和殘留片段大小進行控制,,建議盡量將DNA殘留片段的大小控制在200bp以下,。ArcticZymes所有產(chǎn)品的開發(fā),、生產(chǎn)及銷售等都符合ISO13485:2016質量管理體系標準。山西SAN HQ TF高鹽核酸酶70921

ArcticZymes廠家對鹽活性核酸酶系列產(chǎn)品(Salt Active Nucleases,,SANs)的生產(chǎn)及質控,,包括SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶,在符合ISO13485:2016體系基礎上,,增加了cGMP質控標準,,如microbes、endotoxin,、蛋白酶等,;同時提供TSE/BSE聲明、無動物源(Animal-Origin Free)聲明,、非轉基因聲明等文件協(xié)助藥物申報,。此外,ArcticZymes的生產(chǎn)場地接受客戶的定期審計,,其第三方審計文件已得到國際TOP CDMO及Biotech的認可,,并已經(jīng)成為國際TOP CDMO的供應商。具體文件體系可以跟廠家或對應銷售人員聯(lián)系,。山西SAN HQ TF高鹽核酸酶70921致力于從深海微生物中識別新的冷適應酶,,用于分子研究、體外診斷和制藥領域,。
ArcticZymes Technologies成立于20世紀80年代后期,,致力于從海洋生物中識別新的冷適應酶,。ArcticZymes目標明確,推進分子研究,、診斷和therapeutics領域的發(fā)展,。30多年來,ArcticZymes只專注于酶學研究,,匯集一批志同道合的科學家,,在酶學領域追求zhuoyue、勇于創(chuàng)新,。ArcticZymes開發(fā)創(chuàng)新解決方案,,與客戶緊密協(xié)作,提升產(chǎn)品品質,,從高質量到zhuoyue,,達成他們的目標,重新定義生物藥生產(chǎn)的邊界,。在ArcticZymes,,我們精心設計解決方案,以從未出現(xiàn)的方式推動行業(yè)向前發(fā)展,。
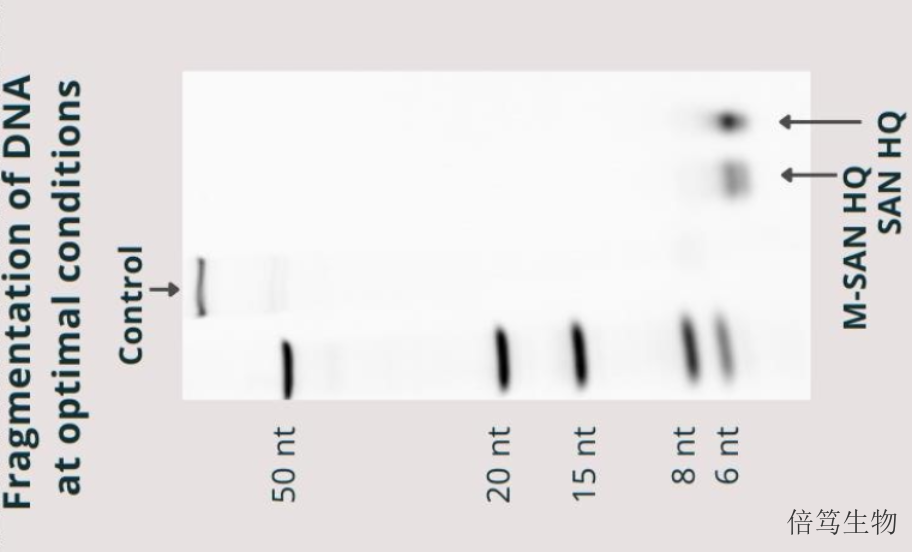
大規(guī)模生產(chǎn)階段,,AAV/LV載體生產(chǎn)流程跟抗體、疫苗類藥物的生產(chǎn)類似,,主要包含上游培養(yǎng),、下游純化及制劑部分。上游培養(yǎng)分為質粒開發(fā),、細胞擴增,、三質粒共轉染及病毒載體生產(chǎn)等步驟。下游純化分為細胞裂解釋放AAV病毒顆粒(可以通過去污劑,、機械作用,、高滲或凍融操作等)or收獲細胞上清液得到含LV病毒原液、加入核酸酶以減少宿主細胞核酸污染,、澄清是通過離心或過濾等方法去除細胞碎片和雜質等,、超濾濃縮以減少后續(xù)色譜純化體系、親合及離子交換等純化得到高純度病毒載體,。制劑部分主要是超濾更換緩沖液,、過濾除菌及制劑灌裝等。SAN HQ高鹽核酸酶更適合用于AAV生產(chǎn),。
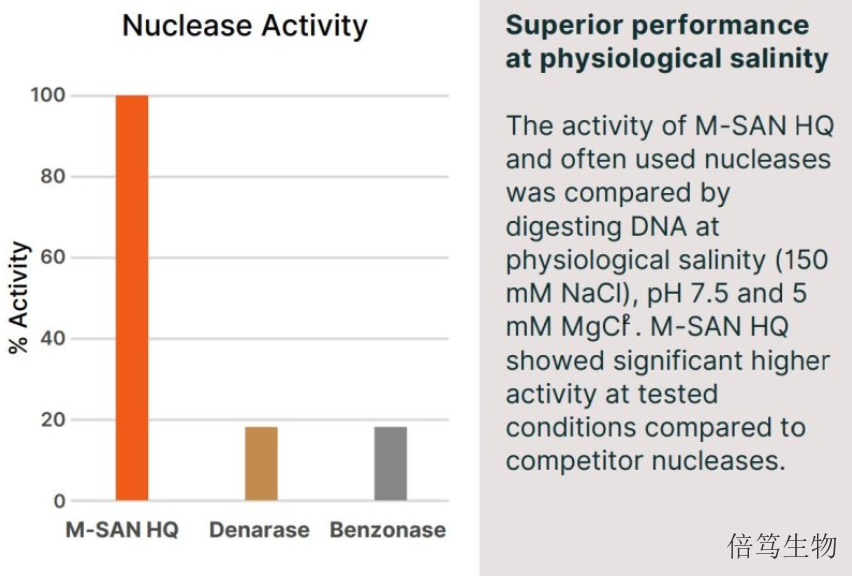
市售的SAN HQ高鹽核酸酶有三個規(guī)格,,分別是25kU、500kU及5MU,,分別滿足研發(fā)初期及大規(guī)模生產(chǎn)各階段的要求,。通過SDS-PAGE檢測蛋白純度在98%以上,。基于ArcticZymes Technologies的30年的酶學開發(fā)及大規(guī)模生產(chǎn)經(jīng)驗,,SAN HQ的生產(chǎn)體系穩(wěn)定,,產(chǎn)品純度高,批次一致性好,,無蛋白酶活性,。廠家開發(fā)出特異的緩沖液體系,使SAN HQ保存起來更加穩(wěn)定,,-15℃ - -30℃條件下有效期3年左右,。研究數(shù)據(jù)表明,經(jīng)過5-6次的反復凍融,,SAN HQ高鹽核酸酶活性沒有明顯變化,。SAN HQ提高核酸污染去除效率,同時提高目標產(chǎn)物產(chǎn)量,。江蘇高鹽條件高鹽核酸酶70921-150
在如抗體,、病毒載體藥物等的生產(chǎn)工藝流程中,核酸雜質的去除至關重要,。山西SAN HQ TF高鹽核酸酶70921
基因藥物常用的AAV載體有三種生產(chǎn)方法,,分別是三質粒瞬轉體系、桿狀病毒表達載體體系和包裝細胞體系,。其中,,20多年前開發(fā)的三質粒瞬轉表達技術仍然占據(jù)腺相關病毒AAV生產(chǎn)的主流地位,其三質粒分別是Helper質粒(含E2a/b,、E4和VARNA基因)、目標基因表達質粒及輔助質粒(含Cap和Rep基因),。雖然AAV病毒載體的血清型不同,,但AAV的生產(chǎn)流程基本一致,主要有質粒共轉宿主細胞HEK293,、293細胞生產(chǎn)病毒顆粒,、從細胞培養(yǎng)上清或/及細胞裂解液中收獲病毒載體、純化/制劑/無菌過濾/灌裝等流程,。山西SAN HQ TF高鹽核酸酶70921
上海倍篤生物科技有限公司是一家有著先進的發(fā)展理念,,先進的管理經(jīng)驗,在發(fā)展過程中不斷完善自己,,要求自己,,不斷創(chuàng)新,時刻準備著迎接更多挑戰(zhàn)的活力公司,,在上海市等地區(qū)的醫(yī)藥健康中匯聚了大量的人脈以及**,,在業(yè)界也收獲了很多良好的評價,,這些都源自于自身的努力和大家共同進步的結果,這些評價對我們而言是比較好的前進動力,,也促使我們在以后的道路上保持奮發(fā)圖強,、一往無前的進取創(chuàng)新精神,努力把公司發(fā)展戰(zhàn)略推向一個新高度,,在全體員工共同努力之下,,全力拼搏將共同上海倍篤生物科技供應和您一起攜手走向更好的未來,創(chuàng)造更有價值的產(chǎn)品,,我們將以更好的狀態(tài),,更認真的態(tài)度,更飽滿的精力去創(chuàng)造,,去拼搏,,去努力,讓我們一起更好更快的成長,!
- 湖北智能中鹽核酸酶銷售電話 2025-06-24
- 天津綜合中鹽核酸酶聯(lián)系方式 2025-06-24
- 海南進口中鹽核酸酶廠家直銷 2025-06-24
- 湖北需求高鹽核酸酶聯(lián)系方式 2025-06-24
- 青海哪些高鹽核酸酶價格表 2025-06-24
- 甘肅質量中鹽核酸酶 2025-06-24
- 云南中鹽核酸酶銷售電話 2025-06-24
- 陜西質量高鹽核酸酶哪家公司銷售 2025-06-24
- 遼寧質量高鹽核酸酶用途 2025-06-24
- 天津需求中鹽核酸酶聯(lián)系方式 2025-06-24
- 北京包含什么ELISA試劑盒電話多少 2025-06-24
- 西北醫(yī)療生物指示劑 2025-06-24
- 萊文DRG系統(tǒng)優(yōu)勢 2025-06-24
- 上?;瘜W遺傳技術哪家專業(yè) 2025-06-24
- 國產(chǎn)TOC檢測系統(tǒng) 2025-06-24
- 白喉桿菌CRM197代理商 2025-06-24
- 云南全腸道菌群檢測方式 2025-06-24
- 美容院艾灸機器人收費 2025-06-24
- FTM培養(yǎng)基配方 2025-06-24
- 南京25ml血清移液管型號 2025-06-24