河北等滲條件中鹽核酸酶70950
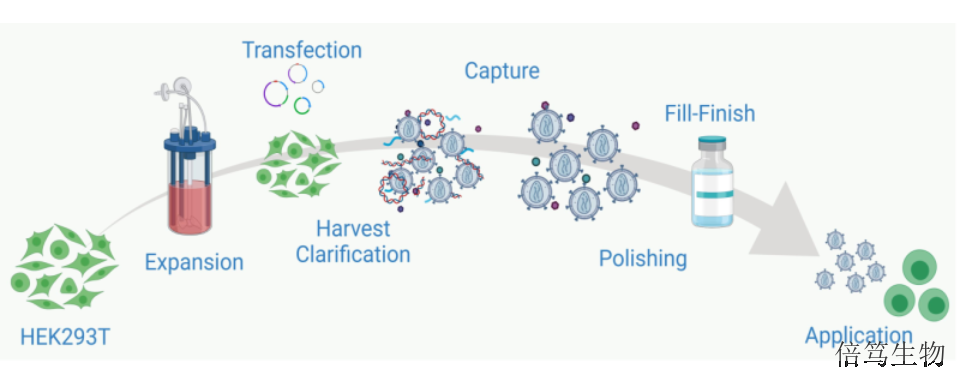
大規(guī)模生產(chǎn)階段,AAV/LV載體生產(chǎn)流程跟抗體,、疫苗類藥物的生產(chǎn)類似,,主要包含上游培養(yǎng)、下游純化及制劑部分,。上游培養(yǎng)分為質(zhì)粒開發(fā),、細(xì)胞擴增、三質(zhì)粒共轉(zhuǎn)染及病毒載體生產(chǎn)等步驟,。下游純化分為細(xì)胞裂解釋放AAV病毒顆粒(可以通過去污劑,、機械作用、高滲或凍融操作等)or收獲細(xì)胞上清液得到含LV病毒原液,、加入核酸酶以減少宿主細(xì)胞核酸污染,、澄清是通過離心或過濾等方法去除細(xì)胞碎片和雜質(zhì)等、超濾濃縮以減少后續(xù)色譜純化體系,、親合及離子交換等純化得到高純度病毒載體,。制劑部分主要是超濾更換緩沖液、過濾除菌及制劑灌裝等,。染色質(zhì)的雙螺旋結(jié)構(gòu)影響DNA的檢測與酶切處理,,而中鹽核酸酶降解染色質(zhì)效率更高。河北等滲條件中鹽核酸酶70950
病毒載體作為細(xì)胞藥物生產(chǎn)的關(guān)鍵原材料,,直接關(guān)系到細(xì)胞產(chǎn)品質(zhì)量,。載體質(zhì)量的控制和工藝穩(wěn)定性和批間一致性都是關(guān)系到產(chǎn)品能否產(chǎn)業(yè)化的關(guān)鍵。在生產(chǎn)純化過程中,,需要去除上游過程中的培養(yǎng)基成分,、誘導(dǎo)劑、宿主蛋白和核酸等雜質(zhì),,但是由于逆轉(zhuǎn)錄病毒顆粒比較大,,高異質(zhì)表面糖蛋白,而且活性易于受剪切影響,,對下游純化提出了巨大的挑戰(zhàn),。目前病毒載體純化方法包括超速離心、離子交換層析,、分子排阻層析,、親和層析、滲濾等。各種方法各有利弊,,就產(chǎn)業(yè)化而言,,離子交換純化效果比較好,條件易于摸索,,易于規(guī)模放大,。陜西ArcticZymes中鹽核酸酶70950M-SAN HQ中鹽核酸酶生產(chǎn)符合ISO 13485:2016規(guī)范,提供相關(guān)文件用于申報,。
ArcticZymes廠家對鹽活性核酸酶系列產(chǎn)品(Salt Active Nucleases,,SANs)的生產(chǎn)及質(zhì)控,包括SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶,,在符合ISO13485:2016體系基礎(chǔ)上,,增加了cGMP質(zhì)控標(biāo)準(zhǔn),如microbes,、endotoxin,、蛋白酶等;同時提供TSE/BSE聲明,、無動物源(Animal-Origin Free)聲明、非轉(zhuǎn)基因聲明等文件協(xié)助藥物申報,。此外,,ArcticZymes的生產(chǎn)場地接受客戶的定期審計,其第三方審計文件已得到國際TOP CDMO及Biotech的認(rèn)可,,并已經(jīng)成為國際TOP CDMO的供應(yīng)商,。具體文件體系可以跟廠家或?qū)?yīng)銷售人員聯(lián)系。
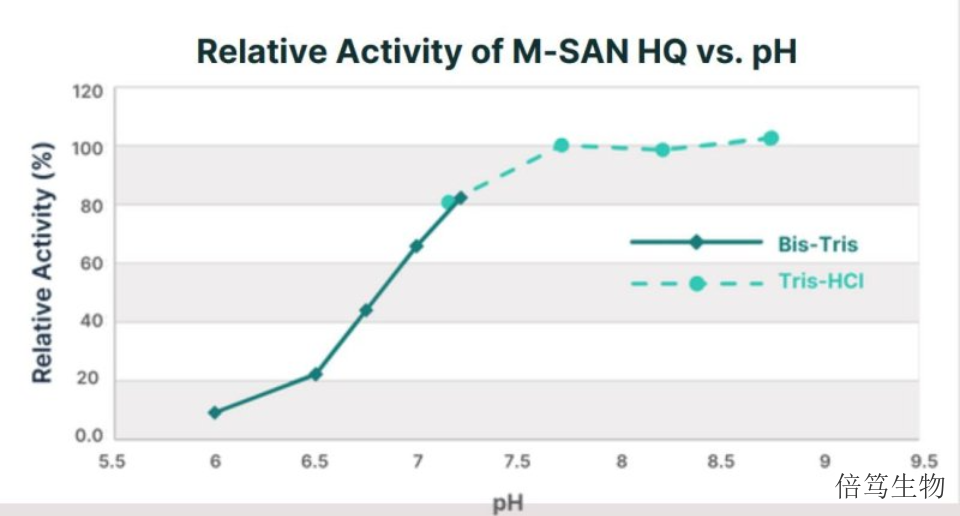
市售的M-SAN HQ中鹽核酸酶有三個規(guī)格,,分別是25kU,、500kU及5MU,分別滿足研發(fā)初期及大規(guī)模生產(chǎn)各階段的要求,。通過SDS-PAGE檢測蛋白純度在99%以上,。基于ArcticZymes Technologies的30年的酶學(xué)開發(fā)及大規(guī)模生產(chǎn)經(jīng)驗,,M-SAN HQ的生產(chǎn)體系穩(wěn)定,,產(chǎn)品純度高,批次一致性好,,無蛋白酶活性,。廠家開發(fā)出特異的緩沖液體系,使M-SAN HQ保存起來更加穩(wěn)定,,-15℃ - -30℃條件下保存4年沒有活性下降,。研究數(shù)據(jù)表明,經(jīng)過5-6次的反復(fù)凍融,M-SAN HQ中鹽核酸酶活性沒有明顯變化,。ArcticZymes的產(chǎn)品開發(fā),、生產(chǎn)、銷售和營銷過程均通過ISO13485質(zhì)量標(biāo)準(zhǔn)的認(rèn)證,。
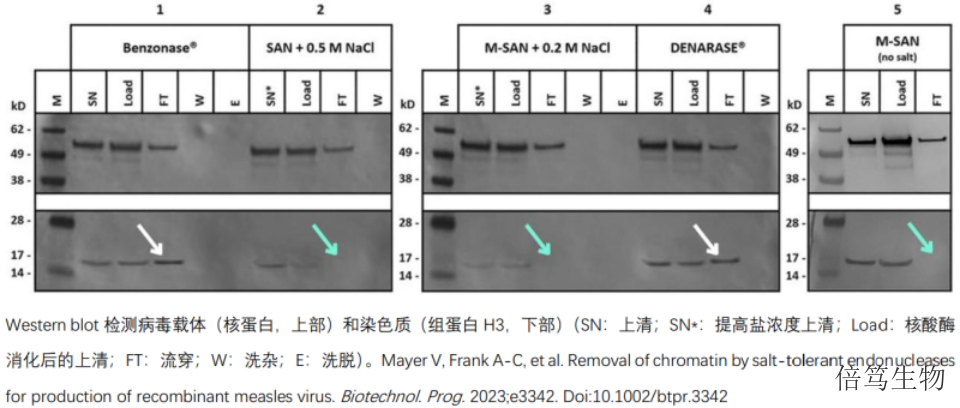
監(jiān)管部門對HCD的殘留量有明確的規(guī)定,。美國FDA發(fā)布的指導(dǎo)原則中指出生物制品HCD殘余限度為 100pg/劑,對于大劑量生物制品如單克隆抗體,,根據(jù)其殘留DNA來源及給藥途徑,,殘留量可放寬至 10ng/劑。細(xì)胞基因藥物終產(chǎn)品的DNA殘留有兩種來源,,分別是宿主細(xì)胞DNA(HCD)和轉(zhuǎn)染用的質(zhì)粒,。質(zhì)粒和HCD的存在形式不同,去除效率也差別很大,。其中,,質(zhì)粒是裸露的DNA雙鏈,帶強負(fù)電荷,,通過色譜純化主要是離子交換能夠很高效去除,;HCD則是以核小體緊密折疊形成的染色質(zhì)形式存在,幾乎不以裸DNA形式存在,,所以很難去除,。相比于全能核酸酶,在生理鹽條件下M-SAN HQ中鹽核酸酶將染色質(zhì)DNA剪切成更小片段的效率更高,。福建M-SAN HQ中鹽核酸酶70950
在150mM NaCl條件下,,M-SAN HQ中鹽核酸酶的酶切活性達(dá)到常規(guī)核酸酶的5倍左右。河北等滲條件中鹽核酸酶70950
ArcticZymes Technologies于2019年推出了M-SAN HQ中鹽核酸酶,,2021年推出對應(yīng)的M-SAN HQ ELISA kit,。該試劑盒原理是采用雙抗夾心法定量檢測各種生物制品的中間品、半成品和成品中M-SAN HQ中鹽核酸酶的殘留含量,,特異性的anti-M-SAN作為捕獲抗體偶聯(lián)在孔板上,,辣根過氧化酶HRP標(biāo)記anti-M-SAN作為檢測抗體,TMB是檢測反應(yīng)底物,。該試劑盒特異識別M-SAN HQ中鹽核酸酶,,對其它核酸酶沒有特異性結(jié)合。它的定量范圍是0.12-7.5ng/ml,;12*8strips的設(shè)計規(guī)格,,使用靈活,更能降低使用成本,。河北等滲條件中鹽核酸酶70950
- 四川效果中鹽核酸酶銷售電話 2025-06-24
- 湖北智能中鹽核酸酶銷售電話 2025-06-24
- 天津綜合中鹽核酸酶聯(lián)系方式 2025-06-24
- 江蘇在線中鹽核酸酶聯(lián)系方式 2025-06-24
- 海南進(jìn)口中鹽核酸酶廠家直銷 2025-06-24
- 湖北需求高鹽核酸酶聯(lián)系方式 2025-06-24
- 北京質(zhì)量高鹽核酸酶 2025-06-24
- 海南M-SAN HQ中鹽核酸酶銷售電話 2025-06-24
- 青海哪些高鹽核酸酶價格表 2025-06-24
- 河北貨號高鹽核酸酶用途 2025-06-24
- 黃浦區(qū)是什么醫(yī)療管理服務(wù)主題 2025-06-24
- 河南4K錄像醫(yī)用刻錄機生產(chǎn)廠家 2025-06-24
- 安徽培養(yǎng)基一次性生物耗材廠家價格 2025-06-24
- 河北全腸道菌群檢測哪家好 2025-06-24
- 江蘇太空艙按摩椅批發(fā)廠家 2025-06-24
- 成都洗鼻鹽批發(fā)價 2025-06-24
- 北京包含什么ELISA試劑盒電話多少 2025-06-24
- 四川效果中鹽核酸酶銷售電話 2025-06-24
- 廣東呼吸機醫(yī)療設(shè)備培訓(xùn)教育標(biāo)準(zhǔn) 2025-06-24
- 島津TOC總碳 2025-06-24