江西70950-202高鹽核酸酶
從國內(nèi)來看,,由于 AAV 基因藥物研發(fā)管線絕大部分集中在眼科遺傳病上,,載體用量較小,,三質(zhì)粒共轉(zhuǎn)染 AAV 系統(tǒng)足以滿足未來的臨床及商業(yè)需求,,因此,國內(nèi)的 AAV 生產(chǎn)系統(tǒng)主要以三質(zhì)粒為主,。然而,,考慮到未來 AAV 基因藥物在血液、神經(jīng)系統(tǒng),、肌肉系統(tǒng)等領(lǐng)域的臨床應(yīng)用,,三質(zhì)粒系統(tǒng)顯然難以勝任。如藥明生基從國外收購了 OXGENE 的輔助腺病毒 AAV 生產(chǎn)系統(tǒng) TESSA,,據(jù)報(bào)道較三質(zhì)粒系統(tǒng)有10倍的提升,;而基因藥物 CDMO 企業(yè)北京五加和基因則在國內(nèi)率先采用了陳海峰博士的威洛克公司授權(quán)的Bac-to-AAV 系統(tǒng),,憑借公司在病毒載體領(lǐng)域持續(xù)30年的研發(fā)經(jīng)驗(yàn),不斷摸索,、試驗(yàn),,終于在臨床級生產(chǎn)方面獲得了巨大的成功,為 AAV 基因藥物管線研發(fā)公司錦籃基因進(jìn)行多批次臨床 CDMO 代工生產(chǎn),。江蘇高鹽核酸酶哪家好呢,,歡迎咨詢上海倍篤生物 。江西70950-202高鹽核酸酶
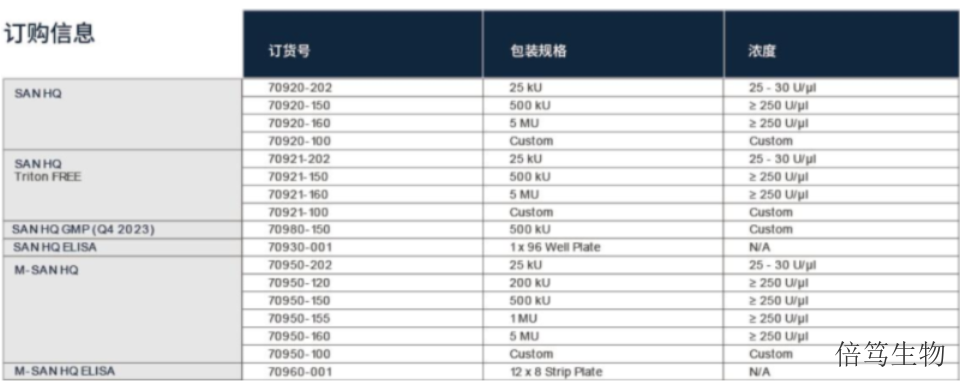
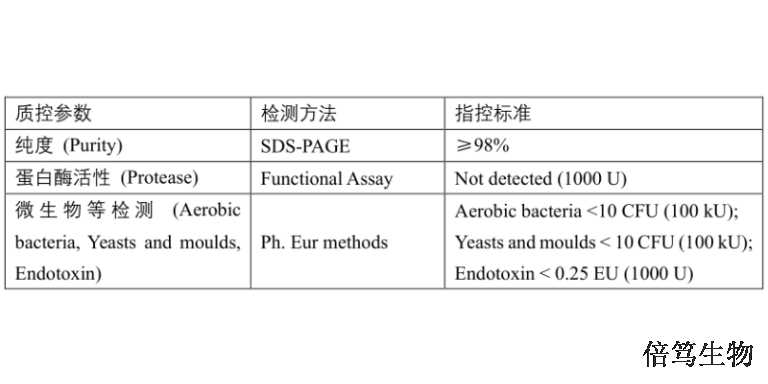
ArcticZymes廠家對鹽活性核酸酶系列產(chǎn)品(Salt Active Nucleases,,SANs)的生產(chǎn)及質(zhì)控,,在符合ISO13485:2016體系基礎(chǔ)上,增加了cGMP質(zhì)控標(biāo)準(zhǔn),,如microbes,、endotoxin、蛋白酶等,,符合USP-EP要求,。廠家提供HQ級別和GMP級別的SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶,,從成本角度分別滿足臨床前和早期臨床階段,、商業(yè)化大規(guī)模生產(chǎn)階段的需求;且GMP級SAN HQ高鹽核酸酶已完成在FDA的藥物主文件(Drug Master File, DMF)申報(bào)備案,,助力加快藥物申報(bào)流程,。山東特色高鹽核酸酶用途上海高鹽核酸酶產(chǎn)品質(zhì)量哪家好呢,歡迎咨詢上海倍篤生物 ,。
在抗體藥物及核酸藥物領(lǐng)域,,倍篤生物產(chǎn)品線涵蓋藥物研發(fā)的全流程,主要用——RNA轉(zhuǎn)染試劑,、生物活性物質(zhì)純化分離用填料產(chǎn)品,、ADC的payload抗體(如anti-DXD、anti-Eribulin,、anti-MMAE等),、動物造模用陽性及陰性抗體、泊洛沙姆P 188 Bio,、工藝雜質(zhì)及外源污染物殘留檢測產(chǎn)品,、抗體結(jié)構(gòu)域分析蛋白酶、蛋白聚糖分析水解酶等,,品牌有德國Genovis,、德國BASF、中國君研生物,、中國金傳生物,、中國毫厘科技,、中國再帆生物等。這些國產(chǎn)品牌都具有國內(nèi)自研,、自產(chǎn)能力,,批次生產(chǎn)穩(wěn)定可靠、品質(zhì)可控,,為行業(yè)發(fā)展提供更多國產(chǎn)選擇,。
核酸酶活性受到很多因素影響,如鹽濃度,、pH,、底物、溫度等,。因此,,不同客戶、不同項(xiàng)目中核酸酶的使用條件都不一樣,。目前,,生物制藥行業(yè)對Benonase全能核酸酶的使用比較熟悉,如生理鹽或低鹽濃度,、脫鹽操作等,。對于AdV/AAV等項(xiàng)目,使用SAN HQ高鹽核酸酶替代Benzonase時(shí),,只需提高反應(yīng)體系總鹽濃度到400mM-500mM即可,,溫度、Mg2+濃度等條件不用做任何調(diào)整,,同樣酶量的SAN HQ對宿主細(xì)胞DNA(HCD)的去除效果更好,、病毒載體得率更高。經(jīng)過工藝優(yōu)化后,,可以將SAN HQ高鹽核酸酶的用量減少到原來的1/3-1/4,,且HCD去除效果及產(chǎn)品得率更高。SAN HQ高鹽核酸酶在鹽濃度400-650mM條件下活性達(dá)到峰值,。
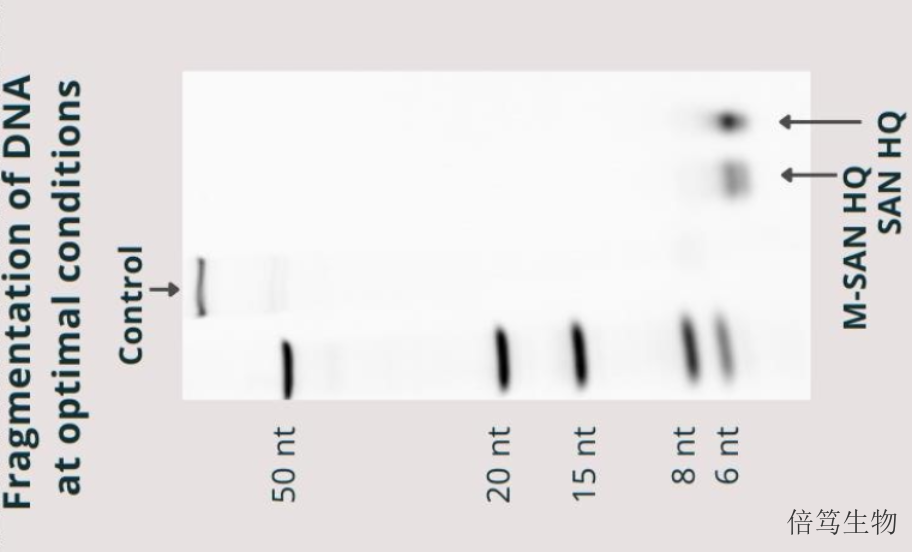
一個美國客戶做了對照實(shí)驗(yàn),,比較Benzonase和SAN HQ高鹽核酸酶純化病毒載體的效率。實(shí)驗(yàn)設(shè)計(jì)如下,,HEK293細(xì)胞轉(zhuǎn)染及培養(yǎng)后,,分別取了150Million的293細(xì)胞進(jìn)行裂解,分別在各自適宜的條件下(即SAN HQ組反應(yīng)條件為500mM鹽濃度,,而Benzonase組反應(yīng)條件是150mM鹽濃度)加入等量的酶(0,、2kU、3kU,、4kU,、5kU,、6kU),37°孵育1hr,,加入Picogreen染料后檢測DNA的殘留量,。結(jié)果發(fā)現(xiàn),SAN HQ高基因療法制造商面臨的挑戰(zhàn)與抗體療法剛出現(xiàn)時(shí)單克隆抗體制造商面臨的挑戰(zhàn)相似,。例如,,在生產(chǎn)、儲存和處理過程中,,單克隆抗體也會受到低滴度,、產(chǎn)品和工藝相關(guān)雜質(zhì)和降解的挑戰(zhàn)。盡管與重組單克隆抗體相比,,單劑量AAV產(chǎn)品與工藝相關(guān)雜質(zhì)相關(guān)的風(fēng)險(xiǎn)可能更低(取決于雜質(zhì)的類型,、劑量和給藥途徑),但這也不能忽視,。由于這些相似性,,制藥商、化學(xué)品和輔料供應(yīng)商有機(jī)會進(jìn)行合作,,并開發(fā)創(chuàng)新的解決方案,,以實(shí)現(xiàn)穩(wěn)健和成本效益高的AAV產(chǎn)品生產(chǎn)。鹽核酸酶組用更少的酶得到了更好的去除效果(即2kU的SAN HQ消化結(jié)果明顯優(yōu)于6kU的Benzonase),,且SAN HQ的高純化效率是非血清型依賴的,。南京高鹽核酸酶售后服務(wù)哪家好呢,,歡迎咨詢上海倍篤生物 ,。淮安70921-160高鹽核酸酶銷售電話
無錫高鹽核酸酶售后服務(wù)哪家好呢,,歡迎咨詢上海倍篤生物 ,。江西70950-202高鹽核酸酶
近年來,AAV在cancer疾病的醫(yī)治中顯示出巨大的價(jià)值,。AAV作為基因藥物的載體已在肺,、肝、眼,、腦,、肌肉等多個臨床試驗(yàn)(超過100次)中得到應(yīng)用,并在盲癥和血友病方面取得了巨大成功,。2012年,,AAV1載體編碼的脂蛋白脂肪酶成為歐盟批準(zhǔn)的shou個用于醫(yī)治脂蛋白脂肪酶缺乏癥的基因產(chǎn)物(Glybera)。5年后,,另一種AAV介導(dǎo)的基因藥物(Luxturna)隨后獲準(zhǔn)在美國上市,?;贏AV9的基因療(Zolgensma)也被用于醫(yī)治脊髓性肌肉萎縮。腺病毒在基礎(chǔ)和實(shí)驗(yàn)研究有這么強(qiáng)的生命力原因在于:宿主范圍廣,,對人致病率低,;腺病毒粒子相對穩(wěn)定,病毒基因重排頻率低,;安全性高,,不整合到染色體中,無插入致病基因,,不干擾其他宿主基因,。江西70950-202高鹽核酸酶
- 河南70950-202高鹽核酸酶用途 2025-06-23
- 重慶倍篤生物中鹽核酸酶量大優(yōu)惠 2025-06-23
- 湖南特色中鹽核酸酶價(jià)格表 2025-06-23
- 天津哪些中鹽核酸酶廠家直銷 2025-06-23
- 河南倍篤生物高鹽核酸酶用途 2025-06-23
- 天津哪些中鹽核酸酶聯(lián)系方式 2025-06-23
- 江蘇70950-202高鹽核酸酶 2025-06-23
- 山西質(zhì)量中鹽核酸酶價(jià)格表 2025-06-23
- 湖北70950-202中鹽核酸酶用途 2025-06-23
- 重慶國內(nèi)中鹽核酸酶哪家公司銷售 2025-06-23
- 先端子午流注 2025-06-23
- 松江區(qū)醫(yī)藥ASAP技術(shù)穩(wěn)定性預(yù)測 2025-06-23
- 婦科手術(shù)床采購 2025-06-23
- 佳木斯中醫(yī)穴位針灸實(shí)訓(xùn)教學(xué)系統(tǒng) 2025-06-23
- 中醫(yī)院艾灸儀24小時(shí)服務(wù) 2025-06-23
- 大腸腸道菌群檢測方式 2025-06-23
- 甘肅假肢廠商 2025-06-23
- 華東補(bǔ)牙水門汀用法 2025-06-23
- 國產(chǎn)全自動核酸提取儀 2025-06-23
- 福建專業(yè)的病理實(shí)驗(yàn)外包推薦 2025-06-23