�Ϻ�NDAeCTD�l(f��)��ܛ�� ֵ����ه �x���Ƽ�����(y��ng)
�l(f��)؛���c���㽭ʡ������
�l(f��)���r�g��2025-04-23
�l(f��)؛���c���㽭ʡ������
�l(f��)���r�g��2025-04-23
eCTD��C��(bi��o)��(zh��n)�ć�(y��n)�����c����W�ˌ�eCTD����CҪ��֞顰�e�`�������桱�͡���ʾ��Ϣ������,�����С��e�`���ֱ�ӌ�(d��o)����ܡ���C�Ŀ���w�����149�l�������ļ�����Ҏ(gu��)������·���L�����ƣ�,��PDF���x�ԣ���ֹ�ܴa���o(h��)����XML�Ǽ��ļ������Ե�,������,���ļ��U(ku��)չ����횷���Ҏ(gu��)������.xpt�����R����(sh��)��(j��)���������ļ��A�Ӽ�������Ŀ䛻��ϴ���ļ�,�����^���Ї�����������C��(bi��o)��(zh��n)���ĺ����棨54�l��,���W�˵���C�wϵ�����(f��)�s���w�F(xi��n)����ߘ�(bi��o)��(zh��n)�ļ��g(sh��)�O(ji��n)��,����DMFע��������P(gu��n)���g(sh��)֧��,���Ϻ�NDAeCTD�l(f��)��ܛ��
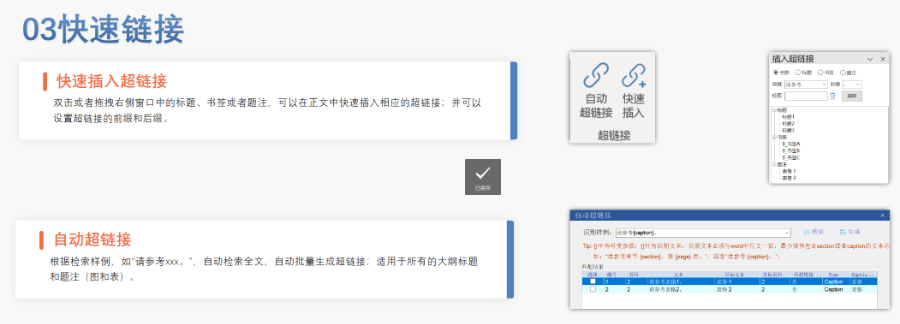
���g(sh��)�ډ��c�d�Ј�����(zh��n) ���͖|�ρ������ɼ{eCTD������IT���A(ch��)�O(sh��)ʩ������(d��o)��ʩ�M(j��n)�Ȝ���,���W��ͨ�^��eCTDȫ���h���ṩ���g(sh��)Ԯ��,�������d�Ј�������C�wϵ����Ӗ(x��n)�����,����ˎ����ᘌ���ͬ�^(q��)�����f������,��������ģ�K1���ӱ��ط�(w��n)���Ԕ�(sh��)��(j��)�� �O(ji��n)�ܿƌW(xu��)�c��(chu��ng)���� eCTD֧���挍�����C��(j��)��RWE�����m��(y��ng)���R��ԇ��O(sh��)Ӌ������,�����ل�(chu��ng)ˎ����,��EMA��PRIMEӋ����ͻ���ԯ����ṩeCTD����ͨ�������S���A���ύģ�K��(sh��)��(j��),����ˎ�̓���ˎ��eCTD���п������M�Üp��̓�(y��u)�Ȍ��u,�� ����(y��ng)朰�ȫ�c��Ӌۙ eCTD��XML�����ļ�ӛ������ύ�汾��֧�ֹ���(y��ng)朆��}���ݷ�����ԭ��ˎCEP�������輰�r��׃����Ϣ,���_�������Ƅ��S�̫@ȡ��(sh��)��(j��),���^(q��)�K朼��g(sh��)ԇ�c����ۙeCTD��(sh��)��(j��)������ֹ�۸ĺ�δ�ڙ�(qu��n)�L��,�� �Ļ���c��ʩ�ϵK �����ϚW����ƫ�Â��y(t��ng)���|(zh��)����,����(d��o)��eCTD�ƏV�����^��EMAͨ�^���Z�N��Ӗ(x��n)���Ϻͅ^(q��)��f(xi��)�{(di��o)�T�ƶȴ��M(j��n)�Ļ��m��(y��ng),���ИI(y��)���{(di��o)������˼�S,����eCTD�ġ���Ҏ(gu��)ؓ(f��)��(d��n)���D(zhu��n)���顰������(y��u)�ݡ������KeCTD����(w��)���Ŀɿ�����ESG����ύͨ����Ո���P(gu��n)���g(sh��)֧��,��
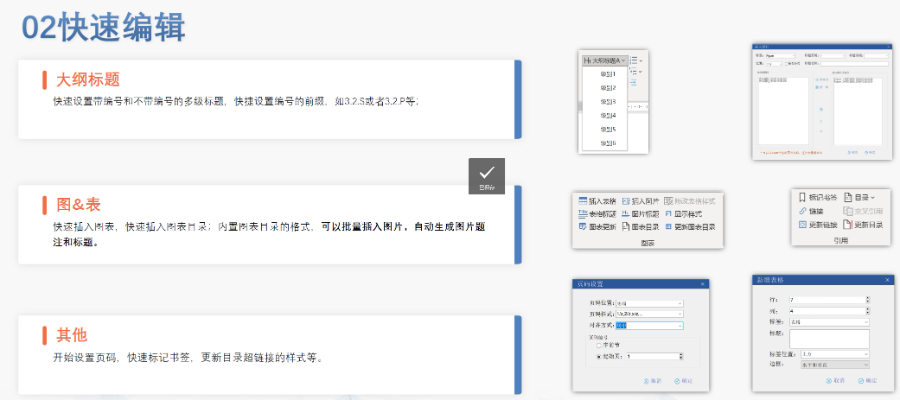
ANDAһ�㲻��Ҫ�ṩ�R��ǰ��������R�������w����(sh��)��(j��)���C���䰲ȫ�Ժ���Ч�ԣ����ⶾ�����R����,�������������Ո�˱�횺����C����a(ch��n)Ʒ�cԭ��ˎ����������Ч��,�� ���ա�(li��n)��ʳƷ,��ˎƷ�ͻ��yƷ������ 505��j����Ҫ�M��FDA�f����ՈANDA��ˎƷ��������l���� ����ˎ�������FDA����(j��ng)�^�t(y��)����ͬ���u�r����(zh��n)��ˎƷ�����Q"��Ƥ��"��������,����FDA�x����RLD/RS�M(j��n)�Ќ��շ���; ���Գɷ�,�����͡�Ҏ(gu��)��,���oˎ;��,���m��(y��ng)�Y��Ҫ�cRLD��ͬ,�� ����ˎ����C���cRLD������Ч���ϵ�ͬ,�������������Ч�ԣ� ��횰�������(li��n)�������21 CFR����ˎƷ���a(ch��n)����Ҏ(gu��)���������a(ch��n)�^��,�� �oՓ�Ї�߀������,��Ҫ�����ˎ���|(zh��)����횵�ͬ�����Ǹ��څ����Ƅ��ģ��@�ǫ@���Ļ���Ҫ�c,�� ע�⣺���ԭ��ˎδ���О�RLD,����Ո�˿������������FDA��Ո,��
ANDA�f���� ����ICH M4��CTD��ʽ�����Y��,������eCTD��ʽ�f���� ͨ�^ESGͨ���f���Y��,�� �յ�CDER��letter,���f���Y���ѽ�(j��ng)�M(j��n)��FDA��(sh��)��(j��)�죻 ��GDUFA�M,�����Y���f�����10�Ճ�(n��i)���~�� ANDA���գ� �U�M��F(xi��n)DA���������Y�ϵ�������,��������60��o����(f��),�� ��һ�N��r��ANDA�oȱ�ݣ�F(xi��n)DA�o��Ո�˰l(f��)�����ţ�Acceptance Letter��,�� �ڶ��N��r��ANDA��������10��Сȱ��,��F(xi��n)DA����ͨ�^�Ԓ������,������]���ȷ�ʽ֪ͨ�l(f��)��IR (��ϢՈ��),����Ո����7���՚v�Ճ�(n��i)��������δ���r�a��������Ҫ���Y��,��F(xi��n)DA������ԓANDA,�� �����N��r��ANDA����1�����߶����ش�ȱ�ݣ���10�����ϵ�Сȱ��,��F(xi��n)DA������ԓANDA,�� ע������@߅�����գ�ֻ��75%���M��,���Ĵ�������eCTD������P(gu��n)���g(sh��)֧��,��
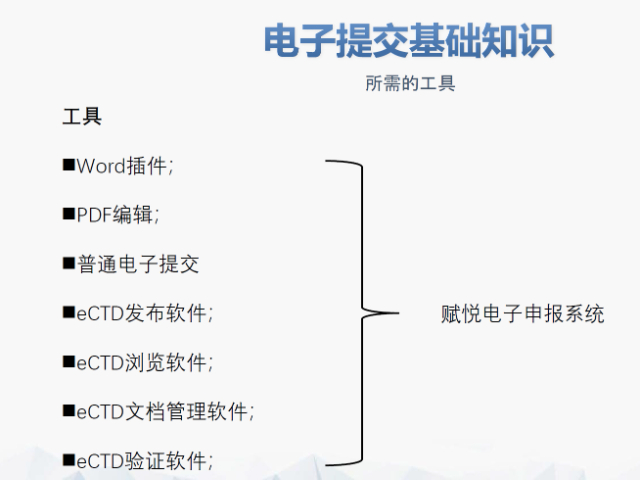
�Ї����M(j��n)һ���c���H��܉�����M(j��n)eCTD�Ș�(bi��o)��(zh��n)��(y��ng)��,�����ˎƷע��Ч�ʺ��|(zh��)��,��AI���g(sh��)������ˎƷע���I(l��ng)��V����(y��ng)�ã����o�����u�ˆT����,��δ��ˎƷע���Y�ό���ע�ؽY(ji��)��(g��u)����(sh��)��(j��),�������ڱO(ji��n)�ܙC(j��)��(g��u)��Ч�@ȡ�����Ô�(sh��)��(j��)�� eCTD�Ȕ�(sh��)�ֻ����ߌ��Ƅ�ˎƷ�O(ji��n)�����ǻ۱O(ji��n)�ܺ�ȫ�������ڱO(ji��n)�ܰl(f��)չ,����߱O(ji��n)��Ч�ʺ��|(zh��)��,���^(q��)�K朼��g(sh��)���Б�(y��ng)��ǰ�����ɘ�(g��u)��ȫ��y(t��ng)һ��ˎƷ���(sh��)��(j��)ƽ�_,����(sh��)��(j��)���r��,��ˎƷע���I(l��ng)��?q��)���ע�ؔ?sh��)��(j��)�ռ�������������,����O(ji��n)�ܙC(j��)��(g��u)����I(y��)�ṩ�Q��֧��,�� ������֮��չ��δ��,���S��eCTD��ˎƷע���I(l��ng)��ďV����(y��ng)�úͲ���l(f��)չ,���Ї����������c���H��܉��ˎƷע���wϵ���@������������Ї�ˎƷע�Ե�Ч�ʺ��|(zh��)��,���Ƅ��Ї�ˎƷ�����������_,��ͬ�r����I(y��)Ҳ��Ҫ�����P(gu��n)ע���g(sh��)�l(f��)չ�ӑB(t��i)�ͱO(ji��n)������׃�������r�{(di��o)�������(zh��n)�Ժ�Ҏ(gu��)��,�����m��(y��ng)δ�����Ј������ͱO(ji��n)��Ҫ��,���W��NDAע��������P(gu��n)���g(sh��)֧�֡��㽭INDeCTDע��ϵ�y(t��ng)
���ô�eCTD���ܛ�����P(gu��n)���g(sh��)֧��,���Ϻ�NDAeCTD�l(f��)��ܛ��
���h��Q�c���ɾȝ�(j��) ����Ո�ˌ����u�Y(ji��)���Ю��h,������EMA��CHMP��Ո�،��飬���ښW�˷�Ժ���������V�A,��eCTD�������ύӛ䛿����鷨���C��(j��),���C����Ո�������к�Ҏ(gu��)�x��(w��)��EDQM�O(sh��)���ٲ�ί�T��,��̎��CEP�����еļ��g(sh��)���h,�� �ИI(y��)څ���c������� ȫ��eCTD����(w��)�Ј������L���_(d��)12%���W��ռ��(j��)35%���~,����Ҫ����(w��)�̰���PharmaLex,��Certara�ȡ��^��ˎ��ͨ�^�Խ�IT�F(tu��n)��ͳɱ�,������С����I(y��)��ه����Ԍ�ע�аl(f��),���˹����ܣ�AI�����ļ��Ԅ����ɺ͌��u��Ҋ�A(y��)�y�еđ�(y��ng)����u���ࡣ ���߅��c�c�������� EMAͨ�^���_eCTDժҪ����ģ�K2.5�R����Ҫ���������u����,�����߽M�����ύ��ҊӰ푌��u�Q��,�����ֳɆT��Ҫ��ģ�K1���������Z�汾�f��������������ˎ������,��δ��,��eCTD4.0��֧��ֱ��朽ӻ��߷���ƽ�_�����F(xi��n)ȫ�������ڻ���,���Ϻ�NDAeCTD�l(f��)��ܛ��
 �Ϻ�ԭ��ˎeCTD����(w��)���Ŀɿ� ����(w��)���� �x���Ƽ�����(y��ng)
�Ϻ�ԭ��ˎeCTD����(w��)���Ŀɿ� ����(w��)���� �x���Ƽ�����(y��ng)
���h
 �㽭����ˎeCTDע��ϵ�y(t��ng) �\�Ž�(j��ng)�I �x���Ƽ�����(y��ng)
�㽭����ˎeCTDע��ϵ�y(t��ng) �\�Ž�(j��ng)�I �x���Ƽ�����(y��ng)
���h
 �Ϻ�ANDAeCTD����(y��ng)�� �\�ŷ���(w��) �x���Ƽ�����(y��ng)
�Ϻ�ANDAeCTD����(y��ng)�� �\�ŷ���(w��) �x���Ƽ�����(y��ng)
���h
 �|������eCTD �N�ķ���(w��) �x���Ƽ�����(y��ng)
�|������eCTD �N�ķ���(w��) �x���Ƽ�����(y��ng)
���h
 ����CDE eCTD���ý�Q���� ����(w��)���� �x���Ƽ�����(y��ng)
����CDE eCTD���ý�Q���� ����(w��)���� �x���Ƽ�����(y��ng)
���h