江蘇eCTD服務(wù)商
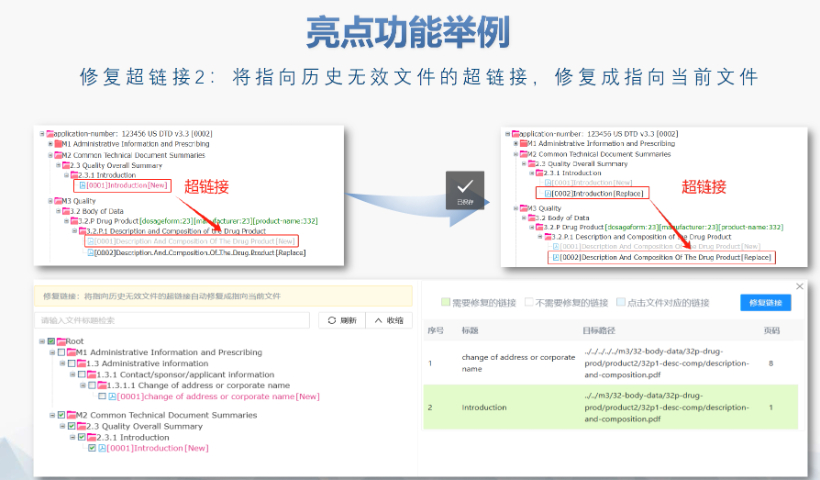
電子遞交的合規(guī)性與風(fēng)險管理 歐盟要求申請人確保電子資料與紙質(zhì)版本完全一致,,若未在規(guī)定時間提交紙質(zhì)文件可能導(dǎo)致注冊終止,。驗證過程中,“錯誤”級別問題(如文件命名不規(guī)范、XML邏輯錯誤)必須修正,,而“警告”和“提示信息”則建議優(yōu)化以提升審評體驗,。EDQM和EMA均提供驗證工具,申請人需在遞交前完成內(nèi)部預(yù)驗證,。 官方費用結(jié)構(gòu)與支付流程 歐盟eCTD遞交費用因?qū)徳u程序類型而異:集中程序費用較高,,涵蓋科學(xué)評估和合規(guī)審查成本;國家程序費用由各成員國自行設(shè)定,。CEP申請需向EDQM支付評審費,,具體金額根據(jù)原料藥類型和變更復(fù)雜度分級。繳費需通過官方指定渠道完成,,并附上付款憑證作為模塊1的組成部分,。 多語言支持與翻譯要求 盡管歐盟允許使用英語提交,但部分成員國要求模塊一的行政文件翻譯為本地語言,。臨床試驗數(shù)據(jù)庫(如SDTM和ADaM)需以英語呈現(xiàn),,同時提供雙語標(biāo)簽以支持多國審閱。專業(yè)翻譯服務(wù)在確保技術(shù)術(shù)語準(zhǔn)確性方面至關(guān)重要,,尤其針對復(fù)雜藥學(xué)和非臨床數(shù)據(jù),。瑞士IND注冊申報相關(guān)技術(shù)支持。江蘇eCTD服務(wù)商
美國藥物主文件(Drug Master File, DMF)是向FDA提交的機(jī)密技術(shù)文件,,用于支持藥品生產(chǎn),、質(zhì)量控制及合規(guī)性審查。以下為申報的要點和流程總結(jié): DMF概述與類型 ?定義與作用 DMF是藥品生產(chǎn)全過程的詳細(xì)檔案,,包含原料藥,、輔料、包裝材料等的生產(chǎn)設(shè)施,、工藝,、質(zhì)量控制等信息,供制劑廠商引用以支持其注冊申請,。其意義在于保護(hù)企業(yè)機(jī)密的同時,,滿足FDA對供應(yīng)鏈透明度的要求。 ?DMF類型 ?Ⅱ類:原料藥,、中間體及制劑(如微生物外泌體,、細(xì)胞株等生物制品均屬此類)。 ?Ⅲ類:包裝材料,。 ?Ⅳ類:輔料,、著色劑等添加劑。 ?Ⅴ類:非臨床/臨床數(shù)據(jù)等特殊信息(需FDA預(yù)先批準(zhǔn)),。 注:Ⅰ型(生產(chǎn)設(shè)施與人員)已于2000年停用,。無錫中國eCTD銷售電話瑞士NDA注冊申報相關(guān)技術(shù)支持,。
美國eCTD的強(qiáng)制實施時間與范圍:美國自2017年5月5日起要求藥申請(NDA)、仿制藥申請(ANDA)和生物制品許可申請(BLA)必須通過eCTD格式提交,,2018年5月5日進(jìn)一步擴(kuò)展至臨床試驗申請(IND)和藥品主文件(DMF),。FDA通過《聯(lián)邦食品、藥品和化妝品法案》第745A條明確電子提交的強(qiáng)制性,,豁免非商業(yè)化IND和部分DMF類型(如Ⅲ類),。2023年數(shù)據(jù)顯示,F(xiàn)DA接收的eCTD申請占比已達(dá)92%,,標(biāo)志著電子化審評體系的成熟,。企業(yè)若未按規(guī)范提交(如缺少文件或重復(fù)序列號),將直接被拒收,。
2020年暴發(fā)后,,F(xiàn)DA進(jìn)一步推動電子化進(jìn)程,例如允許遠(yuǎn)程電子簽章和臨時放寬部分格式要求,,但驗證標(biāo)準(zhǔn)(如PDF版本,、書簽鏈接有效性)并未降低。這一時期的實踐為eCTD在緊急審批中的靈活性提供了案例,,也凸顯了其作為危機(jī)應(yīng)對工具的價值,。 盡管美國尚未部署eCTD V4.0,但其技術(shù)方向已明確:支持醫(yī)療器械和保健品申報,、增強(qiáng)數(shù)據(jù)可復(fù)用性,、優(yōu)化審評系統(tǒng)與人工智能的集成。此外,,區(qū)塊鏈技術(shù)在電子簽章和數(shù)據(jù)溯源中的應(yīng)用探索,,可能成為下一階段升級的重點澳大利亞ANDA注冊申報相關(guān)技術(shù)支持,。
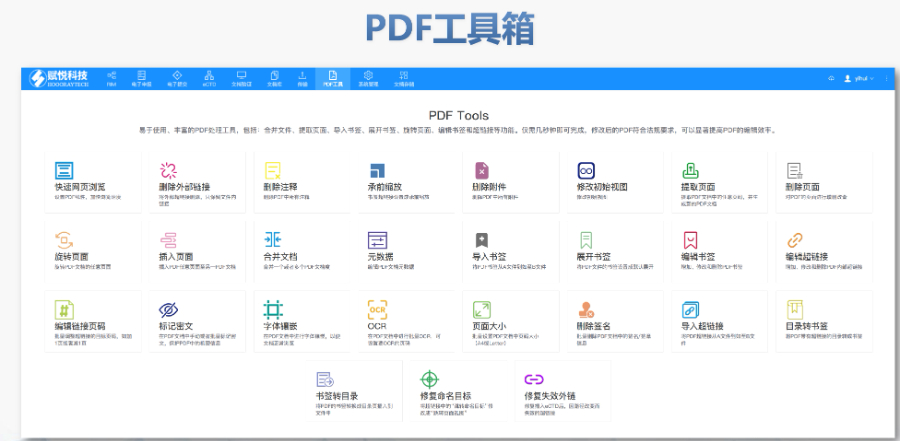
eCTD的技術(shù)架構(gòu)與模塊要求:美國eCTD基于XML技術(shù),,嚴(yán)格遵循ICH M4框架,分為5個模塊:模塊1(地區(qū)行政信息),、模塊2(技術(shù)總結(jié)),、模塊3-5(質(zhì)量、非臨床與臨床數(shù)據(jù)),。其中,,模塊1需包含F(xiàn)DA特定的文件,涵蓋申請編號,、聯(lián)系人和DMF授權(quán)書等行政信息,。模塊2-5需與ICH CTD全球統(tǒng)一標(biāo)準(zhǔn)一致,但FDA對文件顆粒度要求更細(xì),,例如非臨床研究報告需拆分并標(biāo)記Study ID,。PDF文件需符合FDA v4.1格式規(guī)范,,包括字體嵌入、書簽層級和超鏈接功能,。美國IND注冊申報相關(guān)技術(shù)支持,。江蘇中國eCTD使用
瑞士DMF注冊申報相關(guān)技術(shù)支持。江蘇eCTD服務(wù)商
澳大利亞的藥品電子通用技術(shù)文檔(eCTD)注冊申報體系是澳大利亞y藥品商品管理局(TGA)推動藥品審評現(xiàn)代化的重要舉措,。eCTD作為國際通行的電子化注冊申報標(biāo)準(zhǔn),,通過結(jié)構(gòu)化數(shù)據(jù)格式(如XML)整合了藥品質(zhì)量、安全性和有效性的技術(shù)文檔,,實現(xiàn)了從傳統(tǒng)紙質(zhì)遞交向數(shù)字化流程的轉(zhuǎn)型,。根據(jù)TGA要求,eCTD需遵循通用技術(shù)文檔(CTD)框架,,分為五個模塊:模塊1包含澳洲特定的行政信息(如產(chǎn)品說明書草案和GMP證明),;模塊2為質(zhì)量、非臨床及臨床研究的綜述與總結(jié),;模塊3至模塊5則分別涵蓋藥學(xué),、非臨床和臨床的詳細(xì)數(shù)據(jù)。澳大利亞自2024年起加速推進(jìn)eCTD實施,,要求創(chuàng)新藥注冊申報優(yōu)先采用該格式,,以提升審評效率并支持全球同步申報。 申報流程上,,企業(yè)需通過TGA指定的電子提交門戶(如eSubmission Gateway)上傳eCTD序列,,并在受理后5個工作日內(nèi)同步提交紙質(zhì)版模塊1-5資料。江蘇eCTD服務(wù)商
賦悅科技(杭州)有限責(zé)任公司是一家有著雄厚實力背景,、信譽可靠,、勵精圖治、展望未來,、有夢想有目標(biāo),,有組織有體系的公司,堅持于帶領(lǐng)員工在未來的道路上大放光明,,攜手共畫藍(lán)圖,,在浙江省等地區(qū)的數(shù)碼、電腦行業(yè)中積累了大批忠誠的客戶粉絲源,,也收獲了良好的用戶口碑,,為公司的發(fā)展奠定的良好的行業(yè)基礎(chǔ),也希望未來公司能成為*****,,努力為行業(yè)領(lǐng)域的發(fā)展奉獻(xiàn)出自己的一份力量,,我們相信精益求精的工作態(tài)度和不斷的完善創(chuàng)新理念以及自強(qiáng)不息,斗志昂揚的的企業(yè)精神將**賦悅科技供應(yīng)和您一起攜手步入輝煌,,共創(chuàng)佳績,,一直以來,,公司貫徹執(zhí)行科學(xué)管理、創(chuàng)新發(fā)展,、誠實守信的方針,,員工精誠努力,協(xié)同奮取,,以品質(zhì),、服務(wù)來贏得市場,我們一直在路上,!
- 高新區(qū)中國eCTD歡迎選購 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊系統(tǒng) 2025-05-14
- 上?;瘜W(xué)藥品eCTD格式 2025-05-09
- 南京電子申報eCTD哪個品牌好 2025-05-09
- 太倉NDAeCTD服務(wù)價格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 清遠(yuǎn)檔案自動化修圖軟件售價 2025-06-09
- 南昌3D虛擬人服務(wù)商 2025-06-09
- 重慶本地蜂蜜 2025-06-09
- 飛騰加固筆記本加固計算機(jī)供應(yīng)商 2025-06-09
- 廣東國產(chǎn)電腦維修怎么用 2025-06-09
- 黃浦區(qū)網(wǎng)絡(luò)營銷企劃一體化 2025-06-09
- 房山區(qū)不銹鋼機(jī)箱生產(chǎn)廠家 2025-06-09
- 江寧區(qū)高科技iOSAPP開發(fā) 2025-06-09
- 硬件資源優(yōu)化GOPT工程驗證平臺 2025-06-09
- 倉儲RFID智能貨架 2025-06-09