中國香港INDeCTD
設(shè)施費(fèi)動(dòng)態(tài)調(diào)整 API工廠和制劑工廠年費(fèi)分別約6.8萬和14.5萬美元(2025財(cái)年),,CMO工廠費(fèi)用為制劑費(fèi)的24%。國外工廠需額外支付1.5萬美元跨境檢查費(fèi),。 ?繳費(fèi)時(shí)限與懲罰 費(fèi)用需在財(cái)年首日(10月1日)起20天內(nèi)繳納,,逾期將列入拖欠名單并暫停ANDA受理,,涉事藥品視為冒牌產(chǎn)品。 ?豁免與特殊情形 PET藥物,、非商業(yè)產(chǎn)品及停產(chǎn)超一年的工廠可豁免繳費(fèi),。已繳費(fèi)工廠若年度內(nèi)無生產(chǎn)活動(dòng),仍需繳納費(fèi)用,。 ?行業(yè)影響與策略 費(fèi)用上漲推動(dòng)企業(yè)優(yōu)化申報(bào)策略,,例如集中ANDA提交周期、采用CMO外包降低設(shè)施費(fèi),,并通過預(yù)認(rèn)證(如DMF完整性評(píng)估)減少重復(fù)支出,。 澳大利亞IND注冊(cè)申報(bào)相關(guān)技術(shù)支持。中國香港INDeCTD
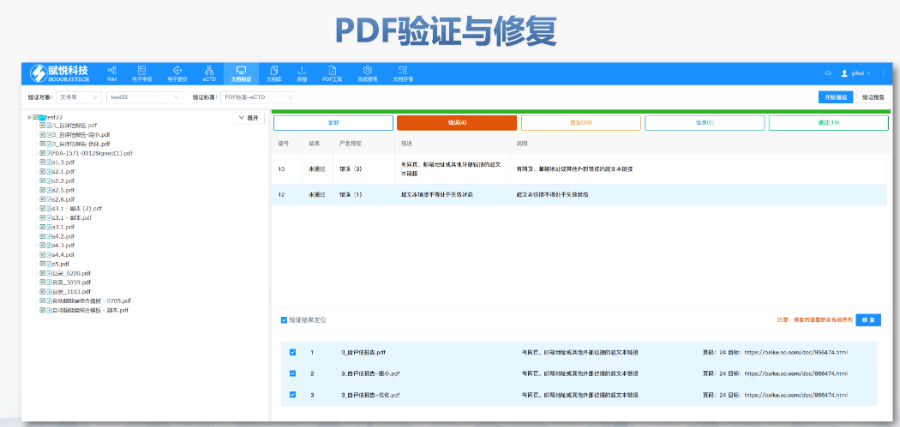
電子簽章與傳輸安全 文件需經(jīng)AES-256加密后刻錄至不可擦寫光盤,,并附MD5校驗(yàn)碼,。光盤損壞或病毒污染將觸發(fā)重遞交流程,原載體按銷毀程序處理,。 ?審評(píng)與核查協(xié)同 自2018年起,,F(xiàn)DA要求提交兩套光盤分別用于審評(píng)和現(xiàn)場(chǎng)核查,2022年調(diào)整為“1套審評(píng)+1套核查+1套專項(xiàng)資料”模式,,提升流程效率,。 ?國際化兼容性增強(qiáng) 美國eCTD系統(tǒng)支持與歐盟、日本等地區(qū)的XML互操作性,,但區(qū)域差異(如模塊1的標(biāo)簽要求)仍需人工適配,。 ?未來通道創(chuàng) FDA計(jì)劃引入API接口支持企業(yè)系統(tǒng)直連,并探索基于云存儲(chǔ)的實(shí)時(shí)提交與審評(píng),,減少物理媒介依賴,。南京原料藥eCTD報(bào)價(jià)加拿大eCTD注冊(cè)外包相關(guān)技術(shù)支持。
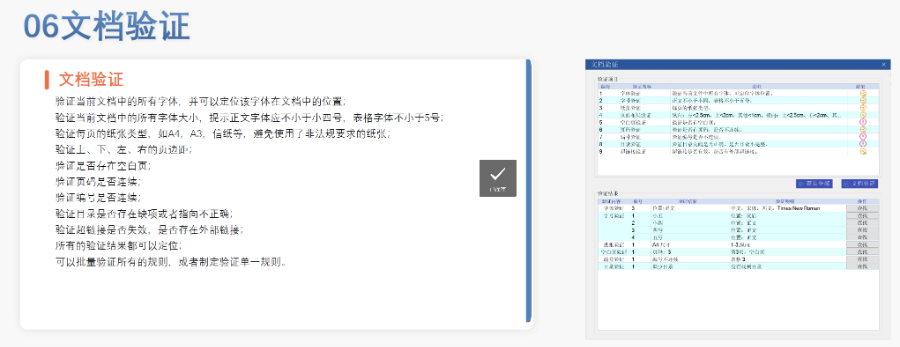
美國于2003年成為全球早采用eCTD(電子通用技術(shù)文檔)的國家之一,,初由CDER和CBER作為電子提交平臺(tái)試點(diǎn),。2008年起,eCTD正式成為藥申請(qǐng)(NDA)和生物制品許可申請(qǐng)(BLA)的標(biāo)準(zhǔn)格式,,并在2012年通過《藥申報(bào)者付費(fèi)法案》(PDUFA)進(jìn)一步強(qiáng)化其法律地位,。至2017年,F(xiàn)DA強(qiáng)制要求所有藥申請(qǐng)(NDA),、簡略藥申請(qǐng)(ANDA)及藥物主文件(DMF)必須采用eCTD格式提交,,標(biāo)志著其從可選到強(qiáng)制的轉(zhuǎn)型。這一進(jìn)程在2018年擴(kuò)展至臨床試驗(yàn)申請(qǐng)(IND),,終實(shí)現(xiàn)全類型藥品注冊(cè)的電子化覆蓋
賦悅Word插件 自主研發(fā)Word插件 快速編輯:整合word常用功能按鈕,,避免頻繁切換菜單;內(nèi)置標(biāo)題、段落,、文字,、目錄、超鏈接等的格式和樣式,,可快速設(shè)置和更文檔的格式 快速鏈接:雙擊或者拖拽的方式,,制作文本超鏈接或者題注超鏈接;可搜索全文關(guān)鍵字,,自動(dòng)制作超鏈接 文檔拆分:可根據(jù)不同的條件將word文件顆?;绶止?jié)符,、頁眉,、頁腳、頁碼范圍和自定義頁碼等 PDF轉(zhuǎn)換:WORD轉(zhuǎn)PDF,,自動(dòng)判斷是否生成書簽,,自動(dòng)鑲嵌所有字體,生成PDF快速網(wǎng)頁瀏覽的PDF,,確保生成的PDF所有屬性符合法規(guī)要求 文檔驗(yàn)證:驗(yàn)證文檔的字體,、字號(hào)、紙張,、頁面布局,、空白頁、頁碼,、編號(hào),、目錄、超鏈接等,,并且可以定位驗(yàn)證結(jié)果 可定制:可根據(jù)用戶需求定制格式和樣式模板歐盟IND注冊(cè)申報(bào)相關(guān)技術(shù)支持,。
澳大利亞的藥品電子通用技術(shù)文檔(eCTD)注冊(cè)申報(bào)體系是澳大利亞y藥品商品管理局(TGA)推動(dòng)藥品審評(píng)現(xiàn)代化的重要舉措。eCTD作為國際通行的電子化注冊(cè)申報(bào)標(biāo)準(zhǔn),,通過結(jié)構(gòu)化數(shù)據(jù)格式(如XML)整合了藥品質(zhì)量,、安全性和有效性的技術(shù)文檔,實(shí)現(xiàn)了從傳統(tǒng)紙質(zhì)遞交向數(shù)字化流程的轉(zhuǎn)型,。根據(jù)TGA要求,,eCTD需遵循通用技術(shù)文檔(CTD)框架,分為五個(gè)模塊:模塊1包含澳洲特定的行政信息(如產(chǎn)品說明書草案和GMP證明),;模塊2為質(zhì)量,、非臨床及臨床研究的綜述與總結(jié);模塊3至模塊5則分別涵蓋藥學(xué),、非臨床和臨床的詳細(xì)數(shù)據(jù),。澳大利亞自2024年起加速推進(jìn)eCTD實(shí)施,要求創(chuàng)新藥注冊(cè)申報(bào)優(yōu)先采用該格式,,以提升審評(píng)效率并支持全球同步申報(bào),。 申報(bào)流程上,企業(yè)需通過TGA指定的電子提交門戶(如eSubmission Gateway)上傳eCTD序列,,并在受理后5個(gè)工作日內(nèi)同步提交紙質(zhì)版模塊1-5資料,。瑞士DMF注冊(cè)申報(bào)相關(guān)技術(shù)支持。閔行區(qū)國產(chǎn)eCTD服務(wù)價(jià)格
中DMF注冊(cè)申報(bào)相關(guān)技術(shù)支持,。中國香港INDeCTD
《中國eCTD驗(yàn)證實(shí)踐手冊(cè)》作為2025年2月發(fā)布的技術(shù)指南(發(fā)布日期見),,為藥品注冊(cè)申請(qǐng)人提供了系統(tǒng)化的eCTD申報(bào)驗(yàn)證操作指引。該手冊(cè)基于《中國eCTD驗(yàn)證標(biāo)準(zhǔn)V1.0》的框架,,重點(diǎn)覆蓋驗(yàn)證流程中的六大關(guān)鍵領(lǐng)域:基礎(chǔ)識(shí)別,、文件/文件夾規(guī)范、ICH骨架文件完整性,、區(qū)域性管理信息校驗(yàn),、研究標(biāo)簽文件(STF)邏輯性及PDF技術(shù)合規(guī)性。手冊(cè)特別強(qiáng)調(diào)對(duì)"錯(cuò)誤警告提示"三級(jí)驗(yàn)證結(jié)果的差異化處理策略,,指導(dǎo)申請(qǐng)人通過賦悅eCTD軟件進(jìn)行元數(shù)據(jù)填報(bào),、STF節(jié)點(diǎn)配置及擴(kuò)展節(jié)點(diǎn)合規(guī)性檢查,同時(shí)針對(duì)中國特有的注冊(cè)類型差異提出模塊化申報(bào)資料準(zhǔn)備方案,。對(duì)于PDF文檔,,手冊(cè)細(xì)化到書簽路徑、超鏈接屬性及字體嵌入等技術(shù)細(xì)節(jié),,確保電子資料符合CDE審評(píng)系統(tǒng)的解析要求,。此外,手冊(cè)還結(jié)合生物制品與化學(xué)藥品的申報(bào)差異,,明確了3.2.R擴(kuò)展節(jié)點(diǎn)的使用限制,,并通過案例解析說明函與申請(qǐng)表生命周期的管理規(guī)則。中國香港INDeCTD
- 吳江區(qū)國際注冊(cè)eCTD 2025-04-20
- 靜安區(qū)eCTD遞交 2025-04-20
- 杭州原料藥eCTD 2025-04-19
- 吳江區(qū)生物制品eCTD名稱 2025-04-19
- 河南eCTD注冊(cè)系統(tǒng) 2025-04-19
- 山東國內(nèi)注冊(cè)eCTD是什么 2025-04-19
- 南京電子申報(bào)eCTD推薦 2025-04-19
- 河北eCTD軟件 2025-04-19
- 寧波國產(chǎn)eCTD服務(wù)電話 2025-04-19
- 杭州電子申報(bào)eCTD注冊(cè)系統(tǒng) 2025-04-19
- 數(shù)字營銷一站式推廣后的運(yùn)營優(yōu)化 2025-04-20
- 湖南液晶屏升降器廠家 2025-04-20
- 上海新能源電池母排測(cè)試系統(tǒng)找誰買 2025-04-20
- 離散行業(yè)軟件商哪個(gè)好 2025-04-20
- 廣東同步時(shí)間系統(tǒng)時(shí)鐘同步設(shè)備 2025-04-20
- 蘇州品牌光解膜私人定做 2025-04-20
- 南京工業(yè)清洗機(jī)銷售 2025-04-20
- 天津雷達(dá)點(diǎn)云激光雷達(dá) 2025-04-20
- 圖形化建模界面系統(tǒng)建模軟件激發(fā)創(chuàng)新潛能 2025-04-20
- 貴州超頻服務(wù)器供應(yīng) 2025-04-20