-
智能檢測(cè)技術(shù)在線路板生產(chǎn)中的應(yīng)用
-
半導(dǎo)體封裝技術(shù)與線路板的結(jié)合
-
微型化趨勢(shì)對(duì)線路板設(shè)計(jì)的影響
-
線路板回收技術(shù)的發(fā)展現(xiàn)狀
-
PCB高頻材料在高頻線路板中的重要性
-
工業(yè) 4.0 背景下線路板制造的轉(zhuǎn)型
-
PCB柔性線路板技術(shù)的進(jìn)展
-
全球供應(yīng)鏈變動(dòng)對(duì)線路板行業(yè)的影響
-
AI 技術(shù)在線路板生產(chǎn)中的應(yīng)用
-
PCB新能源汽車對(duì)線路板技術(shù)的影響
南京eCTD推薦
歐洲藥品管理局:集中審評(píng)程序由歐洲藥品管理局(European Medicines Agency, EMA)負(fù)責(zé)協(xié)調(diào)。 人用藥品委員會(huì):人用藥品委員會(huì)(Committee for Medicinal Products for Human Use, CHMP)負(fù)責(zé)提供科學(xué)意見,。 歐盟委員會(huì):CHMP的意見隨后被提交給歐盟委員會(huì)(European Commission, EC),,由歐盟委員會(huì)做出是否授權(quán)的終決定。這個(gè)決定在整個(gè)歐盟都是具有法律約束力的,。 審批過程: 申請(qǐng)人向EMA提交申請(qǐng),,包括eCTD(電子通用技術(shù)文檔)格式的藥品注冊(cè)文檔。 EMA的CHMP分配一個(gè)科學(xué)評(píng)估團(tuán)隊(duì)(Rapporteur和Co-Rapporteur),,負(fù)責(zé)初步評(píng)估,。 CHMP基于評(píng)估團(tuán)隊(duì)的報(bào)告提供科學(xué)意見。 歐盟委員會(huì)根據(jù)CHMP的意見做出終決定,,批準(zhǔn)或拒絕藥品上市,。 授權(quán)范圍 如果藥品獲得批準(zhǔn),將獲得在整個(gè)歐盟,、冰島,、列支敦士登和挪威有效的上市許可(Central Marketing Authorisation, CMA)。澳大利亞eCTD注冊(cè)外包相關(guān)技術(shù)支持,。南京eCTD推薦

電子簽章與安全性 FDA要求所有PDF文件需經(jīng)數(shù)字簽名,,并通過MD5校驗(yàn)確保傳輸完整性,。簽章需符合21 CFR Part 11的電子記錄規(guī)范,部分情況下允許臨時(shí)放寬(如期間的遠(yuǎn)程簽署),。 ?多模塊協(xié)同驗(yàn)證 模塊1(行政文件)的區(qū)域性元數(shù)據(jù)(如申請(qǐng)類型,、聯(lián)系人信息)需與模塊2-5的內(nèi)容邏輯一致。例如,,生物制品的3.2.R擴(kuò)展節(jié)點(diǎn)命名需遵循特定規(guī)則,,而化學(xué)藥品則禁止使用此類擴(kuò)展。 ?驗(yàn)證工具與流程 主流工具如LORENZ eValidator支持自動(dòng)化驗(yàn)證,,生成包含錯(cuò)誤定位與修復(fù)建議的詳細(xì)報(bào)告,。企業(yè)需在提交前完成內(nèi)部驗(yàn)證,并通過“藥品業(yè)務(wù)應(yīng)用系統(tǒng)”推送受理狀態(tài),。 ?常見問題與規(guī)避策略 高頻錯(cuò)誤包括PDF安全設(shè)置,、書簽鏈接失效、STF(研究標(biāo)簽文件)缺失等,。例如,,未在5.3.1章節(jié)標(biāo)注研究ID會(huì)導(dǎo)致驗(yàn)證警告,需通過說明函解釋,。企業(yè)可通過建立標(biāo)準(zhǔn)化模板庫和預(yù)檢流程降低風(fēng)險(xiǎn),。 ?后續(xù)監(jiān)管與更 FDA定期更驗(yàn)證標(biāo)準(zhǔn)(如2022年增臨床試驗(yàn)數(shù)據(jù)完整性檢查),企業(yè)需通過訂閱官方通知或第三方服務(wù)商獲取動(dòng)態(tài)浙江賦悅科技eCTD文件如何制作美國注冊(cè)鄧白氏號(hào)申請(qǐng)相關(guān)技術(shù)支持,。
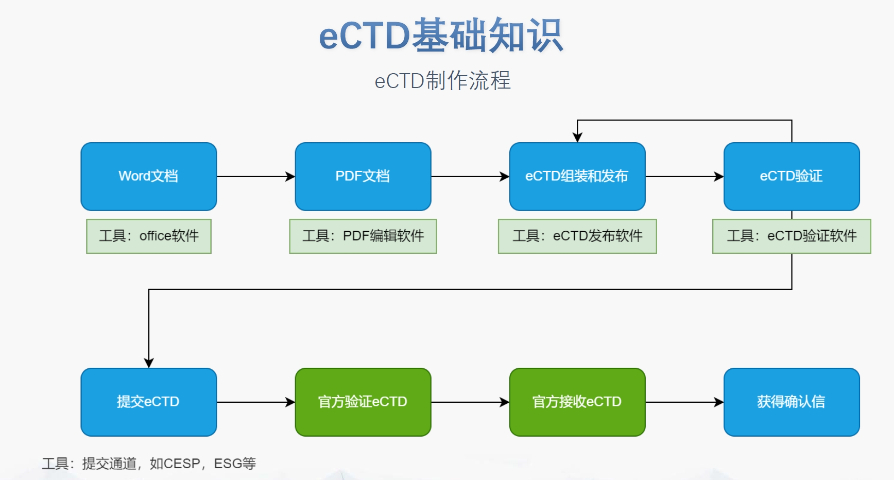
此次eCTD實(shí)施范圍的擴(kuò)大對(duì)外企而言影響,。實(shí)施范圍的擴(kuò)大為外企提供了更多選擇,特別是在產(chǎn)品線中NDA和AND占比相當(dāng)?shù)那闆r下,。外企的系統(tǒng)和流程相對(duì)成熟,,因此它們對(duì)eCTD擴(kuò)大范圍持積極態(tài)度,更愿意嘗試和改變,。盡管過程中可能遇到技術(shù)或法規(guī)上的問題,,但企業(yè)認(rèn)為通過不斷反饋和與CDE溝通,能夠幫助提高整體申報(bào)效率和質(zhì)量,。此外,,外企還面臨向更集成化法規(guī)信息管理系統(tǒng)的挑戰(zhàn),特別是當(dāng)需要遷移到系統(tǒng)時(shí),。如果盡早將產(chǎn)品遷移到eCTD,,無論是系統(tǒng)遷移還是后續(xù)的生命周期管理都會(huì)更加順暢。 隨著eCTD實(shí)施范圍的擴(kuò)大,,供應(yīng)商將擁有更多的業(yè)務(wù)機(jī)會(huì),。然而,中國藥品注冊(cè)體系相對(duì)年輕化,,在推進(jìn)eCTD實(shí)施過程中可能面臨各種問題,。短期內(nèi),,中小企業(yè)可能面臨資金壓力,需要考慮是否投入資金購買的eCTD系統(tǒng),。中長期來看,,企業(yè)更關(guān)注的是如何建立一套完善的文檔管理體系,而不是完成遞交,。這需要企業(yè)在前期投入更多時(shí)間和精力進(jìn)行流程優(yōu)化和人員培訓(xùn),。
電子簽章與傳輸安全 文件需經(jīng)AES-256加密后刻錄至不可擦寫光盤,并附MD5校驗(yàn)碼,。光盤損壞或病毒污染將觸發(fā)重遞交流程,,原載體按銷毀程序處理。 ?審評(píng)與核查協(xié)同 自2018年起,,F(xiàn)DA要求提交兩套光盤分別用于審評(píng)和現(xiàn)場(chǎng)核查,,2022年調(diào)整為“1套審評(píng)+1套核查+1套專項(xiàng)資料”模式,提升流程效率,。 ?國際化兼容性增強(qiáng) 美國eCTD系統(tǒng)支持與歐盟,、日本等地區(qū)的XML互操作性,,但區(qū)域差異(如模塊1的標(biāo)簽要求)仍需人工適配,。 ?未來通道創(chuàng) FDA計(jì)劃引入API接口支持企業(yè)系統(tǒng)直連,并探索基于云存儲(chǔ)的實(shí)時(shí)提交與審評(píng),,減少物理媒介依賴,。eCTD注冊(cè)外包相關(guān)技術(shù)支持。
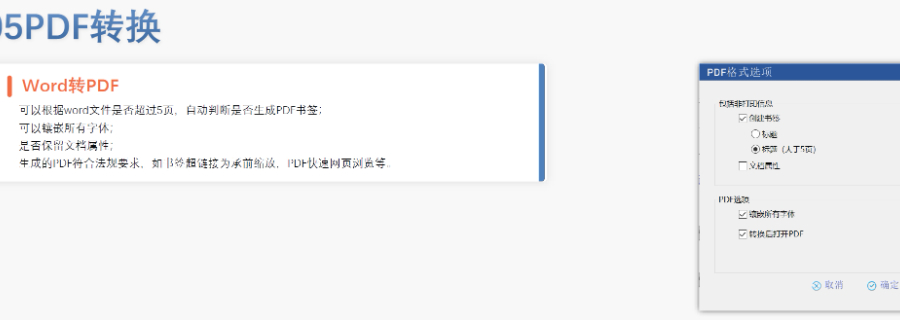
危機(jī)應(yīng)對(duì)與應(yīng)急遞交機(jī)制 在公共衛(wèi)生緊急事件(如COVID-19)中,,EMA允許簡化eCTD序列,,優(yōu)先審評(píng)關(guān)鍵模塊并暫緩非數(shù)據(jù)。申請(qǐng)人可通過快速通道(Fast Track)提交疫苗或藥物的eCTD資料,,審評(píng)周期可壓縮至6個(gè)月,。此類申請(qǐng)需附風(fēng)險(xiǎn)評(píng)估報(bào)告,并承諾后續(xù)補(bǔ)交完整數(shù)據(jù),。 數(shù)據(jù)安全與長期存檔 歐盟要求eCTD資料存檔期限至少為藥品上市后30年,,EMA采用分布式存儲(chǔ)和區(qū)塊鏈技術(shù)確保數(shù)據(jù)不可篡改。申請(qǐng)人需定期備份本地副本,,并使用符合GDPR要求的加密傳輸協(xié)議(如AS2)遞交,。歷史數(shù)據(jù)的遷移和格式轉(zhuǎn)換(如NeeS轉(zhuǎn)eCTD)需遵循特定技術(shù)規(guī)范。 環(huán)保效益與可持續(xù)發(fā)展 eCTD取代紙質(zhì)遞交后,,歐盟每年減少約500噸紙張消耗,,審評(píng)流程的數(shù)字化降低碳足跡約30%。虛擬審評(píng)會(huì)議和電子簽名進(jìn)一步減少了差旅需求,,契合歐盟2050碳中和目標(biāo),。未來,,eCTD4.0將通過數(shù)據(jù)壓縮技術(shù)進(jìn)一步降低服務(wù)器能耗。中NDA注冊(cè)申報(bào)相關(guān)技術(shù)支持,。蕪湖仿制藥eCTD常用解決方案
美國API的DMF申報(bào)相關(guān)技術(shù)支持,。南京eCTD推薦
美國eCTD的強(qiáng)制實(shí)施時(shí)間與范圍:美國自2017年5月5日起要求藥申請(qǐng)(NDA)、仿制藥申請(qǐng)(ANDA)和生物制品許可申請(qǐng)(BLA)必須通過eCTD格式提交,,2018年5月5日進(jìn)一步擴(kuò)展至臨床試驗(yàn)申請(qǐng)(IND)和藥品主文件(DMF),。FDA通過《聯(lián)邦食品、藥品和化妝品法案》第745A條明確電子提交的強(qiáng)制性,,豁免非商業(yè)化IND和部分DMF類型(如Ⅲ類),。2023年數(shù)據(jù)顯示,F(xiàn)DA接收的eCTD申請(qǐng)占比已達(dá)92%,,標(biāo)志著電子化審評(píng)體系的成熟,。企業(yè)若未按規(guī)范提交(如缺少文件或重復(fù)序列號(hào)),將直接被拒收,。南京eCTD推薦
- 高新區(qū)中國eCTD歡迎選購 2025-05-14
- 靜安區(qū)生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區(qū)賦悅科技eCTD供應(yīng)商 2025-05-14
- 南京生物制品eCTD注冊(cè)系統(tǒng) 2025-05-14
- 上?;瘜W(xué)藥品eCTD格式 2025-05-09
- 南京電子申報(bào)eCTD哪個(gè)品牌好 2025-05-09
- 太倉NDAeCTD服務(wù)價(jià)格 2025-05-09
- 浦東新區(qū)原料藥eCTD文件如何制作 2025-04-26
- 南京新藥eCTD找哪家 2025-04-26
- 廣東國產(chǎn)電腦維修怎么用 2025-06-09
- 房山區(qū)不銹鋼機(jī)箱生產(chǎn)廠家 2025-06-09
- 江寧區(qū)高科技iOSAPP開發(fā) 2025-06-09
- 倉儲(chǔ)RFID智能貨架 2025-06-09
- 福建話筒升降器改造調(diào)節(jié) 2025-06-09
- 普陀區(qū)通保三級(jí)通信網(wǎng)絡(luò)安全防護(hù)測(cè)評(píng) 2025-06-09
- 蘇州現(xiàn)代化電話交換系統(tǒng)訂做價(jià)格 2025-06-09
- 現(xiàn)代曝光引流結(jié)構(gòu)設(shè)計(jì) 2025-06-09
- 廣西臺(tái)式電腦租賃定制價(jià)格 2025-06-09
- 北京無線RFID讀卡器報(bào)價(jià) 2025-06-09