天津外泌體提取試劑
外泌體(exosome),,特指直徑在40-100nm的盤狀囊泡,。其主要來源于細(xì)胞內(nèi)內(nèi)溶酶體微粒內(nèi)陷形成的多囊泡體,,經(jīng)多囊泡體外膜與細(xì)胞膜融合后釋放到胞外基質(zhì)中。現(xiàn)已證實(shí)可以分泌外泌體的細(xì)胞有:肥大細(xì)胞,、淋巴細(xì)胞,、樹突狀細(xì)胞、瘤細(xì)胞,、間充質(zhì)干細(xì)胞等,。外泌體在免疫中抗原呈遞、瘤的生長(zhǎng)與遷移,、組織損傷的修復(fù)等生理病理上起著重要的作用,。同時(shí),不同細(xì)胞分泌的外泌體具有不用的組成成分和功能,,可作為疾病診斷的生物標(biāo)志物,。細(xì)胞外囊泡是蛋白質(zhì)、mRNA,、miRNA和脂質(zhì)運(yùn)輸來完成細(xì)胞間通訊通路的重要媒介,,根據(jù)它們的大小和發(fā)生分為三類,包括外泌體,、微泡和凋亡小體,。外泌體的提取、分離方法:超高速離心法,。天津外泌體提取試劑

外泌體(Exosome)是細(xì)胞主動(dòng)分泌的囊泡樣小體,,大小均一,直徑30-200nm,,密度1.10-1.18g/ml,,來源普遍,幾乎所有細(xì)胞都可分泌,,在血液,,尿液,唾液,,腦脊液,,腹水,,乳汁等體液中普遍分布。外泌體較早在1986年發(fā)現(xiàn)于培養(yǎng)的綿羊紅細(xì)胞上清液中,。1996年,,研究者發(fā)現(xiàn)外泌體作為抗原呈遞因子參與T細(xì)胞依賴的抗一些病癥反應(yīng),開啟了外泌體蛋白研究的新天地,。2013年諾貝爾生物/醫(yī)學(xué)獎(jiǎng)解答了細(xì)胞如何組織其內(nèi)部較重要的運(yùn)輸系統(tǒng)之一——囊泡傳輸系統(tǒng)的奧秘,。超離法因操作簡(jiǎn)單,獲得的囊泡數(shù)量較多而廣受?歡迎,,但過程比較費(fèi)時(shí),,且回收率不穩(wěn)定,純度也受到質(zhì)疑,。長(zhǎng)沙正規(guī)外泌體提取試劑推薦廠家外泌體提?。撼x法是較常用的外泌體純化手段,采用低速離心,、高速離心交替進(jìn)行,。

外泌體的提取方法:1、色譜法,。色譜法是利用根據(jù)凝膠孔隙的孔徑大小與樣品分子尺寸的相對(duì)關(guān)系而對(duì)溶質(zhì)進(jìn)行分離的分析的方法,。樣品中大分子不能進(jìn)入凝膠孔,只能沿多孔凝膠粒子之間的空隙通過色譜柱,,首先被流動(dòng)相洗脫出來,;小分子可進(jìn)入凝膠中絕大部分孔洞,在柱中受到更強(qiáng)地滯留,,更慢地被洗脫出。分離到的外泌體在電鏡下大小均一,,但是需要特殊的設(shè)備,,應(yīng)用不普遍。2,、超濾離心,。由于外泌體是一個(gè)大小約幾十納米的囊狀小體,大于一般蛋白質(zhì),,利用不同截留相對(duì)分子質(zhì)量(MWCO)的超濾膜對(duì)樣品進(jìn)行選擇性分離,,便可獲得外泌體。超濾離心法簡(jiǎn)單高效,,且不影響外泌體的生物活性,,是提取細(xì)胞外泌體的一種新方法。
外泌體在肺病進(jìn)程中的作用:在一些病癥微環(huán)境中,,一些病癥細(xì)胞來源的外泌體能夠誘導(dǎo)CD4+T分化為調(diào)節(jié)性T細(xì)胞,,壓制機(jī)體的抗一些病癥免疫反應(yīng),;肺病細(xì)胞分泌的外泌體含有miR-21和miR-29a,可在免疫細(xì)胞中結(jié)合并啟動(dòng)TLR8,,使TLR介導(dǎo)的NF-κB信號(hào)通路活化,,從而導(dǎo)致一些病癥的生長(zhǎng)和轉(zhuǎn)移。在肺病的侵襲和轉(zhuǎn)移過程中,,細(xì)胞間通訊扮演著重要的角色,。據(jù)有關(guān)報(bào)道稱,NSCLC分泌的外泌體內(nèi)TGFβ和IL10的高表達(dá)與肺病的轉(zhuǎn)移密切相關(guān),。此外,,啟動(dòng)的T細(xì)胞可以通過調(diào)控Fas信號(hào)通路增加基質(zhì)金屬蛋白酶9(MMP9)的表達(dá),進(jìn)而促進(jìn)肺病的轉(zhuǎn)移,。這些機(jī)制有望成為肺病治病的潛在靶點(diǎn),。雖然大多數(shù)外泌體都是促進(jìn)一些病癥的侵襲與轉(zhuǎn)移,但也有報(bào)道稱,,外泌體miR-302b可以通過壓制TGFβRⅡ來壓制肺病細(xì)胞的轉(zhuǎn)移與增殖,。如純度和回收率低,雜蛋白較多(假陽性),,顆粒大小不均一,,產(chǎn)生難以去除的聚合物使用可截留100KD分子量的膜,通過離心截留上清中的外泌體,,截留完成后,。
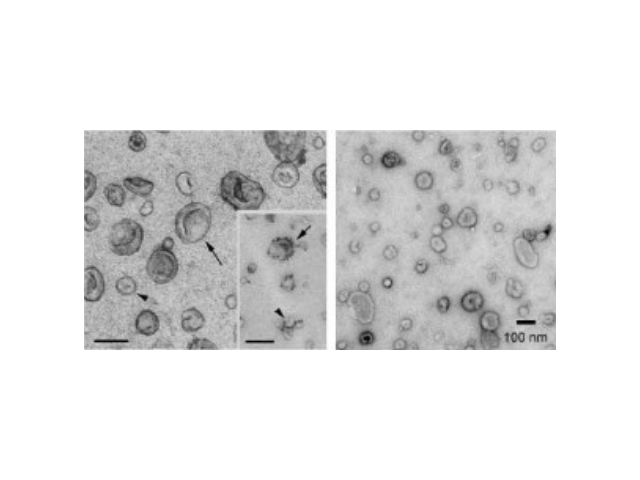
作為一種分子通斷開關(guān)的KRAS發(fā)生突變時(shí)會(huì)處于“開啟”狀態(tài)。在80%~95%的胰腺導(dǎo)管腺?。≒DAC)當(dāng)中,,這個(gè)基因發(fā)生突變,這也是這種一些疾病中較為常見的突變,。這些研究人員證實(shí)iExosome能夠運(yùn)送特異性地靶向KRAS的siRNA和shRNA分子,,并且比他們的合成對(duì)應(yīng)物脂質(zhì)體(liposome)更加高效。脂質(zhì)體不具有外泌體表現(xiàn)出的天然復(fù)雜性和優(yōu)勢(shì),。德州大學(xué)MD安德森一些疾病中心一些疾病生物學(xué)助理教授ValerieLeBleu博士說,,“我們的研究提示著與脂質(zhì)體相比,外泌體表現(xiàn)出運(yùn)送siRNA分子和壓制侵襲性胰腺瘤生長(zhǎng)的優(yōu)異能力,。我們也證實(shí)外泌體表面上的CD47存在允許它們躲避來自循環(huán)單核細(xì)胞的吞噬作用,。”此提取方法條件復(fù)雜,,成本高,。珠海正規(guī)外泌體提取試劑廠家
外泌體的提取、分離方法:尺寸排阻色譜法和超濾法,。天津外泌體提取試劑
外泌體表面有其特異性標(biāo)記物(如CD63,、CD9蛋白),,用包被抗標(biāo)記物抗體的磁珠與外泌體囊泡孵育后結(jié)合,即可將外泌體吸附并分離出來,。磁珠法具有特異性高,、操作簡(jiǎn)便、不影響外泌體形態(tài)完整等優(yōu)點(diǎn),,但是效率低,,外泌體生物活性易受pH和鹽濃度影響,不利于下游實(shí)驗(yàn),,難以普遍普及,。聚乙二醇(PEG)可與疏水性蛋白和脂質(zhì)分子結(jié)合共沉淀,早先應(yīng)用于從血清等樣本中收集菌類,,現(xiàn)在也被用來沉淀外泌體,,其原理可能與競(jìng)爭(zhēng)性結(jié)合游離水分子有關(guān)。利用PEG沉淀外泌體存在不少問題:比如純度和回收率低,,雜蛋白較多(假陽性),,顆粒大小不均一,產(chǎn)生難以去除的聚合物,,機(jī)械力或者吐溫-20等化學(xué)添加物將會(huì)破壞外泌體等,,因此發(fā)表文章時(shí)易受質(zhì)疑,。如純度和回收率低,,雜蛋白較多(假陽性),顆粒大小不均一,,產(chǎn)生難以去除的聚合物,。天津外泌體提取試劑
- 寧波正規(guī)無血清細(xì)胞凍存液 2025-04-20
- 蘇州正規(guī)無血清細(xì)胞凍存液哪家便宜 2025-04-20
- 廣州正規(guī)RNA提取試劑廠家推薦 2025-04-20
- 貴陽無血清細(xì)胞凍存液?jiǎn)蝺r(jià) 2025-04-19
- 蕪湖正規(guī)RNA提取試劑進(jìn)貨價(jià) 2025-04-19
- 珠海無血清細(xì)胞凍存液直銷價(jià) 2025-04-19
- 北京正規(guī)外泌體提取試劑銷售廠家 2025-04-19
- 深圳RNA提取試劑銷售廠家 2025-04-19
- 南京正規(guī)RNA提取試劑哪家便宜 2025-04-19
- 杭州RNA提取試劑服務(wù)電話 2025-04-19
- 飛機(jī)零件碳?xì)淝逑磩┕?yīng) 2025-04-20
- 蘇州正規(guī)無血清細(xì)胞凍存液哪家便宜 2025-04-20
- 窗戶密封膠條生產(chǎn) 2025-04-20
- 廣州正規(guī)RNA提取試劑廠家推薦 2025-04-20
- 發(fā)泡密封膠條推薦廠家 2025-04-20
- 臺(tái)州復(fù)合木地板鋪裝膠品牌 2025-04-20
- 南通復(fù)配營(yíng)養(yǎng)預(yù)混料飲料供應(yīng)企業(yè) 2025-04-20
- 惠州全合成水性清洗劑代加工 2025-04-20
- 石家莊5N碲粒廢料回收 2025-04-20
- 南京MS改性密封膠供貨商 2025-04-20