海南等滲條件中鹽核酸酶
慢病毒載體既可以轉(zhuǎn)導(dǎo)分裂細(xì)胞也可以轉(zhuǎn)導(dǎo)非分裂細(xì)胞,被認(rèn)為是安全的,,并且可以提供長期的轉(zhuǎn)基因表達(dá),,是目前較通用的基因轉(zhuǎn)移方法之一。因慢病毒載體能有效地轉(zhuǎn)導(dǎo)靶細(xì)胞,,如造血干細(xì)胞和T細(xì)胞,在細(xì)胞和基因藥物中的應(yīng)用越來越guang泛,。源自人類胚胎腎細(xì)胞的HEK293細(xì)胞系是成熟的生產(chǎn)LV的系統(tǒng),,因為它們非常適合懸浮培養(yǎng)并且易于轉(zhuǎn)染。在無血清培養(yǎng)基中的懸浮培養(yǎng)在大規(guī)模生產(chǎn)中具有優(yōu)勢,,因為它消除了批次之間的差異并降低了不定因子污染的風(fēng)險,。M-SAN HQ ELISA kit規(guī)格是12*8 strip,提高使用效率,。海南等滲條件中鹽核酸酶
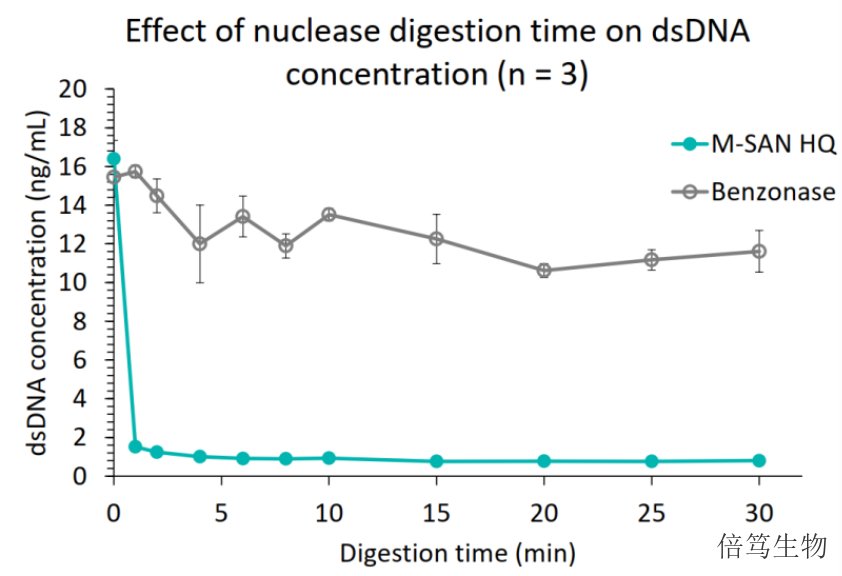
對于含包膜的病毒載體,,如慢病毒LV,、逆轉(zhuǎn)錄病毒RV等,在細(xì)胞培養(yǎng)上清液中收獲,。而M-SAN HQ中鹽核酸酶,,作為市場上更適合生理鹽條件的核酸酶,所以,,M-SAN HQ成了包膜病毒載體生產(chǎn)的更好選擇,。優(yōu)勢在于:1. M-SAN HQ兼容多種細(xì)胞培養(yǎng)體系,在細(xì)胞培養(yǎng)鹽濃度條件下具有更優(yōu)活性,;2. M-SAN HQ酶活更高,、酶切速度更快,縮短孵育時間,;3. M-SAN HQ能夠高效剪切染色質(zhì)到更小片段,,簡化下游工藝流程;4. 相比Benzonase,,M-SAN HQ用量減少1/2-2/3,,降低了酶用量及生產(chǎn)成本。云南中鹽核酸酶70950M-SAN HQ中鹽核酸酶用在生產(chǎn)工藝流程中,,在生理鹽條件下去除雙鏈及單鏈的DNA及RNA,。
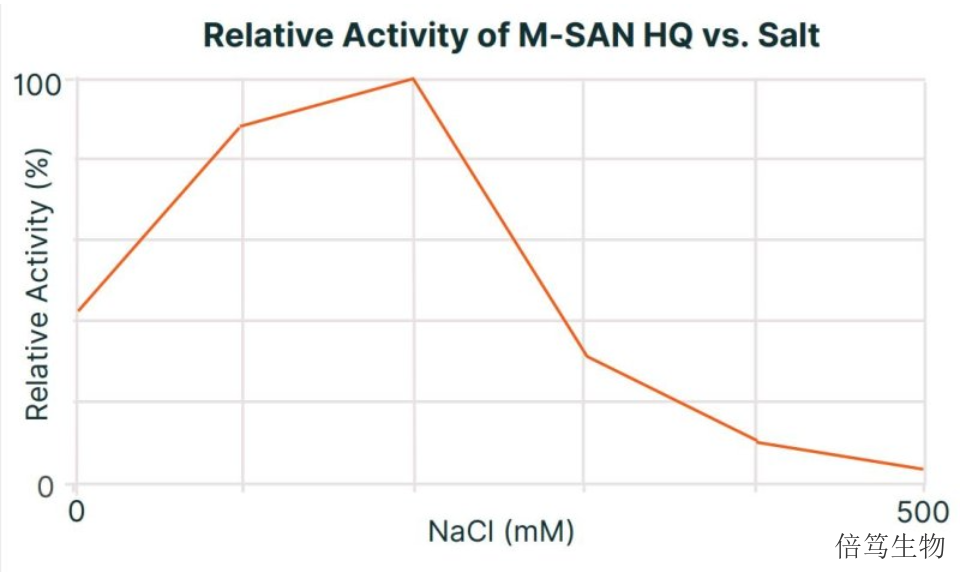
宿主細(xì)胞DNA殘留的擔(dān)憂是基于致ai風(fēng)險理論,特別是生產(chǎn)細(xì)胞系所包含的致ai序列,,比如較常見腺病毒基因E1A和E1B(HEK293, PerC.6 和CAP 細(xì)胞系),,人乳tou瘤病毒E6和E7基因(HeLa細(xì)胞系)等。當(dāng)使用致ai細(xì)胞系生產(chǎn)AAV時,,下游純化須盡可能減少殘留DNA,。工業(yè)上一般使用核酸酶分解殘留DNA,普遍認(rèn)為小于200 bp的DNA片段可有效降低致ai風(fēng)險,。宿主細(xì)胞蛋白殘留與免疫原性,、炎癥或過敏性休克有關(guān)。盡管與非人類的生產(chǎn)原料相比(非人類細(xì)胞系如BHK21或昆蟲細(xì)胞,,以及輔助病毒如HSV,、腺病毒、桿狀病毒),,人類細(xì)胞免疫原性比較弱,。
逆轉(zhuǎn)錄病毒載體可以將7.5Kb左右外源基因整合入靶細(xì)胞基因組,,并穩(wěn)定持久地表達(dá),,已經(jīng)在批準(zhǔn)的CAR-T產(chǎn)品和許多臨床產(chǎn)品中得到應(yīng)用。Shou個成功的基因藥物臨床試驗是利用小鼠白血病病毒(Murin Leukemia Virus,MLV,,gamma逆轉(zhuǎn)錄病毒)作為基因轉(zhuǎn)移載體醫(yī)治兒童的X性染色體連鎖嚴(yán)重聯(lián)合免疫缺陷(SCID-X1),。目前上市的6個細(xì)胞藥物產(chǎn)品全部采用逆轉(zhuǎn)錄病毒(3個為gamma逆轉(zhuǎn)錄病毒載體,,3個慢病毒載體)作為基因轉(zhuǎn)移載體。逆轉(zhuǎn)錄病毒載體目前常用的主要有兩個:gamma逆轉(zhuǎn)錄病毒載體(Retroviral vector,RV)和慢病毒載體(Lentivirus vector,LV),。兩種病毒均屬于逆轉(zhuǎn)錄病毒科,,在自身攜帶的逆轉(zhuǎn)錄酶催化下將其正鏈RNA均逆轉(zhuǎn)錄為cDNA。病毒顆粒比較大,,約為100nm(70-100nm,,有的至200nm),外層為表面突起的脂蛋白套膜,套膜內(nèi)為20面體的衣殼(capsid),核衣殼內(nèi)由一螺旋結(jié)構(gòu)的核酸,。相比全能核酸酶,,M-SAN HQ中鹽核酸酶能將HCD酶切成更小片段,破壞核小體結(jié)構(gòu),。
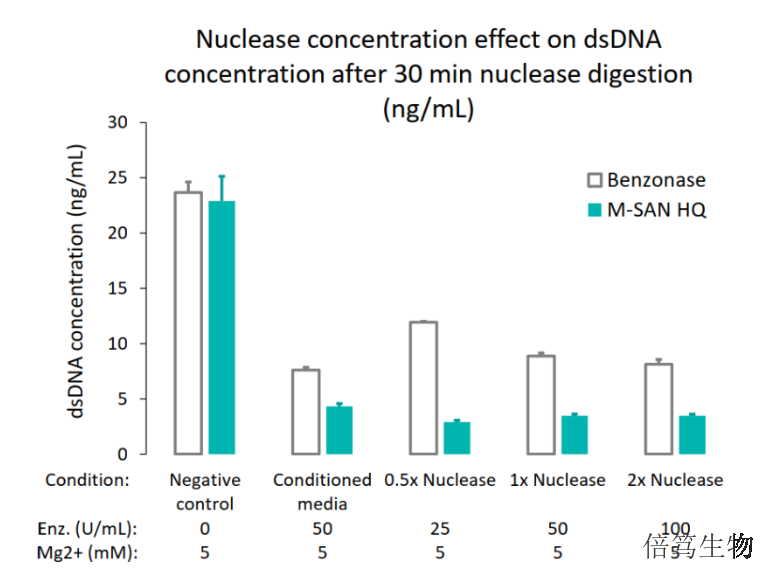
殘留的宿主DNA是生產(chǎn)中產(chǎn)生的雜質(zhì),,其存在潛在的致瘤性、傳染性和免疫原性等風(fēng)險,。相關(guān)研究表明,,基因的大小普遍在200bp以上,因此大于200bp有可能會有一定的致病性,,而且殘留DNA片段越大,,生物制品的風(fēng)險等級越高。因此,,各國監(jiān)管機(jī)構(gòu)對其提出了嚴(yán)格要求。美國食品藥品監(jiān)督管理局(FDA)在《關(guān)于人類基因zhiliao新產(chǎn)品生產(chǎn)指導(dǎo)文件》中明確指出HCD的片段要小于200bp,。2022年5月,,國家藥品監(jiān)督管理局藥品評審中心(CDE)發(fā)布的《體內(nèi)基因藥物產(chǎn)品藥學(xué)研究與評價技術(shù)指導(dǎo)原則(試行)》中也明確指出需對DNA殘留量和殘留片段大小進(jìn)行控制,建議盡量將DNA殘留片段的大小控制在200bp以下,。中鹽核酸酶的生產(chǎn)在符合ISO13485:2016體系基礎(chǔ)上,,增加了cGMP相應(yīng)要求,。湖南等滲條件中鹽核酸酶70950-202
中鹽核酸酶具有純度高(≥99%),、 內(nèi)毒水平低(<0.25EU/1kU)的特點(diǎn);海南等滲條件中鹽核酸酶
在生物工藝中,,核酸酶的主要作用是高效消化宿主細(xì)胞DNA(HCD),,并將其分解成足夠小的片段,以便在下游純化過程中去除,。雖然大多數(shù)核酸酶可以在生理鹽條件下高效地將裸DNA降解成微小片段,,比如Benzonase和SANs都可以把dsDNA分解成小于8nt的寡核苷酸鏈,但實際生產(chǎn)中的核酸污染情況更加復(fù)雜,。HCD通常以染色質(zhì)形式存在,,與細(xì)胞裂解碎片,、病毒顆粒等結(jié)合在一起,影響核酸酶的識別及剪切,。因此,,HCD去除的關(guān)鍵在于——核酸酶如何在復(fù)雜的生產(chǎn)體系中識別并剪切HCD。海南等滲條件中鹽核酸酶
- 青海智能中鹽核酸酶國內(nèi)代理 2025-06-20
- 云南進(jìn)口高鹽核酸酶廠家直銷 2025-06-20
- 鋼城區(qū)70921-202高鹽核酸酶銷售電話 2025-06-20
- 中鹽核酸酶價格 2025-06-20
- 青海國內(nèi)中鹽核酸酶用途 2025-06-20
- 蘇州高鹽核酸酶報價表 2025-06-20
- 山東特色中鹽核酸酶價格表 2025-06-20
- 無錫高鹽核酸酶銷售電話 2025-06-20
- 河北70950-150中鹽核酸酶 2025-06-20
- 萊蕪區(qū)70921-202高鹽核酸酶價格優(yōu)惠 2025-06-20
- 淮安國內(nèi)人工智能輔助診斷設(shè)備戰(zhàn)略 2025-06-22
- 廣州附近哪里有太空艙按摩椅有哪些 2025-06-22
- 崇明區(qū)推薦醫(yī)療軟件戰(zhàn)略 2025-06-22
- 賽多利斯血小板裂解液廠家 2025-06-22
- 供注射用交聯(lián)透明質(zhì)酸 2025-06-22
- 哈爾濱市便攜式隨訪一體機(jī)廠家電話 2025-06-22
- 貴陽奧托博克GeniumX3大腿智能假肢 2025-06-22
- 溫州組合吊塔 2025-06-22
- 云南二類械字號貼膏供應(yīng) 2025-06-22
- 人類胰島素抵抗檢測試劑盒 2025-06-22